 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Окислительно-восстановительные свойства. Реакции присоединения с-нуклеофилов к карбонильным соединениям являются окислительно-восстановительными
|
|
Реакции присоединения С-нуклеофилов к карбонильным соединениям являются окислительно-восстановительными, так как они сопровождаются изменением степеней окисления углеродных атомов.
Присоединение цианид-аниона. Синильная кислота в присутствии следов щелочи очень легко присоединяется к карбонильным соединениям с образованием а-гидроксинитрилов (циангидринов). При этом карбонильный атом углерода, являясь электрофильным центром, выступает окислителем, а углеродный атом цианид-аниона - нуклеофил - выступает восстановителем:

Щелочь необходима для получения из слабой, малодиссоцирующей циановодородной (синильной) кислоты активного нуклеофила - цианид-аниона CN-. Эта реакция применяется для нейтрализации отравления синильной кислотой, для чего обычно используют глюкозу, молекула которой содержит альдегидную группу. Для дегазации паров синильной кислоты в помещении их обрабатывают формальдегидом или формалином:

Конденсации альдольная и кротоновая. В молекулах карбонильных соединений имеется еще один реакционный центр - а-углеродный атом, соединенный с водородным атомом, обладающим некоторой протонной подвижностью. Под действием оснований этот водородный атом отщепляется с образованием соответствующего карбаниона, который, являясь активным С-нуклеофилом (восстановитель), присоединяется к электрофильному центру карбонильной группы 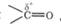 другой молекулы, выступающей окислителем. На примере взаимодействия двух молекул ацет-альдегида эта реакция выглядит так:
другой молекулы, выступающей окислителем. На примере взаимодействия двух молекул ацет-альдегида эта реакция выглядит так:

Продукт реакции содержит и альдегидную и спиртовую группу, поэтому он называется альдолем, а реакция – альдольной конденсацией. Эта реакция, как видно по изменению степеней окисления углеродных атомов, является окислительно-восстановительной.
Альдоли, содержащие подвижный а-водородный атом, в присутствии сильных щелочей или при нагревании легко отщепляют воду, превращаясь в непредельные альдегиды:

Реакция альдольной конденсации альдегидов или кетонов, сопровождаемая отщеплением воды, называется кротоновой конденсацией, которая также является окислительно-восстановительным процессом.
Реакции типа альдольной и кротоновой конденсации позволяют на базе различных карбонилсодержащих метаболитов (альдегидов и кетонов) увеличивать длину углеродной цепи и синтезировать новые метаболиты. Так, в клетках растений осуществляется биосинтез фруктозо-1,6-дифосфата из фосфата глицеринового альдегида и фосфата диоксиацетона при участии фермента альдолазы:

Реакция поликонденсации формальдегида с фенолом с получением фенолформальдегидных полимеров уже рассмотрена (разд. 17.4). В этой окислительно-восстановительной реакции карбонильный атом углерода формальдегида выступает электрофилом (окислителем), а атомы углерода фенола - нуклеофилом (восстановителем).
 |
Окисление а-углеродного атома. Подвижность атомов водорода у а-углеродного атома в карбонильных соединениях позволяет последовательно заместить их при хлорировании. Так, при хлорировании ацетальдегида последовательно замещаются все три а-водородных атома с образованием хлораля:
Карбонильные соединения,содержащие ацетильную группу, реагируют с иодом в щелочном растворе, образуя йодоформ CHI3 - желтое нерастворимое в воде вещество - и
 |
соль карбоновой кислоты:
Поскольку вторичные спирты окисляются иодом до кетона, то эта реакция также протекает с вторичными спиртами, содержащими метильную группу в а-положении. Таким образом, ио-доформная реакция является диагностическим тестом на группы
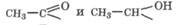 в молекулах органических соединений.
в молекулах органических соединений.
 |
а-Галогензамещенные альдегиды и кетоны -сильные лакриматоры (от лат. lacrima - слеза). Например, хлорацетофенон уже при концентрации 0,003 мг/л вызывает слезотечение, а концентрация 0,004 мг/л считается непереносимой. Это вещество под названием "черемуха" используется для борьбы с нарушителями правопорядка.
Реакция дисмутации. Альдегиды, не способные к реакции альдольной конденсации из-за отсутствия а-водородного атома, под действием щелочи вступают в реакцию межмолекулярной окислительно-восстановительной дисмутации с образованием соответствующих спирта и соли карбоновой кислоты:

Окисление альдегидов. Альдегиды, в отличие от кетонов, легко окисляются мягкими окислителями: оксидом серебра или гидроксидом меди(2). Это качественные реакции на альдегидную группу. Реакция альдегида с аммиачным раствором ок сида серебра (реактив Толленса) сопровождается появлением "серебряного зеркала":

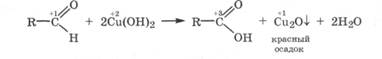
При нагревании альдегида со щелочным раствором гидроксида меди(П) (реактив Фелинга) образуется красный осадок оксида меди(1):
Окисление кетонов. Кетоны кислородом воздуха или слабыми окислителями не окисляются. Под действием сильных окислителей - перманганатов или дихроматов - молекула кетона, окисляясь, расщепляется по связи С—С у карбонильной группы с образованием молекул кислот с меньшим числом углеродных атомов: 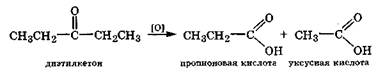
Биологическое окисление. В организме альдегиды обычно окисляются под действием окисленной формы кофермента НАД+, в которой окислителем являются атомы углерода пиридинового кольца (разд. 9.3.3). Так, глицеральдегид-3-фосфат, при участии фосфорной кислоты, окисляется НАД+ в 3-фосфоглицероил-фосфат:

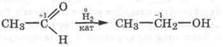 |
Восстановление альдегидов и кетонов. При действии на карбонильные соединения сильных восстановителей, например водорода в присутствии катализаторов (Ni, Pt, Pd), происходит гидрирование карбонильной группы. При этом альдегиды восстанавливаются в первичные спирты:
Кетоны восстанавливаются во вторичные спирты:

В организме восстановление (гидрирование) альдегидов и кетонов до спиртов осуществляется ферментативно под действием восстановленных форм коферментов НАД(Н) или ФАД(2Н), в которых роль восстановителя выполняют их углеродные атомы (разд. 9.3.3).

Дата публикования: 2014-10-16; Прочитано: 3635 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
