 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Способы обозначения оптически активных молекул
|
|
В течение многих лет конфигурация стереоизомеров обозначалась символами D и L, чтобы связать их конфигурацию с конфигурацией 2,3- дигидроксипропаналя (глицеринового альдегида).
 |
D(+) глицериновый альдегид L(-) глицериновый альдегид. Энантиомеры 2,3-дигидроксипропаналя (глицеринового альдегида)
Если конфигурация хирального центра изучаемой молекулы совпадала с конфигурацией (+) глицеринового альдегида, то ей приписывалась D-конфигурация, если имела противоположную, т.е. совпадала с (-) -глицериновым альдегидом, - то L- конфигурацию. В настоящее время правильность произвольно выбранной конфигурации для (+) глицеринового альдегида подтверждена рентгеноструктурным анализом и приобрела силу абсолютной конфигурации. Глицериновый альдегид был выбран первоначально в качестве соединения сравнения, ”стандарта”, по той причине, что его можно было превратить во многие другие встречающиеся в природе соединения. Например (+)глицериновый альдегид можно превратить в (-) молочную кислоту рядом последовательных реакций, не затрагивающих хиральный центр.
 |
D(+) -глицериновый альдегид D(-) -молочная кислота
Схема синтеза (-) молочной кислоты из (+) глицеринового альдегида
Таким образом, обе эти молекулы имеют одинаковую конфигурацию (D), хотя знаки их вращения разные. Заглавные буквы D и L стали символами первой стереохимической номенклатуры. В настоящее время она широко используется в химии углеводов и аминокислот. Например, аминокислоты, входящие в состав белков, относятся к L-ряду.По этой номенклатуре L-конфигурация приписывается тому стереоизомеру, у которого NH2- группа находится слева от вертикальной прямой на проекции Фишера, при условии, если окисленная группа располагается вверху.
 |
L - изомер D-изомер
В природе наиболее распространены углеводы, относящиеся к D-ряду. Отнесение к D-ряду углеводов производится по расположению самой нижней гидроксильной группы, связанной с асимметрическим атомом углерода.
 |
D-глицериновый D-глюкоза
альдегид
D и L система используется часто и в настоящее время, но с помощью этой системы можно обозначить только конфигурацию одного хирального центра. В 1951 году была предложена универсальная стереохимическая номенклатура, позволяющая обозначить любое число хиральных центров. Согласно правилам этой системы, можно дать название стереоизомеру как по проекционной формуле, так и по молекулярной модели, и, наоборот, воспроизвести проекционную формулу. Для обозначения хиральных центров используют символы R и S. Чтобы обозначить хиральный центр соответствующим символом R или S, определяют старшинство заместителей при асимметрическом атоме углерода. Предположим, что старшинство заместителей падает в следующей последовательности: a > b > c > d. Тетраэдрическую модель располагают таким образом, чтобы младший заместитель находился в удаленном от глаза наблюдателя углу тетраэдра. Затем на молекулу смотрят со стороны, удаленной от младшего заместителя. Если при этом старшинство заместителей уменьшается по часовой стрелке (от старшего заместителя к младшему), то такому хиральному центру приписывают символ R, а если против часовой стрелки - то S.
 |
Старшинство групп уменьшается Старшинство групп уменьшается по часовой стрелке против часовой стрелки
Порядок старшинства заместителей определяется следующим образом:
1Атомы, непосредственно связанные с хиральным центром, располагаются в порядке уменьшения их атомных номеров, например: Br > Cl > C > H.
2. Если два или более атомов, непосредственно связанных с хиральным центром, одинаковы, то порядок старшинства определяется атомными номерами следующего слоя:
CH2OH > CH2NH2 > CH3CH2 > CH3
3.Если атом, связанный с хиральным центром, имеет кратные связи, то атом на другом конце кратной связи считается дважды (для двойной связи) или трижды (для тройной связи):
COOH > COH > CH2OH
Более удобно использовать не тетраэдрические модели, а проекционные формулы Фишера. Для этого надо спроектировать модель на плоскость таким образом, чтобы младший заместитель оказался внизу на проекции, а путем четного числа перестановок при хиральном центре добиться их такого расположения, чтобы оно совпадало со старшинством заместителей.
На основании приведенных выше правил и старшинства заместителей вокруг асимметрического атома углерода определим конфигурацию для природной аминокислоты – аланина. Природная аминокислота относится к L-ряду и может быть представлена следующей проекцией Фишера:
CH3-C*H(NH2) –COOH
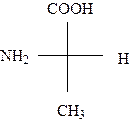 |
L ряд
Хиральный атом связан непосредственно с атомами водорода, азота и двумя атомами углерода. Таким образом можно определить самый старший заместитель (амино-группа) и самый младший (водород). Два других заместителя (CH3 и COOH) имеют одинаковый атомный номер. Для определения их старшинства необходимо учитывать атомные номера атомов, с которыми непосредственно связаны эти заместители. COOH>CH3, и мы получаем такой ряд старшинства заместителей: NH2 > COOH > CH3 > H
Чтобы обозначить конфигурацию аланина в системе “R,S,” необходимо преобразовать проекцию Фишера. Для этого производим первую перестановку, меняя местами H и CH3 (младший заместитель должен быть внизу). Смотрим на проекцию, старшинство не нарушено, но мы сделали одну перестановку (запрещено правилами пользования проекциями Фишера), поэтому мы обязаны сделать вторую (меняем местами группы NH2 и CH3). Мы сделали четное число операций, первая и последняя проекция изображают один и тот же стереоизомер. Определяем падение старшинства заместителей. В данном случае он происходит против часовой стрелки. Природный аланин по системе “R,S” называется 2-(S) -аминопропановая кислота.

L после 1пере- после 2-ой S
становки перестановки
С помощью этой номенклатуры можно дать название для любой молекулы. Так, приведенные выше 2,3-дигидроксибутандиовые кислоты могут быть названы следующим образом: 1- 2(R),3(R) -дигидроксибутандиовая-1,4-кислота; 2-2(S)3(S)-дигидроксибутандиовая-1,4-кислота и 3 изомер- мезовинная кислота- 2-(R),3(S)- дигидроксибутандиовая -1,4-кислота.
Дата публикования: 2014-10-25; Прочитано: 2088 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
