 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Роль аммиака для живых организмов и пути его обезвреживания. ЦИКЛ мочевины и ее свойства
|
|
Химические свойства аммиака и алифатических аминов уже были рассмотрены в разд. 12.2.4. В молекулах этих соединений неподеленная электронная пара атома азота находится на sp3-орбитали, поэтому для нее характерна предельная подвижность, а для аммиака и аминов - высокая основность, нуклеофильность и склонность к комплексообразованию как лигандов. Именно эти особенности химических свойств характерны и для природных аминокислот, так как они содержат «аминный» атом азота (гл. 21). Синтез аминокислот в природе осуществляется в растениях и микроорганизмах, которые ассимилируют простейшие азотсодержащие соединения (аммиак и нитраты) и восстанавливают их до аммиака, используя его для синтеза жизненно важных аминокислот, белков, гетероциклических азотсодержащих соединений и нуклеиновых кислот. Эти ценные природные вещества в готовом виде как продукты питания достаются животным. Большинство организмов экономно используют аминокислоты и нуклеотиды, пропуская их через процессы метаболического обновления, что позволяет использовать их повторно.
Вследствие особенностей метаболизма у животных, в частности дезаминирования аминокислот, в их организмах появляется аммиак. В норме концентрация аммиака поддерживается в крови у человека на уровне 0,4 - 0,7 мг/л. При рН крови аммиак существует почти полностью в виде катиона аммония. Ионы NH4(+), будучи заряженными частицами, с большим трудом проникают через клеточные мембраны. Диссоциация катиона аммония (как сопряженной кислоты с отщеплением протона и образованием аммиака) протекает слабо — pKa(NH4(+))= 9,25. Следовательно, аммиак является сильным акцептором протона. По этой причине, а также из-за склонности к комплексообразованию аммиак хорошо растворяется в воде, образуя малоустойчивое соединение NH3 • H2О - межмолекулярный ассоциат (разд. 12.2.4).
В отличие от катионов аммония, молекулы аммиака в виде ассоциата с молекулой воды легко проходят сквозь мембраны и способны проникать в клетки мозга, а также в их митохондрии. В результате замедляются реакции дезаминирования глутаминовой кислоты с образованием 2-оксоглутарата (разд. 21.2.5). Следовательно, снижается интенсивность реакций: цикла Кребса (разд. 19.4.3), завершения окисления глюкозы (разд. 22.1.2) и синтеза АТФ (разд. 9.3.4), обеспечивающих мозг энергией. Кроме того, аммиак, попадая в нервные ткани, вступает в реакции комплексообразования с катионами биометаллов, нарушая металло-лигандный гомеостаз в этих тканях (разд. 10.5). Все это свидетельствует о токсичности излишка аммиака для животных, поэтому для них проблема удаления из организма токсичного аммиака чрезвычайно важна.
У костных рыб аминный азот транспортируется в виде глутамина в жабры, где содержится глутаминаза, катализирующая гидролиз глутамина до глутаминовой кислоты и аммиака. Образовавшийся аммиак сильно разбавляется потоком воды, омывающим жабры, и уносится им. Таким образом, у рыб функционирует простейшая система избавления организма от излишка аммиака.
В процессе эволюции у млекопитающих сформировалась специальная выделительная система из почек и мочевого пузыря. При этом в мочу поступает не аммиак и не катион аммония, а мочевина CO(NH2)2 (в моче человека содержание мочевины около 2 %). Поэтому основной метаболический путь обезвреживания аммиака у млекопитающих заключается в том, что в клетках печени на его основе синтезируется мочевина. Этот синтез совершается в форме цикла и называется циклом мочевины* (открыт Г. Кребсом и К. Хенселантом в 1932 г.).
Цикл мочевины. Начинается этот процесс с получения карбамоилфосфата в матриксе митохондрий, где много АТФ.
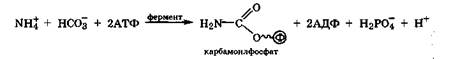 |
I. Образование карбамоилфосфата. Ионы аммония, возникшие в результате окислительного дезаминирования глутаминовой кислоты, взаимодействуют с гидрокарбонат-анионом и АТФ при участии карбамоилфосфатсинтетазы, образуя карбамоилфосфат, содержащий макроэргическую связь:
II. Получение цитруллина. В матриксе митохондрий
карбамоилфосфат конденсируется с аминокислотой орнитином,
которая, являясь гомологом лизина, не входит в состав белков.
Реакция катализируется орнитинкарбамоилтрансферазой:
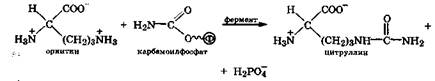
Образовавшийся цитруллин переходит из митохондрий в цитозоль клеток печени, где протекают остальные реакции цикла мочевины.
III. Получение аргининосукцината. Нуклеофильное замещение карбонильной группы цитруллина на аминогруппу аспартата с образованием гуанидиновой группировки аргининосукцината происходит при участии АТФ и катализируется
аргининосукцинатсинтетазой:
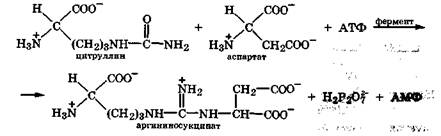
Реакция эндэргоничная, и равновесие смещается вправо за счет последующего гидролиза Н2Р2O7(2-). Таким образом, на протекание первой и третьей реакций цикла мочевины всего расходуется 4 молекулы АТФ.
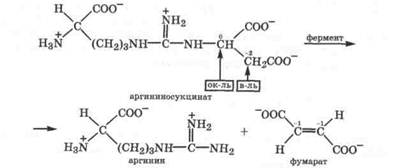 |
IV. Распад аргининосукцината. Под действием аргининосукцинатлиазы аргининосукцинат экзэргонически расщепляется с образованием аргинина и фумарата:
В цикле мочевины это единственная реакция внутримолекулярной дисмутации. Все остальные реакции этого цикла - элек-трофильно-нуклеофильные.
V. Образование мочевины и регенерация ор-нитина. Гидролиз аргинина, катализируемый аргиназой, приводит к образованию мочевины и регенерации орнитина. Реакция экзэргонична. 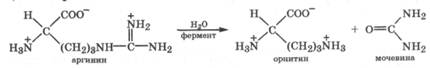
Регенерированный орнитин может снова поступать в митохондрии и участвовать в новом обороте цикла мочевины. Образовавшуюся мочевину кровь переносит из печени в почки, где мочевина извлекается из крови и удаляется из организма с мочой.
Из приведенных реакций видно, что токсичный аммиак превращается в безвредную мочевину. При этом один из атомов азота мочевины образуется из аммиака, другой - из аспартата. Кроме аммиака за счет цикла мочевины организм избавляется еще и от СО2 в виде НСО3. На это очищение от конечных продуктов метаболизма организм расходует 4 молекулы АТФ. Прежде чем рассмотреть особенности обезвреживания аммиака в организме птиц и пресмыкающихся, кратко остановимся на свойствах мочевины.
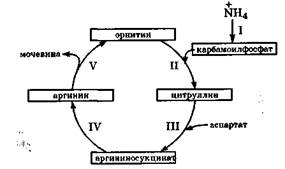
Свойства мочевины. Мочевина является диамидом угольной кислоты, и поэтому ее часто называют карбамидом. В отличие от аммиака, в мочевине у атомов азота их неподеленные электронные пары находятся на 2р-орбитали и участвуют в сопряжении с π-электронами связи С=0. Поэтому основность, нуклеофильность и склонность к комплексообразованию у мочевины понижены. Мочевина является очень слабым основанием; она протонируется по атому кислорода:
 |
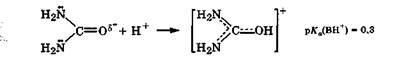
Мочевина легко растворяется в воде, ее растворы имеют нейтральную реакцию. Растворение мочевины в воде происходит с поглощением теплоты.
Мочевина гидролизуется медленно даже при кипячении с водой; процесс ускоряется в присутствии кислот или щелочей:
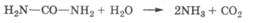
В присутствии фермента уреазы мочевина гидролизуется очень быстро, что очень важно для обмена веществ у животных и круговорота азота в биосфере.
По химическим свойствам мочевина похожа на амиды карбоновых кислот (разд. 19.2.3) с тем отличием, что у мочевины более выражены нуклеофильные и комплексообразующие свойства, так как в ее молекуле карбонильная группа связана с двумя аминогруппами. Мочевина как нуклеофил сравнительно легко ацилируется, образуя азотсодержащие гетероциклические соединения. Ацилирование мочевины малоновой кислотой приводит к барбитуровой кислоте, являющейся пиримидиновым производным:
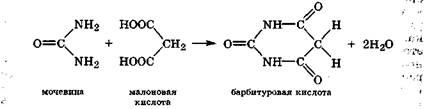
При ацилировании мочевины 5-оксибарбитуровой кислотой образуется мочевая кислота — производное пурина:
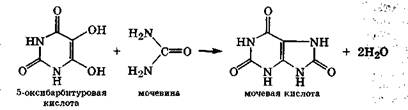
Мочевая кислота и ее соли (ураты) плохо растворимы в воде. Поэтому при нарушениях обмена веществ возможно отложение мочевой кислоты в суставах, что приводит к заболеванию подагрой. Камни мочевого пузыря и почек состоят из мочевой кислоты и ее солей уратов (разд. 11.4).
При нагревании мочевины до 140 °С одна молекула мочевины, отщепляя аммиак, ацилирует другую молекулу мочевины, образуя биурет:
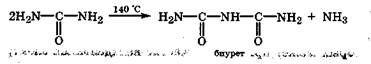
Биурет в щелочной среде с катионами меди(2) дает фиолетовое окрашивание, обусловленное образованием хелатного комплекса (биуретовая реакция):
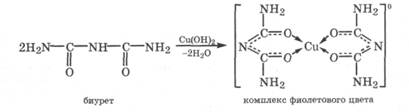 |
Мочевина широко применяется в качестве пролонгированного азотного удобрения и добавки к кормам жвачных животных, у которых в первом отделе желудка (рубец) имеются микроорганизмы, использующие ее для синтеза аминокислот, необходимых организму хозяина. В медицине мочевину применяют в основном в качестве дегидратирующего средства для предупреждения и уменьшения отека мозга и токсического отека легких, а также как средство, понижающее внутриглазное давление. В основе этого эффекта, кроме явления осмоса, вероятно, лежит способность мочевины влиять на пространственную структуру воды в растворе. Дезинфицирующие свойства мочи и использование ее в уринотерапии, возможно, также связаны с особой пространственной структурой воды в ней. Эта структура воды формируется в почечной системе, но при хранении in vitro в результате теплового движения она разрушается, и целебность мочи уменьшается.
Возвратимся к проблеме обезвреживания аммиака у живых существ. В отличие от млекопитающих, организм птиц и пресмыкающихся очищается от аммиака, превращая его сложным путем в мочевую кислоту. Из-за низкой растворимости в воде помет птиц, называемый гуано, представляет собой полутвердую массу, состоящую из кристаллов мочевой кислоты и небольшого количества воды. Богатейшие залежи гуано, используемого как удобрение, сосредоточены в местах гигантских птичьих базаров. В современных условиях источником гуано являются крупные птицефабрики.
Дата публикования: 2014-10-16; Прочитано: 3056 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
