 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задача №19
|
|
Определить направление реакции, приведенной в табл. 2, при температуре Т К (табл. 6) и общем давлении р Па, если число молей неравновесной смеси 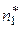 ,
,  (исходные вещества),
(исходные вещества),  ,
, 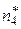 (продукты реакции) даны в табл. 17. Значение константы равновесия при температуре Т взять из задачи №17.
(продукты реакции) даны в табл. 17. Значение константы равновесия при температуре Т взять из задачи №17.
Таблица 17
| Вариант | 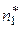
| 
| 
| 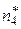
| р ·10–6 , Па |
| 0,5 | 0,2 | 0,3 | – | 9,73 | |
| 0,5 | 0,1 | 0,5 | 0,1 | 9,74 | |
| 0,5 | – | 0,5 | – | 9,75 | |
| 0,25 | 0,25 | 0,25 | 0,25 | 9,73 | |
| 0,3 | 0,2 | 0,2 | 0,3 | 9,73 | |
| 0,25 | 0,35 | 0,15 | 0,25 | 9,73 | |
| 0,6 | – | 0,2 | 0,2 | 9,74 | |
| 0,25 | 0,4 | 0,25 | 0,1 | 9,77 | |
| 0,35 | 0,3 | 0,25 | 0,1 | 9,78 | |
| 0,1 | 0,6 | 0,15 | 0,15 | 9,73 | |
| 0,325 | – | 0,325 | 0,35 | 9,77 | |
| 0,4 | – | 0,3 | 0,3 | 9,77 | |
| 0,3 | 0,3 | 0,4 | – | 9,78 | |
| 0,15 | 0,7 | – | 9,79 | ||
| 0,15 | 0,15 | 0,35 | 0,35 | 9,76 | |
| 0,25 | 0,25 | 0,25 | 0,25 | 9,76 | |
| 0,5 | – | 0,15 | 0,35 | 9,78 | |
| 0,35 | 0,5 | 0,15 | – | 9,79 | |
| 0,5 | 0,4 | 0,1 | – | 9,73 | |
| 0,3 | 0,2 | 0,2 | 0,3 | 9,73 | |
| 0,2 | 0,2 | 0,6 | – | 9,79 | |
| 0,55 | – | 0,15 | 0,3 | 9,74 | |
| 0,35 | 0,55 | 0,1 | – | 9,75 | |
| 0,4 | – | 0,4 | 0,2 | 9,73 | |
| 0,25 | 0,4 | 0,25 | 0,1 | 9,71 | |
| 0,8 | 0,15 | 0,15 | - | 9,77 | |
| 0,3 | – | 0,3 | 0,4 | 9,75 | |
| 0,1 | 0,6 | 0,15 | 0,15 | 9,78 | |
| 0,25 | – | 0,25 | 0,5 | 9,77 | |
| 0,15 | 0,15 | 0,35 | 0,35 | 9,76 |
Решение:
Решение задачи рассмотрим на примере реакции образования аммиака  . Определим направление данной реакции при температуре Т = 800 К и общем давлении р = 9,73·106 Па, если число молей компонентов реакции в исходной неравновесной смеси составило
. Определим направление данной реакции при температуре Т = 800 К и общем давлении р = 9,73·106 Па, если число молей компонентов реакции в исходной неравновесной смеси составило 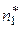 = 0,5;
= 0,5;  = 0,3;
= 0,3;  = 0,2. Значение константы равновесия
= 0,2. Значение константы равновесия  (см. задачу № 17).
(см. задачу № 17).
Установим знак величины  . Воспользуемся уравнением изотермы Вант–Гоффа:
. Воспользуемся уравнением изотермы Вант–Гоффа:
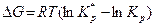 , (63),
, (63),
где  – величина, рассчитываемая по той же формуле, что и
– величина, рассчитываемая по той же формуле, что и 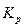 , но для неравновесных условий, как отношение неравновесных парциальных давлений компонентов реакции (
, но для неравновесных условий, как отношение неравновесных парциальных давлений компонентов реакции (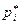 )
)
 .
.
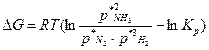 .
.
При анализе уравнения изотермы Вант–Гоффа следует рассмотреть три случая:
1) Если 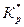 >
> 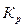 , то
, то 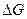 > 0, т.е. реакция идет в обратном направлении в сторону образования исходных веществ.
> 0, т.е. реакция идет в обратном направлении в сторону образования исходных веществ.
2) Если 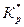 <
< 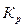 , то
, то 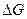 < 0, т.е. реакция идет самопроизвольно в прямом направлении в сторону образования продуктов реакции.
< 0, т.е. реакция идет самопроизвольно в прямом направлении в сторону образования продуктов реакции.
3) Если 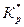 =
= 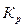 , то
, то 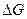 = 0, т.е. система находится в равновесии.
= 0, т.е. система находится в равновесии.
Рассчитаем величину  через
через  – константу, выраженную через мольные доли компонентов в неравновесной исходной смеси.
– константу, выраженную через мольные доли компонентов в неравновесной исходной смеси.
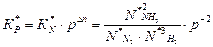 .
.
Для этого рассчитаем величины мольных долей компонентов неравновесной смеси  с использованием формулы
с использованием формулы  .
.
Общее число молей неравновесной смеси
 .
.
Мольные доли компонентов в данном случае:
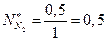 ;
;  ;
; 
численно равны числу молей этих компонентов в системе.
 .
.
Так как 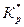 <
< 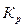 , то выполняется условие (2), следовательно, реакция будет протекать самопроизвольно в прямом направлении. Подтвердим полученные данные расчетом
, то выполняется условие (2), следовательно, реакция будет протекать самопроизвольно в прямом направлении. Подтвердим полученные данные расчетом  :
:
 Дж/моль.
Дж/моль.
Дата публикования: 2014-11-18; Прочитано: 317 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
