 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задача №12. В изолированной системе при Т = 298 К 1 моль идеального газа обратимо изотермически сжимается от давления p1=1,0133·105 Па до p2 (табл
|
|
В изолированной системе при Т = 298 К 1 моль идеального газа обратимо изотермически сжимается от давления p1= 1,0133·105 Па до p2 (табл. 13). Вычислить значения работы расширения А, теплоты Q, изменения внутренней энергии DU, энтальпии DH, энтропии DS, энергии Гиббса DG и энергии Гельмгольца DF системы. Определить направление самопроизвольного процесса.
Таблица 13
| Вариант | p2∙ 10–5, Па | Вариант | p2∙ 10–5, Па | Вариант | p2∙ 10–5, Па |
| 1,019 | 1,925 | 4,035 | |||
| 1,722 | 2,064 | 6,900 | |||
| 1,317 | 8,100 | 4,125 | |||
| 3,039 | 5,066 | 1,310 | |||
| 1,823 | 1,330 | 1,423 | |||
| 1,519 | 1,365 | 1,805 | |||
| 1,215 | 1,578 | 2,148 | |||
| 4,053 | 3,520 | 1,516 | |||
| 2,533 | 2,345 | 2,045 | |||
| 5,066 | 3,543 | 1,790 |
Решение:
Определим изменение характеристических термодинамических функций при обратимом изотермическом сжатии 1 моль идеального газа от p1= 1,0133·105 Па до p2= 1,0133·106 Па.
При изотермическом сжатии идеального газа изменение внутренней энергии ∆U = 0 и изменение энтальпии ∆H = 0. Поэтому из формулы (5)
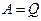 .
.
Работа изотермического сжатия от p1 до p2 определяется по формуле:
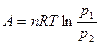 . (43)
. (43)
A = Q = 1∙8,314∙298∙ln(1,0133·105/1,0133·106 ) = – 5698,42 Дж.
Изменение энтропии в изотермическом процессе определяется по формуле
 . (44)
. (44)
 1∙8,314 ∙ln(1,0133·105 /1,0133·106 ) = – 19,12 Дж/К.
1∙8,314 ∙ln(1,0133·105 /1,0133·106 ) = – 19,12 Дж/К.
Изменение состояния системы выражается через изменение энергии Гельмгольца ∆F и изменение энергии Гиббса ∆G:
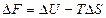 (V = const, T = const); (45);
(V = const, T = const); (45);
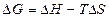 (p = const, T = const); (46).
(p = const, T = const); (46).
∆F = 0 – 298 ∙(–19,12) = 5697,76 Дж.
∆G = 0 – 298 ∙(–19,12) = 5697,76 Дж.
Так как процесс протекает в изолированной системе, критерием направленности самопроизвольного процесса является изменение энтропии. Если ∆S > 0, процесс самопроизвольно идет в прямом направлении. По расчету ∆S < 0, следовательно, процесс идет самопроизвольно в обратном направлении.
Дата публикования: 2014-11-18; Прочитано: 1007 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
