 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Статистичні розподіли для газів
|
|
· Розподіл молекул за швидкостями
· Розподіл Перена
Розподіл молекул за швидкостями. Рух молекул газу описується законами статистичної фізики. В середньому швидкості і енергії всіх молекул однакові. Проте в кожен момент часу енергії і швидкості окремих молекул можуть значно відрізнятись від середнього значення.
| Дж. Максвелл (1831 – 1879) |
На основі молекулярно-кінетичної теорії у 1859 р. англійський фізик Дж. Максвелл уперше встановив закон розподілу молекул ідеального газу за швидкостями. Це був перший приклад статистичного закону в науці. Дж. Максвелл усвідомив, що випадковий рух окремих молекул підпорядкований певному статистичному закону. Через складність математичного виразу цього закону розглянемо лише його графічне зображення (мал. 25).
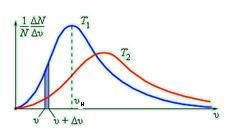
Мал. 25. Графічне зображення розподілу молекул за швидкостями
По осі абсцис відкладена швидкість молекул υ, а по осі ординат - функція f ( υ ) = Δ N / N Δ υ (де N – загальне кількість молекул, Δ N – кількість молекул, що мають швидкості в інтервалі від υ до υ + Δ υ). Максимум на кривій розподілу відповідає найбільш ймовірній швидкості υн. Найбільш ймовірна швидкість – швидкість, якою володіє максимальна кількість молекул газу.
Розподіл молекул за швидкостями залежить від температури. З підвищенням температури максимум функції розподілу зміщується в бік більшої швидкості.
Розподіл молекул за швидкостями (розподіл Максвелла) тривалий час залишався експериментально непідтвердженим.
Дайте відповіді на запитання
1. Які висновки можна зробити із розподілу Максвела?
Дата публикования: 2014-10-25; Прочитано: 1391 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
