 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Свободная поверхностная энергия
|
|
Все виды поверхностных явлений обусловлены тем, что частицы, находящиеся на поверхности раздела, по-разному взаимодействуют с частицами соприкасающихся фаз, причем эти
 |
Рис. 26.1. Схема действия межмолекулярных сил внутри жидкости и на ее поверхности
взаимодействия отличаются по энергии от взаимодействий частиц, содержащихся внутри каждой фазы. Например, молекулы, находящиеся на поверхности жидкости, испытывают неодинаковое воздействие со стороны молекул жидкости и пара. Силы межмолекулярного взаимодействия молекул, расположенных на поверхности, не скомпенсированы, их равнодействующая не равна нулю и направлена в сторону жидкости (рис. 26.1).
Следовательно, потенциальная энергия молекул на поверхности раздела фаз выше, чем у молекул внутри фазы. Эти отличия в энергетическом состоянии всех молекул поверхностного слоя характеризуются свободной поверхностной энергией Gs.
Свободной поверхностной энергией называется термодинамическая функция, характеризующая энергию межмолекулярного взаимодействия частиц на поверхности раздела фаз с частицами каждой из контактирующих фаз.
Свободная поверхностная энергия зависит от количества частиц на поверхности раздела, а потому прямо пропорциональна площади раздела фаз и удельной энергии межфазного взаимодействия:

где 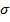 - удельная свободная поверхностная энергия, которая характеризует энергию межфазного взаимодействия единицы площади поверхности раздела фаз, кДж/м2; S - площадь поверхности раздела фаз, м2.
- удельная свободная поверхностная энергия, которая характеризует энергию межфазного взаимодействия единицы площади поверхности раздела фаз, кДж/м2; S - площадь поверхности раздела фаз, м2.
Удельная свободная поверхностная энергия 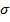 равна работе образования единицы поверхности раздела и зависит от природы контактирующих фаз и температуры. В зависимости от агрегатного состояния контактирующих фаз различают поверхностные явления на подвижной и неподвижной поверхности раздела. В системах газ - жидкость или жидкость - жидкость поверхность раздела подвижна, так как частицы поверхности раздела постоянно обновляются вследствие теплового движения молекул каждой фазы.
равна работе образования единицы поверхности раздела и зависит от природы контактирующих фаз и температуры. В зависимости от агрегатного состояния контактирующих фаз различают поверхностные явления на подвижной и неподвижной поверхности раздела. В системах газ - жидкость или жидкость - жидкость поверхность раздела подвижна, так как частицы поверхности раздела постоянно обновляются вследствие теплового движения молекул каждой фазы.
Удельную свободную поверхностную энергию для подвижных поверхностей раздела фаз называют коэффициентом поверхностного натяжения и обозначают 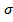 г/ж или
г/ж или 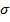 ж/ж. Его величину можно определить экспериментально при помощи сталагмометра и другими методами. Для полярных жидкостей вследствие более сильного межмолекулярного взаимодействия коэффициент поверхностного натяжения больше, чем для неполярных жидкостей. Так,
ж/ж. Его величину можно определить экспериментально при помощи сталагмометра и другими методами. Для полярных жидкостей вследствие более сильного межмолекулярного взаимодействия коэффициент поверхностного натяжения больше, чем для неполярных жидкостей. Так, 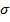 воздух/вода = 0,73 кДж/м2, а
воздух/вода = 0,73 кДж/м2, а 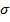 воздух/гексан = 0,18 кДж/м2. С повышением температуры а снижается, так как уменьшается различие в энергии межмолекулярного взаимодействия контактирующих фаз. При критической температуре и выше, когда исчезает различие между газом, паром и жидкостью, а энергия межмолекулярного взаимодействия в системе выравнивается,
воздух/гексан = 0,18 кДж/м2. С повышением температуры а снижается, так как уменьшается различие в энергии межмолекулярного взаимодействия контактирующих фаз. При критической температуре и выше, когда исчезает различие между газом, паром и жидкостью, а энергия межмолекулярного взаимодействия в системе выравнивается, 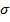 = 0.
= 0.
В системах газ - твердое тело или жидкость - твердое тело поверхность раздела неподвижна. Удельную свободную поверхностную энергию систем с неподвижной поверхностью раздела (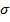 г/тв>
г/тв> 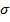 ж/тв) экспериментально определить трудно, но ее значение можно оценить по способности твердой поверхности к смачиванию.
ж/тв) экспериментально определить трудно, но ее значение можно оценить по способности твердой поверхности к смачиванию.
 |
Свободная поверхностная энергия Gs при постоянном давлении совпадает с термодинамической функцией - энергией Гиббса, характеризующей состояние поверхности раздела фаз в гетерогенных системах. В соответствии со II законом термодинамики (разд. 4.4) все самопроизвольные процессы происходят в направлении, приводящем к уменьшению энергии Гиббса, поэтому и все поверхностные явления протекают самопроизвольно только в тех случаях, когда свободная поверхностная энергия системы уменьшается:
Поскольку свободная поверхностная энергия Gs зависит от двух параметров - 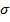 и S, то все поверхностные явления совершаются самопроизвольно, если при этом или снижается удельная свободная поверхностная энергия (
и S, то все поверхностные явления совершаются самопроизвольно, если при этом или снижается удельная свободная поверхностная энергия ( < 0), или уменьшается площадь поверхности раздела фаз (AS < 0), или происходит такое изменение этих величин, чтобы
< 0), или уменьшается площадь поверхности раздела фаз (AS < 0), или происходит такое изменение этих величин, чтобы  GS =
GS =  S < 0.
S < 0.
К самопроизвольным поверхностным явлениям, которые сопровождаются уменьшением Gs за счет уменьшения площади поверхности, относятся: коалесценция - слияние капель жидкости или пузырьков газа — и коагуляция - слипание частиц в дисперсных системах.
К самопроизвольным поверхностным явлениям, сопровождающимся уменьшением Gs за счет снижения удельной свободной поверхностной энергии о, относятся сорбция и ее последствия: смачивание, эмульгирование и др.
Дата публикования: 2014-10-16; Прочитано: 9330 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
