 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Степень окисления углерода в органических соединениях
|
|
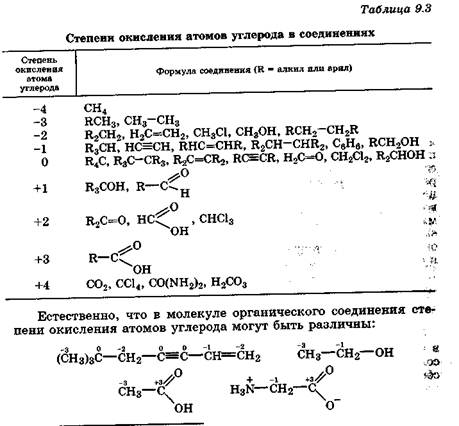 |
В природных органических соединениях степень окисления атомов элементов-органогенов обычно равна: водорода +1, азота -3, кислорода* -2, серы* -2, фосфора +5, а углерода - любой величине от -4 до +4. В органическом соединении степень окисления данного атома углерода является условным зарядом, который рассчитывается с учетом того, что общая пара электронов химической связи между атомами относится полностью к более электроотрицательному атому. Общие пары электронов, принадлежащих соседним атомам одного и того же элемента, включая углерод, не следует учитывать при определении степени окисления. В табл. 9.3 указаны степени окисления атомов углерода в различных соединениях.
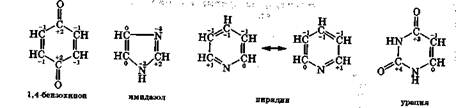 |
Различий в значениях степеней окисления у ос-атомов углерода в молекуле пиридина из-за делокализации кратных связей в действительности, конечно, нет. Однако в производных пиридина указанные различия иногда необходимо учитывать, например в НАД+, НАДФ+.
На основании приведенных примеров можно сформулировать следующее правило:
Степень окисления любого атома углерода в природных органических соединениях равна алгебраической сумме числа всех его связей с атомами более электроотрицательных элементов (кислород, азот, сера), учитываемых со знаком "+", и числа связей с атомами водорода, учитываемых со знаком "-", а все его связи с соседними атомами углерода не учитываются.
Вычисленная степень окисления атомов углерода, хотя и является условной величиной, указывает на смещение электронной плотности в молекуле, а ее изменение в результате реакции четко свидетельствует об окислительно-восстановительном характере этой реакции. Наличие у атомов углерода широкого диапазона степеней окисления от -4 до +4 свидетельствует о его окислительно-восстановительной двойственности. Поэтому в органической химии широко распространены реакции окислительно-восстановительной дисмутации за счет атомов углерода. Причем эти окислительно-восстановительные реакции могут протекать внутри и межмолекулярно.
Дата публикования: 2014-10-16; Прочитано: 15672 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
