 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Окислительно-восстановительные превращения кофакторов и коферментов оксидоредуктаз
|
|
Кофакторы и коферменты, реагируя под влиянием оксидоредуктаз с субстратом, в зависимости от его природы могут быть окислителями или восстановителями. Такая двойственность связана с возможностью их существования в двух сопряженных формах: окисленной и восстановленной.
Оксидоредуктазами, содержащими кофакторы, являются различные цитохромы, железосеропротеины [FexSxProt] и ряд других ферментов. Эти соединения являются комплексами, в которых белок фермента ковалентно связан с комплексообразователем - катионом переходного металла, выполняющего роль кофактора. Кофактором чаще всего бывает железо, медь, а иногда марганец и молибден. Все они образуют с белком не менее двух ковалентных связей. Поскольку для всех перечисленных металлов характерна переменная валентность, то их окислительно-восстановительные превращения связаны с присоединением или отдачей электронов. Вследствие этого обратимо изменяется заряд катиона металла-комплексообразователя. В результате происходит переход оксидоредуктазы из окисленной формы в восстановленную и наоборот:

Вследствие окислительно-восстановительной двойственности оксидоредуктазы с кофакторами способны служить переносчиками электронов и поэтому являются компонентами электронотранспортных цепей (разд. 9.3.5).
В качестве коферментов оксидоредуктаз выступают сложные органические соединения, способные к обратимым окислительно-восстановительным превращениям за счет дисмутации их атомов углерода. Окисленная форма кофермента Коф, выступая акцептором и электронов и протонов, переходит в сопряженную восстановленную форму Коф(хН)

Коферменты связаны с белком оксидоредуктазы достаточно прочно: обычно за счет межмолекулярных связей, но иногда и ковалентно. Рассмотрим особенности строения и окислительно-восстановительных свойств некоторых коферментов.
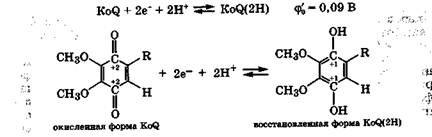
Убихиноны, или кофермент Q (KoQ). Убихиноны - это группа жирорастворимых витаминов Q, являющихся производными бензохинона, содержащими гидрофобный заместитель R, который способствует их соединению с белком с образованием убихинон-протеинов. Убихинонпротеины, являясь окислителями, присоединяют от субстрата два электрона к атомам углерода хиноидной группировки, изменяя их степень окисления. Одновременно к атомам кислорода этого кофермента присоединяются два протона (обычно из водной среды). В результате образуется восстановленная форма - убихинолпротеины KoQ(2H):
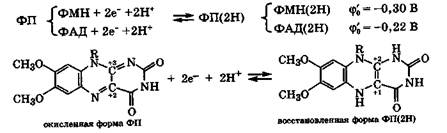 |
Флавопротеины (ФП) - соединения, содержащие изоалло-ксазиновый фрагмент. К ним прежде всего относятся соединения флавинаденинмононуклеотида (ФМН) или флавинаденин-динуклеотида (ФАД) с белком, которые являются производными рибофлавина (витамин В2). Эти коферменты, восстанавливаясь, присоединяют от субстрата два электрона к атомам углерода изоаллоксазинового фрагмента, изменяя их степень окисления. Одновременно два протона (Н+), получаемые обычно из водной среды, присоединяются к атомам азота, в результате образуется восстановленная форма ФП(2Н) - ФМН(2Н) или ФАД(2Н).
Пиридинпротеины - соединения, содержащие никотинамид-адениндинуклеотид (НАД+) или никотинамидадениндинуклео-тидфосфат (НАДФ+), в обозначении окисленных форм которых содержится знак "+", так как они содержат пиридиниевый катион. Оба эти соединения, восстанавливаясь, присоединяют от субстрата-восстановителя два электрона и один протон к атомам углерода пиридинового цикла, переходя в восстановленную форму НАД(Н) или НАДФ(Н) соответственно. Эти коферменты являются производными витамина PP.
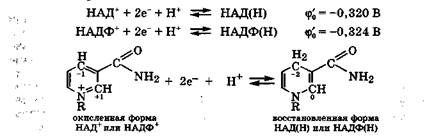
Таким образом, окислительно-восстановительные превращения коферментов оксидоредуктаз протекают за счет атомов углерода и в них принимают участие протоны. Причем окисленная форма любого кофермента выступает акцептором и электронов и протонов, а восстановленная форма - их донором. Подобно оксидоредуктазам с кофакторами, оксидоредуктазы с коферментами могут быть переносчиками электронов, поэтому они также являются компонентами электронотранспортных цепей клетки (разд. 9.3.4).
Окислительно-восстановительные свойства коферментов в организме сильно зависят от того, концентрация какой из форм преобладает. Если преобладает окисленная форма, то кофермент выступает окислителем и способствует окислению субстрата. В случае преобладания восстановленной формы кофермент-вос-становитель способствует восстановлению субстрата. Так, в клетках печени отношение концентраций [НАД+]/[НАД(Н)] > 510, а [НАДФ+]/ [НАДФ(Н)] = 0,01. Поэтому сопряженная система кофермента НАД+ выступает окислителем, способствуя окислению субстратов, а сопряженная система кофермента НАДФ+, в которой преобладает форма НАДФ(Н), ведет себя как восстановитель, способствуя восстановлению субстратов. Таким образом, за счет изменения соотношения концентраций окисленной и восстановленной форм коферментов оксидоредуктаз происходит поддержание окислительно-восстановительного гомеостаза и регуляция метаболизма в организме.
Многие окислительно-восстановительные реакции в организме протекают под действием других коферментов, например глютатиона, липоевой кислоты, пиридоксальфосфата, действие которых рассматривается в разд. 12.2.6, 17.6 и 18.2.4 соответственно.
В биохимической и медицинской литературе часто встречается мнение, что коферменты убихиноны и флавопротеины при восстановлении присоединяют два атома водорода или молекулу водорода, а пиридинпротеины - гидрид-ион, т. е. Н", и что коферменты являются переносчиками указанных частиц. Иногда совокупность электрона и протона {е- + Н+} = = {Н} называют восстановительным эквивалентом. Все эти выражения крайне неудачны, так как противоречат химической сущности протекающих процессов и химически абсурдны, атомарный водород чрезвычайно реакционноспособен, а молекулы водорода, наоборот, химически инертны и чрезвычайно летучи в условиях организма. Гидрид-ион не может образовываться и существовать в воде, которой в организме свыше 60 %. Следует говорить о присоединении или переносе оксидоредуктазами электронов и протонов раздельно, и нельзя объединять эти частицы, так как маршруты их движения в живых системах абсолютно различны. Особенно четко это проявляется в электронотранспортных цепях клетки.
Дата публикования: 2014-10-16; Прочитано: 5376 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
