 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задача №9. Определите абсолютную энтропию ST 1 моль вещества, указанного в таблице 10, при температуре Т К (табл
|
|
Определите абсолютную энтропию ST 1 моль вещества, указанного в таблице 10, при температуре Т К (табл. 6), если известны значения температур плавления и кипения этого вещества. Теплоемкости веществ в различных агрегатных состояниях возьмите из справочника.
Теплоту испарения возьмите из расчетов задачи №5.
Таблица 10
| Вариант | Вещество | ТПЛ, К | ТКИП, К |
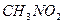 нитрометан нитрометан
| |||
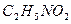 нитроэтан нитроэтан
| |||
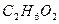 этиленгликоль этиленгликоль
| |||
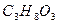 глицерин глицерин
| |||
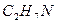 диметиламин диметиламин
| |||
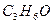 ацетон ацетон
| |||
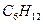 циклогексан циклогексан
| |||
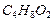 этилацетат этилацетат
| |||
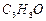 пропанол-1 пропанол-1
| |||
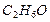 этанол этанол
| |||
 амиловый спирт амиловый спирт
| |||
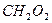 муравьиная кислота муравьиная кислота
| |||
 хлороформ хлороформ
| |||
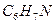 анилин анилин
| |||
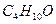 диэтиловый эфир диэтиловый эфир
| |||
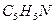 пиридин пиридин
|
Продолжение таблицы 10
| Вариант | Вещество | ТПЛ, К | ТКИП, К |
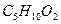 валериановая кислота валериановая кислота
| |||
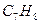 толуол толуол
| |||
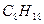 октан октан
| |||
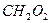 муравьиная кислота муравьиная кислота
| |||
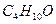 бутанол бутанол
| |||
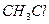 хлорметан хлорметан
| |||
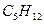 пентан пентан
| |||
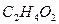 уксусная кислота уксусная кислота
| |||
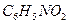 нитробензол нитробензол
| |||
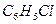 хлорбензол хлорбензол
| |||
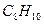 м-ксилол м-ксилол
| |||
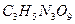 нитроглицерин нитроглицерин
| |||
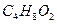 1,4-диоксан 1,4-диоксан
| |||
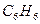 бензол бензол
|
Решение:
Определим абсолютную энтропию 1 моль воды при температуре минус 700 С.
Абсолютное значение энтропиипозволяет определить третье начало термодинамики или теорема Нернста: при абсолютном нуле энтропия правильного кристалла любого чистого вещества равна нулю (эту формулировку теоремы Нернста предложил М.Планк).
S0 = 0 при Т = 0.
Абсолютную энтропию вещества при температуре Т рассчитывают, используя постулат Планка, а также значения теплоемкостей, температур фазовых переходов и теплот фазовых переходов в интервале от 0 К до Т. На практике для расчета абсолютной энтропии при температуре Т используют справочные данные об абсолютных энтропиях веществ при 298 К. При расчете вносится поправка, учитывающая изменение энтропии вещества в интервале от 298 К до Т.
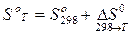 .
.
По условию задачи необходимо определить энтропию при температуре минус 700 С, т.е. при 203 К, следовательно, к значению 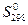 необходимо прибавить изменение энтропии в интервале температур от 298 до 203 К.
необходимо прибавить изменение энтропии в интервале температур от 298 до 203 К.
В заданном интервале температур вода претерпевает фазовое превращение – плавление при 273 К. Расчет энтропии проводится по аддитивной схеме:
 . (31)
. (31)
В справочнике найдем абсолютную энтропию воды при 298 К.
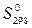 = 69,95 Дж/(моль∙К).
= 69,95 Дж/(моль∙К).
Изменение энтропии при нагревании и плавлении определим по формулам:
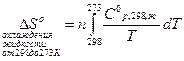 , (32)
, (32)
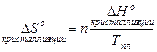 , (33)
, (33)
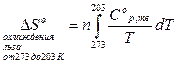 , (34)
, (34)
где n – число молей вещества; по условию задачи n = 1.
Теплоту кристаллизации воды найдем по справочнику:
DHоплавления = 6000 Дж/моль. DHокрист. = - DHоплавления = -6000 Дж/моль.
Примечание: теплоту плавления для органических веществ рассчитайте по формуле 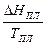 = 54,4 ± 12,6 Дж/(моль·К).
= 54,4 ± 12,6 Дж/(моль·К).
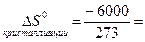 -21,98 Дж/К.
-21,98 Дж/К.
Изменение температуры жидкости равно 25 градусов. Температурный интервал невелик, и можно пренебречь зависимостью теплоемкости жидкой воды от температуры. Для расчетов воспользуемся средним значением теплоемкости; по справочнику
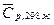 = 75,3 Дж/(моль∙К).
= 75,3 Дж/(моль∙К).
Расчет в этом случае проведем по формуле:
 = -6,59 Дж/К.
= -6,59 Дж/К.
Для льда разность температур составляет 70 градусов. Учтем зависимость теплоемкости от температуры (коэффициенты уравнения возьмем из справочника):
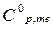 = 4,41 + 109,5·10–3 Т + 46,47·10–6 Т2 Дж/(моль∙К).
= 4,41 + 109,5·10–3 Т + 46,47·10–6 Т2 Дж/(моль∙К).
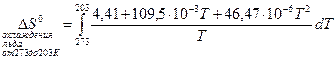 =
=
= 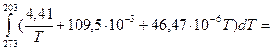
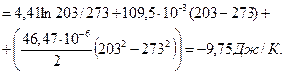
Рассчитаем абсолютную энтропию воды при –700 С (31):
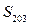 = 69,95 – 21,98 – 6,59 – 9,75 = 31,63 Дж/К.
= 69,95 – 21,98 – 6,59 – 9,75 = 31,63 Дж/К.
Дата публикования: 2014-11-18; Прочитано: 2436 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
