 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задача №10. Вычислите изменение энтропии в реакции, приведенной в табл
|
|
Вычислите изменение энтропии в реакции, приведенной в табл. 2, при температуре T = 298 К и Т К (табл. 6).
Решение:
Определим изменение энтропии реакции  при температурах 298 К и 800 К.
при температурах 298 К и 800 К.
Выписываем из справочника абсолютные энтропии участников реакции:
Таблица 11
| Вещество | S0298 , Дж/(моль·К) |
| N2 | 191,50 |
| H2 | 130,52 |
| NH3 | 192,66 |
 прод прод
| 385,32 |
 исх исх
| 583,06 |
 , реакции , реакции
| – 197,74 |
Изменение энтропии  в ходе реакции при температуре 298 К равно разности абсолютных энтропий продуктов и исходных веществ, взятых с учетом стехиометрических коэффициентов:
в ходе реакции при температуре 298 К равно разности абсолютных энтропий продуктов и исходных веществ, взятых с учетом стехиометрических коэффициентов:
 . (35)
. (35)
 = 2·192,66 –191,50 –3·130,52 =385,32 –583,06= –197,74 Дж/К.
= 2·192,66 –191,50 –3·130,52 =385,32 –583,06= –197,74 Дж/К.
Изменение энтропии реакции при температуре Т рассчитывается по общей формуле:
 . (36)
. (36)
Для приближенного расчета можно пренебречь зависимостью теплоемкостей от температуры и воспользоваться значениями средних теплоемкостей участников реакции. В этом случае расчет ведется по формуле
 . (37)
. (37)
Для точного расчета необходимы данные по зависимости теплоемкостей от температуры. В этом случае изменение энтропии реакции рассчитывается по формуле:
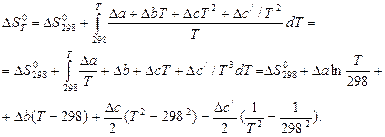 (38)
(38)
Воспользуемся справочными данными и результатами расчетов из задачи №8.
Приближенно:
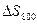 , реакции= – 197,74 + (– 31,88) ln (800/298) = – 229,22 Дж/K.
, реакции= – 197,74 + (– 31,88) ln (800/298) = – 229,22 Дж/K.
Точно:
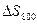 , реакции= – 197,74 + (–50,12) ln(800/298) + 36,91·10–3(800 – 298) +
, реакции= – 197,74 + (–50,12) ln(800/298) + 36,91·10–3(800 – 298) +
+ 1/2(–1,50·10–6)(8002 – 2982) – 1/2(–3,34·105)(1/8002 – 1/2982) =
= – 230,36 Дж/K.
Дата публикования: 2014-11-18; Прочитано: 2018 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
