 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
ПРИЛОЖЕНИЕ. Термодинамические свойства некоторых элементов и неорганических
|
|
Таблица 1
Термодинамические свойства некоторых элементов и неорганических
соединений при стандартных условиях
| Вещество | Состояние | ∆Н0298, кДж/моль | ∆G0298, кДж/моль | ∆S0298, кДж/моль К | Cp0298, кДж/моль К |
| AgCl | тв. | -127,04 | -109,72 | 96,11 | 50,79 |
| AgJ | тв. | -62,38 | -66,32 | 114,22 | 54,43 |
| AgBr | тв. | -99,50 | -95,94 | 107,11 | 52,38 |
| H3BO3 | тв. | -1087,84 | -963,16 | 89,58 | 82,05 |
| BaSO4 | тв. | -1464,40 | -1353,11 | 132,21 | 101,75 |
| HBr | газ | -36,23 | -53,22 | 198,48 | 26,12 |
| C (графит) | тв. | 5,69 | 8,64 | ||
| C (алмаз) | тв. | 1,90 | 2,87 | 2,44 | 6,06 |
| CO | газ | -110,52 | -137,27 | 197,91 | 29,14 |
| CO2 | газ | -393,51 | -394,38 | 213,64 | 37,13 |
| COCl2 | газ | -223,00 | -210,50 | 289,20 | 60,67 |
| CS2 | газ | 115,27 | 65,06 | 237,82 | 45,65 |
| CO(NH2)2 | тв. | -333,19 | -197,15 | 104,60 | 93,14 |
| CaO | тв. | -635,55 | -604,17 | 39,75 | 42,80 |
| Ca(OH)2 | тв. | -986,59 | -896,76 | 76,15 | 84,52 |
| CaCO3 | тв. | -1206,88 | -1128,76 | 92,89 | 81,88 |
| CaC2 | тв. | -62,70 | -67,80 | 70,30 | 62,34 |
| CH4 | газ | -333,17 | -191,15 | 189,19 | 93,14 |
| H2 | газ | 130,59 | 28,84 | ||
| H2O | газ | 241,83 | -228,60 | 188,72 | 83,58 |
| H2O | жидк. | -285,84 | -237,19 | 69,54 | 75,30 |
| H2S | газ | -20,15 | - | 205,60 | - |
| HgCl2 | тв. | -213,00 | -169,60 | 136,00 | 73,00 |
| HgO | тв. | -90,70 | -58,53 | 71,97 | 46,73 |
| HgS | тв. | -58,16 | -48,83 | 77,82 | 12,00 |
| HJ | газ | 25,94 | 1,30 | 206,33 | 29,18 |
| MgO | тв. | -601,,83 | -569,57 | 26,78 | 37,41 |
| Mg(OH)2 | тв. | -924,66 | -833,75 | 63,14 | 77,03 |
| N2 | газ | 191,79 | 29,12 | ||
| NH3 | газ | -48,19 | -16,64 | 192,51 | 35,68 |
| NH4Cl | тв. | -315,39 | -203,89 | 94,56 | 84,10 |
| NO | газ | 90,37 | 86,69 | 210,62 | 29,86 |
| N2O4 | газ | 81,56 | 103,60 | 219,99 | 38,70 |
| HNO3 | тв. | -173,22 | -79,9 | 155,60 | 109,87 |
| O2 | газ | 205,03 | 29,36 | ||
| P | тв. белый | 47,60 | 23,82 | ||
| P | тв. красный | -18,40 | 13,82 | 29,31 | 20,83 |
| P2O5 | тв. | -3012,48 | - | 280,00 | 207,80 |
| PH3 | газ | 9,25 | 18,24 | 210,04 | - |
| HPO3 | жидк. | -982,40 | -902,91 | 150,60 | - |
| PCl3 | газ | -277,00 | -28,27 | 3117,00 | 71,4 |
| H3PO4 | жидк. | -1271,94 | -1147,25 | 200,83 | - |
| PCl5 | газ | -369,45 | -324,55 | 362,90 | 109,2 |
| PbO | тв. | -217,86 | -188,49 | 69,45 | 48,53 |
| PbO2 | тв. | -276,56 | -218,99 | 76,57 | 64,43 |
| PbCl2 | тв. | -369,20 | -313,97 | 136,40 | 76,99 |
| PbS | тв. | -94,31 | -92,68 | 91,21 | 49,50 |
| S ромб. | тв. | 31,88 | 22,59 | ||
| S монок. | тв. | 0,30 | 6,10 | 32,55 | 23,64 |
| SO2 | газ | -296,06 | -370,37 | 248,52 | 39,79 |
| SO3 | газ | -395,18 | -37,37 | 256,22 | 50,63 |
| SO2Cl2 | жидк. | -389,10 | -300,55 | 217,20 | 131,8 |
| Zn | тв. | 41,63 | 25,06 | ||
| ZnO | тв. | 347,98 | -318,19 | 43,93 | 40,25 |
| ZnS | тв. | -202,92 | -198,32 | 57,74 | 45,19 |
Таблица 2
Термодинамические свойства некоторых органических молекул и
биомолекул при стандартных условиях
| Соединение | Формула | Состояние | ∆Н0298, кДж/моль | ∆G0298, кДж/моль | ∆S0298, кДж/моль К | Cp0298, кДж/моль К |
| Уксусная кислота | СН3СООН | жидк. | -484,21 | -389,45 | 159,83 | - |
| Ацетат анион | СН3СОО- | водн. | -485,26 | -404,09 | 205,43 | - |
| Уксусный альдегид | СН3СНО | водн. | -485,60 | -376,89 | 112,97 | - |
| Уксусный альдегид | СН3СНО | газ | -246,81 | -139,08 | 264,22 | 56,07 |
| Ацетон | СН3СОСН3 | жидк. | -246,81 | -153,55 | 198,74 | 126,78 |
| Ацетилен | С2Н2 | газ | 226,73 | 209,20 | 200,83 | 43,93 |
| Аденин | С5Н5N5 | тв. | 97,07 | -300,41 | 151,04 | 143,09 |
| D,L-аланин | С3Н7О2N | тв. | -563,59 | -371,96 | 132,21 | 121,75 |
| L-аланин | С3Н7О2N | тв. | -562,75 | -370,20 | 129,20 | 122,26 |
| D,L-аспараги-новая кислота | C4H7O4N | тв. | -976,96 | -729,27 | 154,39 | - |
| L-аспараги-новая кислота | C4H7O4N | тв. | -972,53 | -729,36 | 170,12 | 155,27 |
| L-аспарагин | C4H8O3N2 | тв. | -790,36 | -530,95 | 174,47 | 160,67 |
| Бензол | C6H6 | жидк. | 49,04 | 172,80 | 124,52 | |
| Масляная кислота | C4H3O2 | жидк. | -535,13 | -379,07 | 226,35 | 179,49 |
| Креатинин | C4H7ON3 | тв. | -237,65 | -28,45 | 167,36 | 138,91 |
| Лимонная кислота | C6H8O7 | тв. | -1543,90 | -1288,63 | 512,54 | - |
| L-цистеин | C3H7O2N | тв. | -532,62 | -342,67 | 169,87 | 173,22 |
| L-цистин | C6H12O4 | тв. | -1044,33 | -685,76 | 280,58 | 262,92 |
| Этанол | C2H5OH | жидк. | -276,98 | -174,18 | 161,04 | 111,96 |
| Этилацетат | C4H8O2 | жидк. | -481,99 | -377,65 | 262,76 | 105,44 |
| Этан | C2H6 | газ | -84,68 | -32,89 | 229,49 | 52,66 |
| Этилен | C2H4 | газ | 52,30 | 68,12 | 219,45 | 43,56 |
| Муравьиная кислота | HCOOH | жидк. | -409,20 | -346,02 | 128,95 | 99,04 |
| Фумаровая кислота | C4H4O4 | тв. | -810,65 | -653,25 | 166,11 | 142,26 |
| Α-D-глюкоза | C6H12O6 | тв. | -1274,45 | -910,65 | 212,13 | 218,87 |
| Β-D-глюкоза | C6H12O6 | тв. | -1268,05 | -908,89 | 228,03 | - |
| α-β-D-глюкоза | C6H12O6 | водн. | -1263,78 | -918,97 | 269,45 | 305,43 |
| Α-D-глюкоза моногидрат | C6H14O7 | тв. | -1571,09 | -1140,55 | 252,30 | - |
| Глюкоза-1-фосфорная кислота | С6H13O9P | водн. | - | -1789,50 | - | - |
| Глюкоза-1-гидрофосфат анион | C3H12O9P- | водн. | - | -1783,22 | - | - |
| Глюкоза-1-фосфат анион | C3H11O9P2- | водн. | - | -1746,11 | - | - |
| Глюкоза-6-фосфорная кислота | C6H13O9P | водн. | - | -1797,45 | - | - |
| Глюкоза-6-гидрофосфат анион | C3H12O9P- | водн. | - | -1789,08 | - | - |
| Глюкоза-6-фосфат анион | C3H11O9P2- | водн. | - | -1753,51 | - | - |
| Глицерин | C3H8O3 | жидк. | -670,70 | -479,49 | 204,60 | 216,73 |
| L-глутами-новая кислота | C5H9O4N | тв. | -1009,18 | -730,95 | 188,20 | 175,23 |
| L-глутамин | C3H10O3N2 | тв. | -925,92 | 532,21 | 195,10 | 183,80 |
| Глицин | C2H5O2N | тв. | -537,23 | -377,69 | 103,00 | - |
| Глицилглицин | C4H8O3N2 | тв. | -746,01 | -491,50 | 189,95 | 163,59 |
| Α-кетоглута-ровая кислота | C5H6O5 | тв. | -1026,34 | - | - | - |
| L-молочная кислота | C3H8O3 | тв. | -2694,04 | -523,25 | 143,51 | 126,61 |
| α-D-молочная кислота | C3H6O3 | жидк. | -673,62 | -518,82 | 192,05 | 211,29 |
| α-лактоза | C12H22O11 | тв. | -2221,20 | - | - | - |
| α-лактоза | C12H22O11 | водн. | -2232,37 | -1564,90 | 394,13 | - |
| β-лактоза | C12H22O11 | тв. | -2236,77 | -1666,91 | 386,15 | 410,45 |
| α-β-лактоза | C12H22O11 | водн. | -2233,09 | -1567,33 | 399,57 | - |
| D,L-лейцин | C6H13O2N | тв. | -649,78 | -358,57 | 207,11 | 195,39 |
| L-лейцин | C6H13O2N | тв. | -646,85 | -356,48 | 209,62 | 208,36 |
| L-яблочная кислота | C4H6O6 | тв. | -1103,52 | - | - | - |
| D,L-яблочная кислота | C4H6O6 | тв. | -1105,41 | - | - | - |
| α-мальтоза | С12Н22О11 | водн. | -2238,27 | -1573,60 | 403,34 | - |
| α-β-мальтоза | С12Н22O11 | водн. | -2238,06 | -1574,69 | 407,94 | - |
| β-мальтоза моногидрат | C12H22O12 | тв. | -253,27 | -1809,58 | 417,56 | 453,96 |
| Метан | CH4 | газ | -74,85 | -50,79 | 186,19 | 35,73 |
| Метанол | CH3OH | жидк. | -238,66 | -166,31 | 126,78 | 81,59 |
| α-метионин | C5H11O2N | тв. | -761,07 | -508,36 | 231,46 | 290,20 |
| Щавелево-уксусная кислота | C4H4O5 | тв. | -984,50 | - | - | - |
| Пальмитиновая кислота | C16H32O2 | тв. | -890,77 | -315,06 | 455,22 | 460,66 |
| Пировиноградная кислота | C3H4O3 | жидк. | -585,76 | - | - | - |
| Пировиноградная кислота | C3H4O3 | водн. | -607,52 | -486,60 | 179,91 | - |
| Пируват-анион | C3H3O3- | водн. | -596,22 | -432,37 | 171,54 | - |
| Пропанол-2 | C3H7OH | жидк. | -317,86 | -180,29 | 180,58 | 154,22 |
| Янтарная кислота | C4H6O2 | тв. | -940,81 | -747,35 | 175,73 | 153,97 |
| Сахароза | C12H22O11 | тв. | -2215,85 | -1551,43 | 403,76 | 633,04 |
| D,L-валин | C5H11O2N | тв. | -607,98 | -359,82 | 181,17 | - |
| α-валин | C5H11O2N | тв. | -617,98 | -359,99 | 178,74 | 168,82 |
| Пропилен | C3H6 | газ | 20,41 | 63,00 | 206,90 | - |
| Пропан | C3H8 | газ | -103,90 | -23,56 | 269,90 | - |
| Ацетилен | C2H2 | газ | 226,75 | 209,20 | 200,80 | - |
| Циклогексан | C6H12 | газ | -123,10 | 31,92 | 298,20 | - |
| Хлористый метил | CH3Cl | газ | -82,00 | 58,80 | 233,50 | - |
| Хлороформ | CHCl3 | газ | -131,80 | -71,80 | 202,90 | - |
| Четырех-хлористый углерод | СCl4 | газ | -106,70 | 68,88 | 309,70 | - |
| Анилин | C6H5NH2 | жидк. | 82,40 | 153,72 | 310,00 | - |
| Мочевина | CО(NH2)2 | тв. | -333,17 | -197,15 | 104,60 | 93,14 |
Таблица 3
Энтальпия сгорания органических соединений при стандартных условиях
| Соединения | ∆Н0298, кДж/моль | |
| Метан | СН4 (газ) | -890,31 |
| Ацетилен | С2Н2 (газ) | -1299,63 |
| Этилен | С2Н4 (газ) | -1410,97 |
| Этан | С2Н6 (жидк.) | -1559,88 |
| Бензол | С6Н6 (жидк.) | -3267,70 |
| Бутан | С4Н10 (газ) | -2678,76 |
| Метанол | СН3ОН (жидк.) | -726,64 |
| Этанол | С2Н5ОН (жидк.) | -1366,91 |
| Глицерин | С3Н8О3 | -1664,40 |
| Этиленгликоль | С6Н6О2 (жидк.) | -1192,86 |
| Диэтиловый эфир | С4Н10О (жидк.) | -2730,90 |
| Уксусная кислота | СН3СООН (жидк.) | -873,79 |
| Глюкоза | С6Н12О6 (к) | -2815,80 |
| Сахароза | С12Н22О11 (к) | -5648,00 |
| Бензойная кислота | С7Н6О2 | -3227,54 |
| Гептанол | С7Н16О (жидк.) | -4618,50 |
| Щавелевая кислота | С2Н2О4 (тв.) | -246,90 |
| Фенол | С6Н6О (тв.) | -3074,40 |
| Гидрохинон | С6Н4(ОН)2 (тв.) | -2857,86 |
| Амиловый спирт | С5Н12О (жидк.) | -3317,66 |
| Ацетон | С3Н6О (жидк.) | -1809,80 |
| Изопропиловый спирт | С3Н8О (жидк.) | -1984,66 |
| Муравьиная кислота | СН2О2 (жидк.) | -270,90 |
| Мочевина | СО(NН2)2 | -636,20 |
| Анилин | С6Н5NН2 | -3409,98 |
| Сероуглерод | СS2 | -1079,40 |
Таблица 4
Криоскопические (К) и эбуллиоскопические (Е) константы растворителей
| Растворитель | К градус | Е градус | t плавления | t кипения |
| Анилин | 5,87 | 3,22 | -5,96 | 184,40 |
| Ацетон | 2,40 | 1,48 | -94,60 | 56,00 |
| Бензол | 5,00 | 2,57 | 5,40 | 80,20 |
| Вода | 1,86 | 0,52 | 100,00 | |
| Камфора | 40,0 | 6,09 | 174,00 | 204,00 |
| Нитробензол | 6,90 | 5,27 | 5,70 | 210,90 |
| Фенол | 7,30 | 3,60 | 41,00 | 182,10 |
| Хлороформ | 4,90 | 3,88 | -63,20 | 61,20 |
| Четыреххлористый углерод | 2,98 | 5,30 | -23,00 | 76,70 |
Таблица 5
Средняя теплоемкость простых веществ и соединений от 298 К до Т1, К
| № | Вещество | 500 К | 600 К | 700 К | 800 К | 900 К | 1000 К | 1100 К |
| Средняя теплоемкость, Дж/моль К | ||||||||
| Cl2 (г) | 35,44 | 35,77 | 36,02 | 36,23 | 36,70 | 36,53 | 36,78 | |
| H2 (г) | 27,54 | 27,84 | 28,09 | 28,33 | 28,55 | 28,77 | 29,17 | |
| N2 (г) | 29,58 | 29,79 | 30,00 | 30,21 | 30,42 | 30,63 | 31,05 | |
| O2 (г) | 30,29 | 30,88 | 31,34 | 31,76 | 32,09 | 32,43 | 32,97 | |
| CO (г) | 29,74 | 30,00 | 30,23 | 30,47 | 30,69 | 30,92 | 31,55 | |
| CO2 (г) | 42,05 | 43,47 | 44,60 | 45,56 | 46,44 | 47,15 | 48,53 | |
| COCl2 (г) | 65,98 | 67,57 | 68,87 | 70,04 | 71,04 | 72,01 | - | |
| CaCO3 (тв) | 95,98 | 100,00 | 103,10 | 105,40 | 108,10 | 110,2 | 113,80 | |
| CaO (тв) | 46,78 | 47,78 | 48,53 | 49,20 | 49,75 | 50,21 | 51,09 | |
| HCl (г) | 29,12 | 29,20 | 29,33 | 29,50 | 29,71 | 29,87 | 30,29 | |
| H2O (г) | 34,48 | 37,98 | 35,52 | 36,02 | 36,57 | 37,07 | 38,12 | |
| MgO (тв) | 41,34 | 42,43 | 43,26 | 43,60 | 44,64 | 45,27 | - | |
| Mg(OH)2 (тв) | 80,17 | 84,31 | - | - | - | - | - | |
| NH3 (г) | 38,91 | 40,17 | 41,71 | 43,22 | 44,73 | 43,35 | 48,37 | |
| NO (г) | 30,54 | 30,79 | 31,04 | 31,30 | 31,51 | 31,71 | 32,13 | |
| NO2 (г) | 41,92 | 43,05 | 43,93 | 44,89 | 45,60 | 46,32 | 47,53 | |
| N2O (г) | 43,41 | 44,78 | 45,90 | 46,84 | 47,67 | 48,41 | 49,76 | |
| N2O3 (г) | 89,75 | 93,40 | 96,58 | 99,45 | 102,14 | 104,66 | - | |
| SO2 (г) | 43,78 | 45,03 | 46,11 | 47,07 | 47,96 | 48,80 | 50,37 | |
| SO3 (г) | 59,28 | 62,08 | 64,48 | 66,55 | 68,54 | 70,37 | 73,78 | |
| CH4 (г) | 41,27 | 44,10 | 46,87 | 49,56 | 52,16 | 54,66 | 59,31 | |
| C2H4 (г) | 53,85 | 58,36 | 62,48 | 66,28 | 69,77 | 72,98 | 78,63 | |
| C2H6 (г) | 65,79 | 71,78 | 77,36 | 82,57 | 87,46 | 92,00 | 100,00 | |
| C6H6 (ж) | 110,70 | 122,70 | 133,50 | 143,20 | 151,80 | 159,50 | 172,50 | |
| C6H12 (г) | 149,90 | 169,10 | 186,70 | 202,90 | 217,50 | 230,60 | - | |
| CH3OH (ж) | 52,21 | 56,03 | 59,64 | 63,04 | 66,23 | 69,22 | - | |
| C2H3OH (ж) | 87,76 | 97,06 | 99,88 | 105,20 | 110,10 | 114,60 | 122,60 |
Таблица 6
Константы диссоциации некоторых слабых кислот при 298 К
| Кислота | К | рК |
| HF | 1,0∙10-3 | 3,00 |
| HCN | 4,9∙10-10 | 9,31 |
| HNO2 | 4,0∙10-4 | 3,40 |
| H2S | 5,7∙10-8 К1 1,2∙10-15 К2 | 7,24 14,92 |
| H2CO3 | 4,2∙10-7 К1 4,8∙10-11 К2 | 6,38 10,32 |
| H3BO3 | 7,3∙10-10 К1 1,8∙10-13 К2 1,6∙10-14 К3 | 9,14 12,74 13,80 |
| H3PO4 | 7,5∙10-3 К1 6,2∙10-8 К2 4,8∙10-13 К3 | 2,13 7,21 12,38 |
| CH3COOH | 1,75∙10-5 | 4,76 |
| C6H5COOH бензойная кислота | 6,2∙10-5 | 4,20 |
| HCOOH | 1,78·10-4 | 3,75 |
| ClCH2COOH хлоруксусная кислота | 1,36∙10-3 | 2,87 |
| C5H5OH | 1,3∙10-10 | 9,89 |
| HOOCCOOH щавелевая кислота | 6,5∙10-2 К1 6,1∙10-5 К2 | 1,19 4,21 |
| (CH2COOH)2 янтарная кислота | 6,4∙10-5 К1 2,7∙10-6 К2 | 4,19 5,57 |
| С6Н8О6 аскорбиновая кислота | 8,0∙10-5 К1 1,6∙10-12 К2 | 4,10 11,79 |
| СН3СНОНСООН молочная кислота | 1,39∙10-4 | 3,86 |
| СН2(СООН)2 малоновая кислота | 4,0∙10-4 К1 9,0∙10-6 К2 | 3,40 5,50 |
| НООССН2С(ОН)(СООН) х СН2СООН лимонная кислота | 8,7∙10-4 К1 1,8∙10-5 К2 4,0∙10-6 К3 | 3,06 4,74 5,40 |
Таблица 7
Константы диссоциации некоторых слабых оснований при 298 К
| Основание | К | рК |
| Аммиак | 1,8∙10-5 | 4,75 |
| Анилин | 3,8∙10-10 | 9,42 |
| Кофеин | 4,1∙10-4 | 3,39 |
| Кокаин | 2,6∙10-6 | 5,59 |
| Креатин | 1,9∙10-11 | 10,72 |
| Этиламин | 5,6∙10-4 | 3,25 |
| Метиламин | 4,4∙10-4 | 3,36 |
| Морфин | 7,4∙10-7 | 6,13 |
| Новокаин | 7,0∙10-6 | 5,16 |
| Пиридин | 1,7∙10-9 | 8,77 |
| Хинин | 1,1∙10-6 К1 1,35∙10-10 К2 | 5,96 9,87 |
| Стрихнин | 1,0∙10-6 К1 2,0∙10-12 К2 | 6,00 11,70 |
| Мочевина | 1,5∙10-14 | 13,82 |
Таблица 8
Значения рН различных систем
| Система | рН |
| 1) Жидкости и ткани организма: сыворотка крови водянистая влага глза слюна чистый желудочный сок молоко кожа печень (внутриклеточная жидкость) | 7,35-7,45 7,40 6,35-6,85 около 0,9 6,6-6,9 6,2-7,5 6,4-6,5 |
| 2) Другие системы: морская вода уксус апельсиновый сок сок грейпфрута томатный сок | 8,0 3,6-4,4 3,2 4,3 8,0 |
Таблица 9
Фундаментальные постоянные
| Постоянная | Значение | |
| в системе СГС | в системе СИ | |
| Число Авогадро (N0) | 6,0225∙1023 | 6,0225∙1023 |
| Постоянная Больцмана (К) | 1,3805∙10-16 эрг/К | 1,3805∙10-23 Дж/К |
| Число Фарадея (F) | 96486,7 Кл/г-экв | 96486,7 Кл/моль |
| Универсальная газовая постоянная (R) | 8,314∙107 эрг/К∙моль | 8,314 Дж/К∙моль |
| Постоянная Планка (h) | 6,6556∙10-27 эрг∙с | 6,6256∙10-34 Дж∙с |
Таблица 10
Эквивалентные электропроводности некоторых электролитов
в бесконечно разбавленных водных растворах (250С)
| Электролит | λ∞ | Электролит | λ∞ | Электролит | λ∞ |
| H2SO4 | 429,8 | KOH | 271,1 | KCl | 149,9 |
| HCl | 426,2 | NH4OH | 271,0 | KNO3 | 145,0 |
| HNO3 | 421,2 | NaOH | 247,8 | NaCl | 126,4 |
Таблица 11
Электролитические подвижности ионов в бесконечно
разбавленных водных растворах
| Ион | λ+ | Ион | λ+ | Ион | λ+ |
| 1/3 Al3+ | 63,0 | K+ | 73,5 | 1/2 Zn2+ | 53,5 |
| 1/2 Ba2+ | 63,7 | Li+ | 38,7 | Brˉ | 78,3 |
| Cs+ | 76,8 | Na+ | 50,1 | Clˉ | 76,3 |
| 1/2 Cu2+ | 54,0 | 1/2 Ni2+ | 54,0 | Fˉ | 55,4 |
| 1/2 Fe2+ | 53,5 | NH4+ | 73,7 | Jˉ | 76,8 |
| 1/3 Fe3+ | 68,0 | 1/2 Pb2+ | 70,0 | NO3ˉ | 71,4 |
| H+ | 349,8 | Pb+ | 77,5 | OHˉ | 197,6 |
| 1/2 SO42ˉ | 80,0 |
Таблица 12
Стандартные электродные потенциалы при 250С и их изотермические
температурные коэффициенты
| Электрод | Электродная реакция | φ0, В | 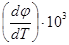 В/град В/град
|
| Li+/Li | Li+ + ē = Li | -3,045 | -0,534 |
| Rb+/Rb | Rb+ + ē = Rb | -2,925 | -1,245 |
| Cs+/Cs | Cs+ + ē = Cs | -2,923 | -1,197 |
| K+/K | K+ + ē = K | -2,925 | -1,080 |
| Ba2+/Ba | Ba2+ + 2ē = Ba | -2,906 | -0,395 |
| Ca2+/Ca | Ca2+ + 2ē = Ca | -2,866 | -0,175 |
| Na+/Na | Na+ + ē = Na | -2,714 | -0,772 |
| Mg2+/Mg | Mg2+ + 2ē = Mg | -2,363 | +0,103 |
| Al3+/Al | Al3+ + 3ē = Al | -1,662 | +0,504 |
| Ti2+/Ti | Ti2+ + 2ē = Ti | -1,628 | - |
| Mn2+/Mn | Mn2+ + 2ē = Mn | -1,180 | -0,080 |
| Se2+/Se | Se2+ + 2ē = Se | -0,770 | - |
| Zn2+/Zn | Zn2+ + 2ē = Zn | -0,763 | +0,091 |
| Cr3+/Cr | Cr3+ + 3ē = Cr | -0,744 | +0,468 |
| SbO2ˉ/Sb | SbO2ˉ + 2H2O + 3ē = Sb + 4OHˉ | 0,670 | - |
| S2ˉ/S | S + 2ē = S2ˉ | -0,510 | - |
| Fe2+/Fe | Fe2+ + 2ē = Fe | 0,440 | +0,052 |
| Cr3+/Cr2+, Pt | Cr3+ + ē = Cr2+ | -0,408 | - |
| Cd2+/Cd | Cd2+ + 2ē = Cd | -0,403 | -0,093 |
| Ti3+/Ti2+, Pt | Ti3+ + ē = Ti2+ | -0,369 | - |
| Ti+/Ti | Ti+ + ē = Ti | -0,336 | -1,327 |
| Co2+/Co | Co2+ + 2ē = Co | -0,277 | +0,060 |
| Mo3+/Mo | Mo3+ + 3ē = Mo | -0,200 | - |
| Ni2+/Ni | Ni2+ + 2ē = Ni | -0,250 | +0,060 |
| Sn2+/Sn | Sn2+ + 2ē = Sn | -0,136 | -0,282 |
| Pb2+/Pb | Pb2+ + 2ē = Pb | -0,126 | -0,451 |
| Ti4+/Ti3+, Pt | Ti4+ + ē = Ti3+ | -0,040 | - |
| 2H+/H2, Pt | 2H+ + ē = ½ H2 | 0,00 | - |
| Sn4+/Sn2+, Pt | Sn4+ + 2ē = Sn2+ | +0,150 | - |
| Cu2+/Cu | Cu2+ + 2ē = Cu | +0,337 | +0,008 |
| OHˉ/O2, Pt | ½ O2 +H2O + 2ē =2 OHˉ | +0,401 | -0,440 |
| Cu+/Cu | Cu+ + ē = Cu | +0,521 | -0,058 |
| 2Jˉ/J2, Pt | J2 + 2ē = 2Jˉ | +0,535 | -0,148 |
| Te4+/Te | Te4+ + 4ē = Te | +0,560 | - |
| MnO4ˉ/MnO42ˉ, Pt | MnO4ˉ + ē = MnO42ˉ | +0,564 | - |
| Fe3+/Fe2+, Pt | Fe3+ + ē = Fe2+ | +0,771 | +1,188 |
| Hg2+/Hg | Hg2+ + 2ē = Hg | +0,788 | - |
| Hg2+/Hg+, Pt | Hg2+ + ē = Hg+ | +0,799 | -1,000 |
| Ag+/Ag | Ag+ + ē = Ag | +0,910 | - |
| 2Brˉ/Br2, Pt | Br2 +2ē = 2Brˉ | +1,065 | -0,629 |
| Pt2+/Pt | Pt2+ + 2ē = Pt | +1,200 | - |
| Mn2+, H+/MnO2, Pt | MnO2 + 4H+ + 2ē = Mn2+ + 2H2O | +1,230 | -0,661 |
| Cr3+/Cr2O72-, H+, Pt | Cr2O72- + 14H+ + 6ē = 2Cr3+ + 7H2O | +1,330 | -1,263 |
| Ti3+/Ti+, Pt | Ti3+ + 2ē = Ti+ | +1,250 | +0,890 |
| Clˉ/Cl2, Pt | Cl2 + 2ē = 2Clˉ | +1,359 | -1,260 |
| Pb2+, H+/PbO2, Pt | PbO2 + 4H+ + 2ē = Pb2+ + 2H2O | +1,455 | -0,238 |
| Au3+/Au | Au3+ + 3ē = Au | +1,498 | - |
| MnO4ˉ, H+/MnO2, Pt | MnO4ˉ+ 4H+ + 3ē = MnO2 + 2H2O | +1,695 | -0,666 |
| SO42ˉ,H+/PbSO4, PbO2 | SO42ˉ + PbO2 + 4H+ + 2ē=PbSO4 +2H2O | +1,682 | +0,326 |
| Au+/Au | Au+ + ē = Au | +1,691 | - |
| 2Fˉ/F2, Pt | F2 + 2ē =2 Fˉ | +2,870 | -1,830 |
Таблица 13
Стандартные потенциалы некоторых окислительно-восстановительных
биологических реакций (водный раствор, 250С, рН = 7,0)
Дата публикования: 2014-11-18; Прочитано: 500 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
