 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Лабораторная работа № 8. Ионно-обменная адсорбция в системе «почва – раствор электролита»
|
|
Ионно-обменная адсорбция в системе «почва – раствор электролита»
Приборы и реактивы: конические колбы объемом 100 мл, 250 мл; бюретки для воды, хлорида натрия С(NaCl)нач = 1 моль/л, трилона Б; фильтры бумажные; воронки; стаканчики для фильтрата; раствор трилона Б С(1/2 Na2H2Y) = 0,01 моль/л; аммонийный буфер (рН = 10); раствор сульфида натрия ω = 2%; раствор гидроксиламина солянокислого, ω = 5%; хромоген черный.
Цель работы: изучение ионно-обменной адсорбции в системе почва-хлорид натрия.
Методика эксперимента
На технических весах взять 5 навесок почвы по 2,0 г и поместить их в конические или круглые плоскодонные колбы емкостью 100 – 200 мл. В каждую колбу налить растворы хлорида натрия разной начальной концентрации, которые готовят из исходного раствора NaCl, молярная концентрация эквивалента которого 1 моль/л путем разбавления водой согласно схеме.
| № колбы | Объем исходного раствора NaCl, мл | Объем воды, мл | Общий объем раствора, мл |
Содержимое колб взбалтывать в течение 20 минут, при этом в системе устанавливается равновесие между ионами Na+ соли и ионами Ca2+ и Mg2+, содержащимися в почве. В общем виде этот ионный обмен можно представить так:
R2Ca + 2Na+ = 2RNa + Ca2+,
где R2, R – органическая составляющая почвы.
После установления равновесия растворам дать отстояться в течение 15-20 минут и отфильтровать их от почвы. Для этого в чистые колбы поместить воронку с фильтром, края которого должны быть на 0,5 см ниже высоты воронки. При фильтровании осторожно слить из колб жидкую фазу.
Получится пять фильтратов (растворов). В них определить суммарную концентрацию Ca2+ и Mg2+, перешедших в раствор из почвы, титрованием трилоном Б.
Трилон Б – органический реагент (натриевая гидросоль этилендиаминтетрауксусной кислоты Na2H2Y), который с катионами Ca2+ и Mg2+ образует внутрикомплексные соединения.
В коническую колбу объемом 250 мл поместить 5 мл фильтрата, добавить 95 мл дистиллированной воды и нагреть смесь до 60-700С, затем прилить 5 мл аммонийного буфера (рН ≈ 10), 0,5 мл раствора Na2S, ω = 2%, 0,5 мл раствора гидроксиламина солянокислого, ω = 5%, добавить 10-15 мг хромогена черного (несколько крупинок) и титровать раствором трилона Б до изменения вишневой окраски в чисто синюю. Результаты записать в таблицу.
| № колбы | Начальная концентрация раствора NaCl, моль/л | Объем трилона Б, пошедшего на титрование, мл | Равновесная концентрация адсорбированных ионов Na+, Г1 | Равновесная концентрация Са2+, Mg2+ на поверхности адсорбента, Г2 | Равновесная концентрация Na+ в растворе, С1 | Равновесная концентрация Са2+, Mg2+ в растворе, С2 | Константа адсорбционного равновесия, Кадс |
Расчет результатов эксперимента
1. Начальная концентрация раствора NaCl в колбах рассчитывается по формуле:  ,
,
где Сисх, Снач – исходная и начальная концентрации растворов NaCl;
Vисх, Vобщ – исходный и общий объем раствора NaCl.
2. Равновесную концентрацию адсорбированных ионов Na+ находят по данным титрования: концентрация Ca2+, Mg2+, перешедших в раствор из почвы, равна концентрации поглощенных ионов Na+, т.е. Г1 = С2.
3. Равновесная концентрация ионов Na+ в растворе (С1) находится как разность (Сисх – Г1).
4. Рассчитанные величины дают возможность построить изотерму адсорбции ионов Na+ в координатах «Г1 – С1».
5. Находят величину Г2 по изотерме, для чего проводят касательную к изотерме адсорбции, которая на оси ординат отсечет отрезок, представляющий собой Г max – максимальную концентрацию ионов Ca2+ и Mg2+, способных к обменной адсорбции.
6. Равновесную концентрацию Ca2+ и Mg2+ на поверхности почвы Г2 находят из соотношения Г2 = Гmax – С2.
7. Константу адсорбционного равновесия Кадс рассчитывают из уравнения: 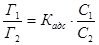 .
.
Дата публикования: 2014-11-18; Прочитано: 586 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
