 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Адсорбция уксусной кислоты почвой
|
|
Опишите следующие основные понятия и закономерности темы:
■ поверхностное натяжение;
■ адсорбция, молекулярная адсорбция;
■ адсорбент, адсорбат, почва – как адсорбент;
■ изотермы адсорбции Лэнгмюра и Фрейндлиха;
■ поверхностно-активные вещества (ПАВ).
Методика эксперимента
В четыре колбы на 250 см3 поместить по 100 мл раствора уксусной кислоты различной концентрации: 0,025 моль/л, 0,05 моль/л, 0,10 моль/л, 0,20 моль/л и добавить по 10 г почвы. Колбочки с растворами встряхивать в течение 15-20 минут для установления адсорбционного равновесия.
Во время отстаивания проб определить точную концентрацию исходных растворов уксусной кислоты титрованием 20,00 мл раствора кислоты раствором гидроксида натрия концентрацией 0,1 моль/л с индикатором. Результаты титрования записать в таблицу.
После установления адсорбционного равновесия растворы отфильтровать отдельно из каждой колбы. Когда отфильтруется весь раствор, в фильтрате определить титрованием равновесную концентрацию уксусной кислоты в четырех пробах так же, как и в случае исходных растворов. Результаты записать в таблицу.
| Начальная концентрация кислоты, моль/л | Объем раствора NaOH, мл, затраченный на титрование | V1cр – V2ср | |||||||
| исходного раствора | равновесного раствора | ||||||||
| титрование № | титрование № | ||||||||
| V1cр | V2ср | ||||||||
| 0,025 | |||||||||
| 0,05 | |||||||||
| 0,10 | |||||||||
| 0,20 |
Адсорбированное количество уксусной кислоты Г выражается числом миллимолей кислоты, приходящейся на 100 г почвы, и определяется по уравнению:
 ,
,
где (V1cр – V2ср) – объем щелочи, эквивалентный количеству уксусной кислоты, адсорбированному из 20,00 мл раствора;
V кис.адс. – объем раствора кислоты, взятый для адсорбции;
С(NаОН) – молярная концентрация щелочи;
Vкис.титр. – объем раствора кислоты, взятый для титрования;
m – масса почвы;
100 – число граммов почвы, на которое производится пересчет адсорбированного количества кислоты.
Подставляя данные опыта, уравнение для расчета адсорбированного количества кислоты принимает вид: Г = 5 (V1cр – V2ср).
Тогда равновесную концентрацию уксусной кислоты можно рассчитать по уравнению:
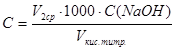 ,
,
которое при Vкис.титр. = 20,00 мл и С(NаОН) = 0,1 моль/л принимает вид: С = 5 ∙ V2ср.
Для построения изотермы адсорбции результаты опыта представляют в таблице:
| Концентрация кислоты, моль/л | Г | С | lgГ | lgС |
| 0,025 | ||||
| 0,05 | ||||
| 0,10 | ||||
| 0,20 |
На миллиметровой бумаге представляется изотерма в координатах «Г – С». Полученная кривая описывается уравнением Фрейндлиха: 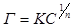 , где Г – количество адсорбированной уксусной кислоты, ммоль/100 г почвы, К и 1/n – константы, определяемые графически. Определив численные значения констант К и 1/n и задаваясь любыми равновесными концентрациями раствора, можно вычислить по уравнению Фрейндлиха количество адсорбированного вещества.
, где Г – количество адсорбированной уксусной кислоты, ммоль/100 г почвы, К и 1/n – константы, определяемые графически. Определив численные значения констант К и 1/n и задаваясь любыми равновесными концентрациями раствора, можно вычислить по уравнению Фрейндлиха количество адсорбированного вещества.
Дата публикования: 2014-11-18; Прочитано: 1984 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
