 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Коагуляция коллоидных систем
|
|
Вариант 1
Изучение коагуляции золя гидроксида железа (III)
Приборы и реактивы: бюретки на 25 мл, пипетки на 5 мл, пробирки в штативе, пробки, карандаш по стеклу, золь гидроксида железа (III), раствор KCl с концентрацией 2 моль/л, раствор Na2SO4 с концентрацией 0,05 моль/л.
Методика эксперимента
а) Определение порога коагуляции под действием хлорида калия.
В 10 пробирок налить по 5 мл золя Fe(OH)3. Затем из бюреток прилить соответствующие количества растворов электролита KCl и воды по схеме (см. таблицу).
| № пробирки | ||||||||||
| Объем воды, мл | 4,5 | 4,0 | 3,5 | 3,0 | 2,5 | 2,0 | 1,5 | 1,0 | 0,5 | |
| Объем KCl, мл | 0,5 | 1,0 | 1,5 | 2,0 | 2,5 | 3,0 | 3,5 | 4,0 | 4,5 | |
| Помутнение + | ||||||||||
| Отсутствие - |
Пробирки закрыть пробками и через 20 минут отметить, в каких пробирках произошла явная коагуляция (помутнение), поставив в таблице знак «+». Записать минимальный объем электролита, необходимый для коагуляции. Рассчитать порог коагуляции γ, моль/л:
γ = 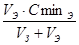 .
.
Определение порога коагуляции электролита Na2SO4 проведите по аналогичной схеме.

 На основании полученных данных установите:
На основании полученных данных установите:
- какие ионы KCl и Na2SO4 электролитов вызывают коагуляцию;
- как валентность иона-коагулянта связана с коагулирующей способностью иона;
- подтверждают ли полученные экспериментальные данные правила Шульце-Гарди.
Вариант 2
Определение порогов коагуляции золя берлинской лазури
Приборы и реактивы: бюретки, пипетки на 5 мл, пробирки в штативе, пробки, карандаш по стеклу, золь берлинской лазури, раствор KCl с начальной концентрацией 2 моль/л.
Методика эксперимента
Приготовить золь берлинской лазури: к 50 мл раствора К4[Fe(CN)6] добавить 60-65 капель раствора FeCl3, непрерывно помешивая смесь.
Для изучения коагуляции золя берлинской лазури см. методику эксперимента варианта 1.
Вопросы для подготовки к лабораторным работам «Влияние среды на набухание желатина» и «Влияние кислоты, щелочи и солей на набухание желатина».
1) Дать определение процесса набухания.
2) Показать и доказать на конкретных примерах избирательность набухания.
3) Что такое неограниченное и ограниченное набухание? Какие параметры системы, а также ВМС изменяются при этом?
4) Степень набухания. Расчет этой величины. Способы определения степени набухания.
5) Степень набухания и роль скоростей набухания различных ВМС в биопроцессах и биосистемах.
6) Вязкость – важная характеристика растворов ВМС. Почему?
7) Расчет и определение молярной массы полимера вискозиметрическим методом.
Дата публикования: 2014-11-18; Прочитано: 488 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
