 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Ионно-обменная адсорбция
|
|
На границе раздела водного раствора и твердого адсорбента практически всегда возникает двойной электрический слой, обусловленный диссоциацией на ионы как растворенных, так и адсорбированных веществ. Кроме того, у ряда адсорбентов существует способность избирательно адсорбировать из раствора ионы одного какого-либо вида.
Адсорбированные ионы на поверхности, находясь в динамическом равновесии с ионами раствора, обмениваются в строго эквивалентном количестве на ионы того же знака, присутствующие в растворе. Такую адсорбцию называют ионно-обменной адсорбцией.
Количественное соотношение между концентрациями обменивающихся ионов устанавливается уравнением Никольского:
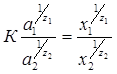 , (5.14)
, (5.14)
где а1 и а2 – активности ионов в равновесном растворе;
х1 и х2 – равновесное количество ионов в твердой фазе;
z1 и z2 – заряды обменивающихся ионов;
К – константа ионного обмена.
Типовые расчеты
Пример 1
При адсорбции аргона коксовым углем при 194,7 К получены следующие результаты:
| Р1, Па | 31,9∙103 | 130,5∙103 | 290,0∙103 |
| Р1, мм.рт.ст. | 24,0 | 98,4 | 218,0 |
| Г1, мг/г | 5,0 | 15,4 | 24,0 |
Рассчитайте постоянные в уравнении Лэнгмюра.
Решение.
Согласно уравнению Лэнгмюра Г/Г∞ является угловым коэффициентом зависимости между Р/Г и Р, а lg 1/КГ∞ - отрезком, отсекаемым этой прямой на оси ординат.
Вычисляем величины Р/Г:
| Р, Па | 31,9∙103 | 130,5∙103 | 290,0∙103 |
| Р/Г | 6,4∙103 | 8,7∙103 | 12,1∙103 |
По полученным данным строим график, отложив по оси абсцисс Р, а по оси ординат – Р/Г:
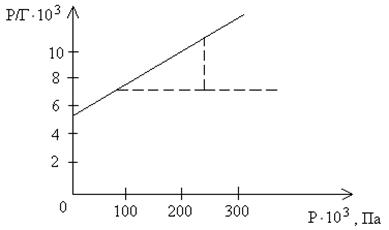
Как видно из графика:
1/Г∞ = (11 - 7) / (240 – 60) = 0,0222
Отсюда Г∞ = 45, 1/КГ∞ = 5,7∙103, тогда
К = 1 / 5,37 ∙ 45 = 0,004.
Пример 2
При исследовании поверхностной активности растворов уксусной кислоты при 200С были получены следующие результаты:
| Концентрация кислоты, моль/л | 0,00 | 0,01 | 0,10 | 0,50 | 1,00 |
| Поверхностное натяжение, дин/см | 73,26 | 70,02 | 66,88 | 61,66 | 57,28 |
Найти величины Г, δ и площади, занимаемой одной молекулой уксусной кислоты при разных концентрациях.
Решение.
Воспользуемся уравнением Гиббса 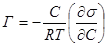 . Находим средние значения Сср, ∆С, ∆σ и ∆σ/∆С (см. таблицу).
. Находим средние значения Сср, ∆С, ∆σ и ∆σ/∆С (см. таблицу).
| Сср | ∆С | ∆σ | ∆σ/∆С |
С1 =  =0,005 =0,005
| 0,01-0,00=0,01 | 70,02-73,26= -3,24 | -3,24/0,01= -324 |
С2 = 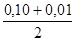 =0,055 =0,055
| 0,1-0,01=0,09 | 66,88-70,02= -3,14 | -3,14/0,09= -34,9 |
С3 = 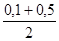 =0,300 =0,300
| 0,5-0,1=0,04 | 61,16-66,88= -5,22 | -5,22-0,4= -13,05 |
С4 = 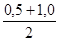 =0,750 =0,750
| 1,0-0,5=0,5 | 57,28-61,66= -4,38 | -4,38/0,5= -8,76 |
По уравнению Гиббса вычисляем величину адсорбции:
Г1 = 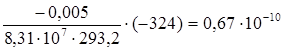 моль/см2,
моль/см2,
Г2 = 0,8 ∙ 10-10 моль/см2,
Г3 = 1,65 ∙ 10-10 моль/см2,
Г4 = 2,75 ∙ 10-10 моль/см2.
Площади, занимаемые одной молекулой уксусной кислоты при данной концентрации, вычисляем по уравнению (5.11):
S1 = 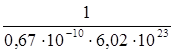 = 0,25 ∙ 10-13 см2,
= 0,25 ∙ 10-13 см2,
S2 = 0,21 ∙ 10-13 см2,
S3 = 0,11 ∙ 10-13 см2,
S4 = 0,06 ∙ 10-13 см2.
Тогда толщину адсорбционного слоя для Г4 вычисляем по формуле:
δ = 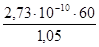 = 1,6 ∙ 10-9,
= 1,6 ∙ 10-9,
где 60 – молярная масса уксусной кислоты, г/моль;
1,05 – плотность уксусной кислоты, г/см3.
Пример 3
Зависимость поверхностного натяжения водных растворов амилового спирта (С5Н11ОН) от концентрации при 250С выражается следующим образом:
| Концентрация, кмоль/м3 | Поверхностное натяжение, мН/м |
| 72,0 | |
| 0,0019 | 70,4 |
| 0,0038 | 69,2 |
| 0,0075 | 66,7 |
| 0,0150 | 61,7 |
| 0,0300 | 55,3 |
| 0,0600 | 46,6 |
| 0,1200 | 38,0 |
Графическим способом определите величину адсорбции амилового спирта из раствора с концентрацией 0,030 кмоль/м3.
Решение.
Построим график зависимости поверхностного натяжения от концентрации. Проведем касательную к кривой в стыке, имеющей ординату 0,030 кмоль/м3. Тангенс угла наклона касательной к оси абсцисс равен  .
.
Из графика находим:
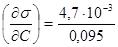 = -0,495 Н/м2 кмоль.
= -0,495 Н/м2 кмоль.
Множитель 10-3 в числителе связан с тем, что σ в таблице и на рис. выражено в мН/м. По уравнению изотермы адсорбции Гиббса находим:
Г = 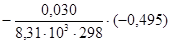 = 5,95∙10-9 кмоль/м2.
= 5,95∙10-9 кмоль/м2.
Пример 4
Рассчитайте количество ммоль аммиака, адсорбированное 100 г почвы, если равновесное количество NH3 равно 12,5 ммоль/л, а константы К и 1/n, определенные экспериментально, соответственно равны 5,01 и 0,30.
Решение.
Расчеты производятся по уравнению Фрейндлиха, представленного в логарифмической форме: 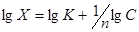 . Подставляя числовые данные, получим: lgХ = 0,70 + 0,3291 = 1,0291, Х = 10,69 ммоль/100 г.
. Подставляя числовые данные, получим: lgХ = 0,70 + 0,3291 = 1,0291, Х = 10,69 ммоль/100 г.
Дата публикования: 2014-11-18; Прочитано: 610 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
