 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Типи окисно-відновних реакцій
|
|
Розрізняють 5 основних типів окисно-відновних реакцій:
1. Реакції, в яких приймають участь один відновник і один окисник, наприклад:
РbS + O2 = PbO + SO2.
Підбір коефіцієнтів здійснюємо методом електронного балансу за лівою стороною реакції
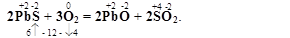
2. Реакції, у яких приймають участь два відновники і один окисник, наприклад
FeS2 + O2 = Fe2O3 + SO2.
Визначаємо коефіцієнти за лівою стороною реакції
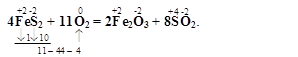
У цій реакції відновниками є атоми заліза і сірки. Атом заліза віддає 1е, два атоми сірки – 10е. Разом 11е. Окисником є молекула кисню, яка приймає 4 електрони.
3. Реакції, у яких крім окисно-відновного процесу відбувається обмінна реакція, наприклад
KMnO4 + HCl = KCl + MnCl2 + Cl2 + H2O.
Підбір коефіцієнтів для реакції цього типу здійснюємо лише за правою стороною реакції
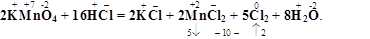
Десять іонів Хлору є відновником, а решта шість приймають участь в обмінній реакції, зв¢язуючи йони К+ і Mn2+.
4. Реакції самоокиснення - самовідновлення). Це такі окисно-відновні реакції, в яких окисник і відновник - один і той же елемент. Підбір коефіцієнтів здійснюємо також лише за правою стороною реакції, наприклад

5. Реакції внутрішньомолекулярного окиснення-відновлення. До цього типу належать реакції, в яких окисник і відновник перебувають всередині однієї й тієї ж молекули. Підбір коефіцієнтів здійснюють за правою стороною реакції, наприклад
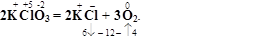
Дата публикования: 2015-09-18; Прочитано: 839 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
