 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Определение значений RF аминокислот
|
|
Величина Rf аминокислоты в данном растворителе, представляющая собой отношение скорости движения фронта растворителя к скорости движения данной аминокислоты, не является строго постоянной величиной. Значения Rf аминокислот в данном растворителе изменяются в зависимости от сорта хроматографической бумаги, рН растворителя, температуры проявления, ряда сопутствующих веществ и некоторых других факторов. Например, в растворителе м-крезол, насыщенный водой, Rf аминокислоты валина при рН 4,0 равняется 0,41, а при рН 6,0 составляет 0,50; Rf аргинина при рН 8,0 равняется 0,10, а при рН 10,0 —0,75; Rf лизина при рН 10,0 равняется 0,45, а при рН 11,0 — 0,10 и т. д. В растворителе н-пропиловый спирт — вода в соотношении 9: 1 при повышении температуры проявления от 10 до 50°С значения Rf глицина, аланина, валина и ряда других аминокислот значительно увеличиваются. Поэтому перед началом определения аминокислот хроматографией на бумаге рекомендуется проверить значение Rf изучаемых аминокислот с использованием соответствующих растворителей, бумаги и методов работы.
Ход определения. Стандартные растворы аминокислот готовят в концентрации ~10 мг аминокислоты в 1 мл. Некоторые аминокислоты (тирозин, аспарагиновая кислота) в воде растворяются плохо, поэтому при их растворении добавляют по нескольку капель НС1. На листы или полосы (шириной 15—20 см) хроматографической бумаги на расстоянии 2,5—3 см микропипеткой наносят такое количество раствора каждой аминокислоты, чтобы содержание любой из них в местах нанесения было не менее 15—20мкг, а для триптофана, гистидина, тирозина, лизина и пролина не менее 20—30 мкг. После подсыхания пятен хроматограммы закрепляют в камере и приливают растворитель.
При хроматографировании аминокислот в качестве растворителей используют смесь н-бутилового спирта, ледяной уксусной кислоты и воды в соотношении 4:1:1 или насыщенный водой фенол. При приготовлении первого растворителя указанные реактивы в необходимых соотношениях тщательно перемешивают и, если растворитель получается недостаточно прозрачным, к нему добавляют еще несколько капель уксусной кислоты. Для приготовления насыщенного водой фенола к 300 г перегнанного фенола добавляют 105 мл воды и тщательно перемешивают. Хроматограммы выдерживают в камере с растворителем в течение 25—30 часов, за этот срок фронт растворителя продвинется почти до нижнего края листа бумаги.
После экспозиции бумагу осторожно вынимают из камеры, отмечают карандашом расстояние, пройденное фронтом растворителя, и кладут в вытяжной или в специальный сушильный шкаф. Растворитель бутанол — уксусная кислота — вода испаряется за несколько часов, а фенол — за 1—2 дня.
После удаления растворителя из бумаги сухую бумагу опрыскивают из пульверизатора 0,2%-ным раствором нингидрина в ацетоне или в бутиловом спирте, кладут в термостат на 5—10 минут при температуре 80—90° или оставляют при комнатной температуре на 12—20 часов. При этом между аминокислотами и нингидридом происходит следующая реакция:

 Аминокислоты окисляются и распадаются на альдегиды, углекислоту и аммиак. Выделившийся аммиак конденсируется со второй молекулой нингидрина и с продуктом его восстановления — дикетооксигидринденом:
Аминокислоты окисляются и распадаются на альдегиды, углекислоту и аммиак. Выделившийся аммиак конденсируется со второй молекулой нингидрина и с продуктом его восстановления — дикетооксигидринденом:
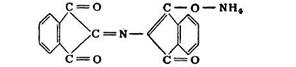
Аммиачная соль энольной формы образовавшегося соединения окрашена в интенсивный сине-фиолетовый цвет. Интенсивность окраски пропорциональна содержанию аминокислот.
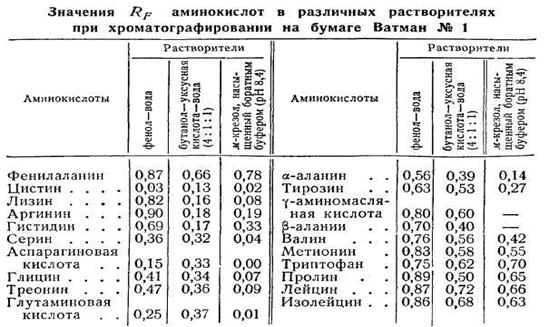
Для вычисления значений Rf окрашенные пятна аминокислот обводят простым карандашом, определяют центры пятен и расстояние от места нанесения аминокислот, выраженное в миллиметрах, делят на расстояние, пройденное от этой же точки фронтом растворителя.
В таблице 2 приведены значения Rf аминокислот о различных растворителях при хроматографировании на бумаге Ватман № 1. Оборудование и реактивы. 1) Хроматографические камеры. 2) Шкаф для сушки хроматограмм. 3) Штатив для нанесения растворов аминокислот на бумагу. 4) Пульверизаторы для опрыскивания хроматограмм. 5) Хроматографическая бумага. 6) Микропипетки.
7) Колбы мерные. 8) Листы стекла. 9) Медицинские перчатки. 10) Пипетки. 11) Набор аминокислот. 12) Нингидрин. 13) Ацетон. 14) Фенол 15) Бутиловый спирт. 16) Уксусная кислота ледяная. 17) Цианистый калий.
Дата публикования: 2015-11-01; Прочитано: 4555 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
