 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Адсорбция ионов из растворов
|
|
В зависимости от природы адсорбента процессы адсорбции ионов электролитов подразделяются на ионную адсорбцию и ионообменную адсорбцию (разд. 26.4.4).
Ионная адсорбция заключается в адсорбции ионов из растворов электролитов на поверхности твердых веществ, кристаллическая решетка которых состоит из ионов или полярных молекул, т. е. на полярных адсорбентах. Ионная адсорбция имеет ряд характерных особенностей.
1. При ионной адсорбции на поверхности адсорбента вследствие адсорбции ионов, называемых потенциалопределяющими, возникает определенный заряд, который притягивает из раствора противоположно заряженные ионы - противоионы; в результате на границе раздела фаз возникает двойной электрический слой.
2. Скорость ионной адсорбции меньше скорости молекулярной адсорбции, так как скорость диффузии сольватированных ионов меньше скорости диффузии молекул и, кроме того, адсорбции ионов предшествует более медленный, чем у молекул, процесс десольватации.
3. Ионная адсорбция не всегда обратима, так как она может сопровождаться хемосорбцией, приводящей, например, к образованию малорастворимого вещества.
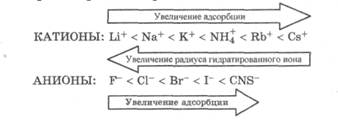
4. Адсорбируемость ионов определяется величиной их заряда, радиуса и степенью сольватации. При равенстве заряда лучше адсорбируются ионы с большим радиусом, так как они менее сольва-тированы. По величине адсорбции ионы располагаются в так называемые лиотропные ряды, которые для водных систем выглядят так:
Многозарядные ионы адсорбируются лучше однозарядных, исключение составляет катион водорода:

5. Если в растворе электролита имеются такие же ионы, как и в составе твердого адсорбента, то ионная адсорбция принимает строго избирательный характер, описываемый правилом Панета - Фаянса - Пескова об избирательной ионной адсорбции.
На поверхности кристалла преимущественно адсорбируются те ионы, которые входят в состав кристаллической решетки адсорбента или изоморфны им по строению и могут достроить кристаллическую решетку.
Иллюстрацией этого правила может служить зарядка поверхности кристаллического осадка иодида серебра, полученного по реакции:

Если количества KI и AgNO3 эквивалентны, то поверхность осадка не заряжена. При избытке KI поверхность осадка заряжена отрицательно за счет адсорбции потенциалопределяющих ионов I:

 |
а при избытке AgNO3 - положительно за счет адсорбции ионов Ag+:
Следовательно, потенциалопределяющие ионы, внедряясь в кристаллическую структуру, в результате избирательной адсорбции сообщают соответствующий заряд поверхности кристалла, а противоионы нейтрализуют этот заряд, оставаясь в растворе. Избирательная ионная адсорбция имеет место при формировании кристаллической решетки электролитов и способствует очистке таких веществ путем перекристаллизации. Она также определяет процессы образования коллоидных частиц (разд. 27.2.1).
Дата публикования: 2014-10-16; Прочитано: 6823 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
