 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Адсорбция на подвижной поверхности раздела фаз
|
|
В соответствии со II законом термодинамики свободная поверхностная энергия жидкостей стремится к минимуму. В чистых жидкостях уменьшение этой энергии может произойти только путем сокращения поверхности. В растворах свободная поверхностная энергия может понижаться за счет уменьшения удельного поверхностного натяжения в результате адсорбции растворенного вещества в поверхностном слое жидкости, приводящей к изменению его состава. Адсорбция растворенных веществ на поверхности жидких адсорбентов описывается уравнением Гиббса, отражающим зависимость между концентрацией вещества на единице поверхности раздела фаз и концентрацией его в объеме раствора:

 |
где Г - величина удельной адсорбции растворенного вещества, измеряемая количеством молей этого вещества, приходящихся на единицу площади поверхности адсорбента, моль/дм2; с - равновесная молярная концентрация растворенного вещества, моль/л; -(d
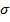 /dc) - понижение удельного поверхностного натяжения, вызванное повышением концентрации растворенного вещества в поверхностном слое.
/dc) - понижение удельного поверхностного натяжения, вызванное повышением концентрации растворенного вещества в поверхностном слое.
Рис. 26.6. Зависимость поверхностного натяжения водных растворов от концентрации в них ПАВ (а) и ПИВ (б)
Величина d 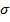 /dc, называемая поверхностной активностью, служит характеристикой поведения растворенного вещества при его адсорбции поверхностью раздела. Поверхностная активность может быть положительной или отрицательной. Если с увеличением концентрации вещества удельное поверхностное натяжение на границе раздела фаз понижается, т. е. d
/dc, называемая поверхностной активностью, служит характеристикой поведения растворенного вещества при его адсорбции поверхностью раздела. Поверхностная активность может быть положительной или отрицательной. Если с увеличением концентрации вещества удельное поверхностное натяжение на границе раздела фаз понижается, т. е. d 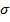 /dc < О, то такое вещество называют поверхностноактивным (ПАВ). В этом случае адсорбция растворенного вещества положительна (Г > 0); это означает, что концентрация растворенного вещества в поверхностном слое больше, чем в объеме раствора (рис. 26.6, а).
/dc < О, то такое вещество называют поверхностноактивным (ПАВ). В этом случае адсорбция растворенного вещества положительна (Г > 0); это означает, что концентрация растворенного вещества в поверхностном слое больше, чем в объеме раствора (рис. 26.6, а).
Вещества, повышающие удельное поверхностное натяжение на границе раздела фаз с увеличением их концентрации, называют поверхностно-инактивными (ПИВ), для них d 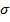 /dc > 0, а адсорбция отрицательна (Г < 0). Отрицательная адсорбция означает, что концентрация растворенного вещества в объеме больше, чем в поверхностном слое раствора (рис. 26.6, б). Примером ПИВ по отношению к воде являются неорганические соли, кислоты и щелочи, молекулы или ионы которых взаимодействуют с водой сильнее, чем молекулы воды между собой. Кроме того, молекулы этих веществ более полярны, чем молекулы воды. Вследствие высокой энергии гидратации молекулы или ионы этих веществ втягиваются в глубину раствора. Поэтому в растворах сильных электролитов пограничный слой толщиной в несколько молекулярных слоев состоит преимущественно из молекул воды, а ионы солей там содержатся в очень малой концентрации, попадая в поверхностный слой только благодаря тепловому движению. Из-за такого состава поверхностного слоя и вследствие усиления полярных свойств системы в целом поверхностное натяжение таких растворов незначительно повышается в сравнении с чистым растворителем (см. рис. 26.6, б).
/dc > 0, а адсорбция отрицательна (Г < 0). Отрицательная адсорбция означает, что концентрация растворенного вещества в объеме больше, чем в поверхностном слое раствора (рис. 26.6, б). Примером ПИВ по отношению к воде являются неорганические соли, кислоты и щелочи, молекулы или ионы которых взаимодействуют с водой сильнее, чем молекулы воды между собой. Кроме того, молекулы этих веществ более полярны, чем молекулы воды. Вследствие высокой энергии гидратации молекулы или ионы этих веществ втягиваются в глубину раствора. Поэтому в растворах сильных электролитов пограничный слой толщиной в несколько молекулярных слоев состоит преимущественно из молекул воды, а ионы солей там содержатся в очень малой концентрации, попадая в поверхностный слой только благодаря тепловому движению. Из-за такого состава поверхностного слоя и вследствие усиления полярных свойств системы в целом поверхностное натяжение таких растворов незначительно повышается в сравнении с чистым растворителем (см. рис. 26.6, б).
Дата публикования: 2014-10-16; Прочитано: 4912 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
