 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Окислительно-восстановительные свойства карбоновых кислот и их производных
|
|
Карбоновые кислоты могут быть окислителями за счет протона карбоксильной группы. За счет углеродных атомов в положениях а и B, а также карбонильной группы карбоновые кислоты и особенно их производные могут проявлять и окислительные, и восстановительные свойства в зависимости от свойств реагента и условий реакции.
Протон кислоты — окислитель. Карбоновые кислоты за счет протона карбоксильной группы окисляют металлы, стоящие в ряду напряжений до водорода:

Окислительно-восстановительные свойства углеродного атома карбоксильной группы (реакция декарбоксилирования). В отличие от других карбоновых кислот, атом углерода карбоксильной группы муравьиной кислоты НСООН имеет степень окисления +2, так как эта кислота содержит не ацильную, а альдегидную
группу  . Поэтому для муравьиной кислоты характерна
. Поэтому для муравьиной кислоты характерна
реакция серебряного зеркала, т. е. восстановление катионов серебра до чистого серебра. В этой реакции углеродный атом карбоксильной группы выступает восстановителем. При этом сама муравьиная кислота превращается в СО2 и Н2О, т. е. происходит ее декарбоксилирование:

 |
При нагревании до 300°С солей кальция и бария насыщенных карбоновых кислот они подвергаются декарбоксилированию с одновременным внутримолекулярным ацилированием возникающего карбаниона с образованием кетона:
за счет углеродных атомов карбонильных групп, один из которых выступает окислителем  а другой – восстановителем
а другой – восстановителем 
При сплавлении со щелочью ацетат натрия декарбоксилируется с образованием метана и карбоната натрия:
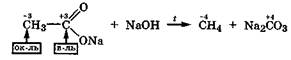
В этой реакции также наблюдается внутримолекулярная окислительно-восстановительная дисмутация за счет карбонильного атома углерода и а-углеродного атома.
Рассмотренные примеры показывают, что в реакциях декарбоксилирования углеродные атомы карбоксильной группы могут быть и восстановителями, и окислителями. Эти реакции могут иметь гомолитический (свободнорадикальный) или гете-ролитический (электрофильно-нуклеофильный) механизм. Свободнорадикальный механизм более вероятен для высокотемпературных реакций, а электрофильно-нуклеофильный - для каталитических и ферментативных реакций.
Окисление а-углеродного атома и реакции конденсации с его участием. Электроноакцепторный эффект карбоксильной группы повышает подвижность водородных атомов, связанных с a-углеродным атомом, и склонность этого углеродного атома к окислительно-восстановительным превращениям. В результате при галогенировании карбоновых кислот атомы галогена вводятся в 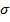 -положение. Так, при хлорировании уксусной кислоты хлором последовательно замещаются все три водородных атома а-метильной группы, при этом а-углеродный атом проявляет восстановительные свойства:
-положение. Так, при хлорировании уксусной кислоты хлором последовательно замещаются все три водородных атома а-метильной группы, при этом а-углеродный атом проявляет восстановительные свойства:

Реакция хлорирования уксусной кислоты протекает по свободнорадикальному механизму.
Рассмотрим реакции конденсации с участием а-углеродного атома. В сильноосновной среде (спиртовый раствор алкоголята натрия) а-водородный атом одной молекулы сложного эфира карбоновой кислоты, например этилацетата, отщепляется в виде протона и на а-углеродном атоме возникает карбанион. Этот активный С-нуклеофил атакует углеродный атом карбонильной группы (электрофильный центр) другой молекулы эфира с возникновением новой С—С-связи. При этом образуется эфир Р-кетокарбоновой кислоты, например этилацетоацетилоат в случае конденсации этилацетата:

Подобная реакция называется сложноэфирной конденсацией или конденсацией Кляйзена. Ее обычно рассматривают как нуклеофильное замещение у карбонильного атома углерода, т. е. как реакцию С-ацилирования. Однако важен и тот факт, что в этой реакции происходит межмолекулярная окислительно-восстановительная дисмутация, в которой окислителем (электрофилом) является карбонильный углеродный атом одной молекулы, а восстановителем (нуклеофилом) - а-углеродный атом другой молекулы.
В организме, несмотря на водную среду, подобная конденсация чрезвычайно распространена в метаболизме карбоновых кислот, но она происходит с тиоэфирами-ацилкоферментами А при участии соответствующих ферментов. Так, при конденсации двух молекул ацетилкофермента А образуется ацетоацетилкофермент А:

Окислительно-восстановительные реакции, сопровождаемые образованием или разрывом связей С—С, лежат в основе метаболизма карбоновых кислот в организме (разд. 19.4).
Дата публикования: 2014-10-16; Прочитано: 6200 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
