 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Задача №4
|
|
Определите стандартную теплоту образования соединения (табл. 4) из простых веществ, если известна его теплота сгорания при температуре Т =298 К и давлении р = 1,0133·105 Па. Принять, что продуктами сгорания являются CO2 (Г), H2О (Ж), и N2 (Г).
Использовать известные теплоты сгорания простых веществ:
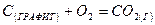 DН= – 393,795 кДж/моль;
DН= – 393,795 кДж/моль;
 DН= – 286,043 кДж/моль.
DН= – 286,043 кДж/моль.
Таблица 4
| Вариант | Вещество | 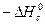 , кДж/моль , кДж/моль
|
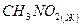 нитрометан нитрометан
| 709,278 | |
 нитроэтан нитроэтан
| 981,852 | |
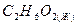 этиленгликоль этиленгликоль
| 1180,315 | |
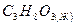 глицерин глицерин
| 1662,239 | |
 диметиламин диметиламин
| 1774,229 | |
 ацетон ацетон
| 1787,012 | |
 циклогексан циклогексан
| 3919,910 | |
 этилацетат этилацетат
| 2246,390 | |
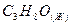 пропанол-1 пропанол-1
| 2011,853 | |
 этанол этанол
| 1370,680 | |
 амиловый спирт амиловый спирт
| 3323,222 | |
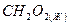 муравьиная кислота муравьиная кислота
| 254,580 | |
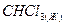 * хлороформ * хлороформ
| 428,060 | |
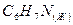 анилин анилин
| 3398,588 | |
 диэтиловый эфир диэтиловый эфир
| 2726,710 | |
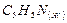 пиридин пиридин
| 2577,140 | |
 валериановая кислота валериановая кислота
| 2853,859 | |
 толуол толуол
| 3950,769 | |
 октан октан
| 5516,163 | |
 муравьиная кислота муравьиная кислота
| 254,580 |
Продолжение таблицы 4
| Вариант | Вещество | 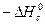 , кДж/моль , кДж/моль
|
 бутанол бутанол
| 2671,900 | |
 ** хлорметан ** хлорметан
| 759,940 | |
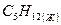 пентан пентан
| 3509,200 | |
 уксусная кислота уксусная кислота
| 874,580 | |
 нитробензол нитробензол
| 2884,00 | |
 ** хлорбензол ** хлорбензол
| 3110,300 | |
 м-ксилол м-ксилол
| 4551,810 | |
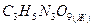 нитроглицерин нитроглицерин
| 1541,400 | |
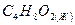 1,4-диоксан 1,4-диоксан
| 2316,560 | |
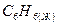 бензол бензол
| 3267,580 |
* Продукты сгорания: CO2 (Г), Cl2(Ж) и HCl (Р-Р);
** Продукты сгорания: CO2 (Г), H2О(Ж) и HCl (Р-Р).
Решение:
Вычислим стандартную теплоту образования карбамида 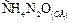 . По определению теплота образования – это тепловой эффект реакции образования одного моля вещества из простых веществ при стандартных условиях. Следовательно, в задаче требуется найти тепловой эффект реакции:
. По определению теплота образования – это тепловой эффект реакции образования одного моля вещества из простых веществ при стандартных условиях. Следовательно, в задаче требуется найти тепловой эффект реакции:
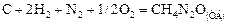 +
+  .
.
Для решения задачи применим метод комбинирования термохимических уравнений.
Воспользуемся изменениями энтальпий следующих реакций:
(а) 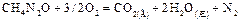 , DН1= –634,749 кДж/моль.
, DН1= –634,749 кДж/моль.
(b)  , DН2 = – 393,795 кДж/моль.
, DН2 = – 393,795 кДж/моль.
(c) 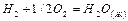 , DН3 = – 286,043 кДж/моль.
, DН3 = – 286,043 кДж/моль.
Необходимая нам реакция образования карбамида из простых веществ получается при сложении термохимических уравнений (b) и (c), за вычетом уравнения (а). Уравнение (c) необходимо умножить на коэффициент 2. Следовательно,

 = –393,795 + 2·(–286,043) – (–634,749) = –331,132 кДж/моль.
= –393,795 + 2·(–286,043) – (–634,749) = –331,132 кДж/моль.
Справочная величина теплоты образования карбамида
 = –333,170 кДж/моль.
= –333,170 кДж/моль.
Дата публикования: 2014-11-18; Прочитано: 2751 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
