 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Программы для самостоятельной работы
|
|
Программа 1
1. Если в реакцию 1-го порядка вступает 1000 молекул и за одну секунду 500 из них распадаются, то сколько молекул распадается за 2 секунды?
2. Будет ли скорость химической реакции более чувствительна к температуре при возрастании энергии активации? Какая из реакций: каталитическая или некаталитическая более чувствительна к изменению температуры, если предположить, что изменение температуры не влияет на катализатор?
Программа 2
1. Рассчитать период полупревращения для реакции омыления метилацетата в растворе гидроксида натрия, если начальная концентрация каждого реагента 0,03 моль/л. Реакция протекает при 250С, и константа скорости при этой температуре составляет 11,5 л∙моль-1∙мин-1.
2. Химическую реакцию изучают при 270С и 370С. Константы скорости прямой реакции при этих температурах равны 3,4 и 8,5 мин-1. Рассчитать энергию активации для данной реакции.
Программа 3
1. Каталитическое разложение пероксида водорода является реакцией первого порядка. Константу реакции изучали путем титрования проб одинакового объема раствором KMnO4. Результаты титрования приведены в таблице.
| t, мин | |||
| V, KMnO4, мл | 22,8 | 13,8 | 8,25 |
Определить константу скорости реакции разложения Н2О2.
2. Энергия активации реакции разложения HJ равна 183,92 кДж/моль. Определить долю молекул, обладающих энергией, достаточной для разложения при 400 и 500 К.
Программа 4
1. Период полураспада одного из радиоактивных изотопов кобальта равен 5,3 года. Считая реакцию распада реакцией I порядка, определить константу скорости.
2. Скорость реакции термического разложения бромистого этила подчиняются уравнению реакции первого порядка, и константа скорости описывается выражением:
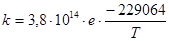 сек-1.
сек-1.
Определить температуру, при которой за один час разлагается 70% вещества.
Программа 5
1. Константа скорости омыления этилацетата едким натром при 100С равна 2,38 л∙моль-1∙мин-1. Найти период полураспада при этой температуре, если смешать 1 л раствора этилацетата и 1 л раствора NаОН с начальной концентрацией 0,05 моль/л.
2. Зависимость константы скорости реакции первого порядка разложения N2О5 от температуры описывается выражением:
 сек-1.
сек-1.
Рассчитать время, за которое распадается 90% N2О5 при температуре 500С.
Программа 6
1. После фотоокисления в присутствии метиленового синего отбирают пробы и спектрофотометрически титруют N – этилмалеимидом. Результаты титрования при 200С приведены в таблице.
| Время, мин | |||||
| Оптическая плотность | 0,145 | 0,120 | 0,091 | 0,052 | 0,033 |
Определить константу скорости и период полураспада при 200С.
2. Каков период полураспада SiН4 при 7000С, если зависимость константы скорости от температуры описывается выражением:
 сек-1.
сек-1.
Программа 7
1. Период полураспада 90Sn равен 28,1 лет. Если начальная масса изотопа 1 г, то какая масса его останется к 18 и 70 годам?
2. При определенной температуре за 10 часов разложилось 30% вещества. Считая реакцию разложения реакцией первого порядка, определить, сколько времени потребуется для разложения 99% вещества.
Программа 8
1. Период полураспада изотопа 14С равен 5730 лет. Археологический образец содержит древесину, которая имела только 72% 14С по отношению к живым деревьям. Каков возраст образца?
2. Реакция имеет энергию активации 64790 Дж/моль и константу скорости при 200С, равную 1,2 мин-1. Рассчитать константу скорости при 00С.
Программа 9
1. Для реакции омыления метилацетата щелочью при 200С изменение концентрации щелочи со временем показано в таблице.
| t, мин | |||||||
| С (NaOH), моль/л∙103 | 10,00 | 7,40 | 6,34 | 5,50 | 4,64 | 3,63 | 2,54 |
Показать графически, что реакция омыления является реакцией второго порядка и определить константу скорости при 250С.
2. Реакция второго порядка за 500 сек протекает на 20%. За какое время она пройдет на 60%?
Программа 10
1. Константа скорости реакции первого порядка SO2Cl2 = SO2 + Cl2, при 3200С равна 2,2∙10-5 сек-1. Какой процент разложится при 3200С в течение 2 часов?
2. Вещество А смешивается с веществами В и С равных концентраций 1 моль/л. Через 1000 сек останется 50% вещества А. Сколько вещества А останется через 2000 сек, если реакция имеет: первый порядок, второй порядок?
Программа 11
1. Реакция C4H9J + OHˉ = Jˉ + C4H9OH имеет второй порядок и константу скорости 39,1 л∙моль-1∙мин-1 при 00С. Был приготовлен раствор, содержащий 0,004 моль/л йодистого бутила и 0,005 моль/л NаОН. Через какое время прореагирует 90% йодистого бутила?
2. Константа скорости реакции 2N2О = 2N2 + О при 9000С равна 5∙10-4 сек-1. Начальная концентрация N2О равна 3,2 моль/л. Определить скорость реакции при указанной температуре, когда N2О разложится на 78%.
Программа 12
1. Энергия активации разложения HJ составляет 183,92 кДж/моль. Какая доля молекул обладает энергией, достаточной для разложения при 4000 и 5000С?
2. Период полураспада радиоактивного изотопа 137Cs, который попал в атмосферу в результате Чернобыльской аварии 29,7 лет. Через сколько лет количество изотопа составит лишь 1% от исходного?
Программа 13
1. Чему равна доля активных молекул для некоторой реакции с энергией активации 100 кДж/моль при температуре 100 и 1000 К?
2. Установлено, что реакция второго порядка завершается на 75% за 92 минуты при исходной концентрации реагента 0,26 моль/л. Какое время потребуется, чтобы при тех же условиях концентрация реагента достигла 0,16 моль/л?
Программа 14
1. Рассчитать увеличение (в %) доли активных столкновений для реакции с энергией активации 100 кДж/моль при изменении температуры 2000С до 2100С.
2. Превращение бензилового спирта в бензиловый эфир (реакция первого порядка) при 600С произошло за 10 минут на 75,2%. Вычислить константу скорости реакции.
Программа 15
1. Для реакции разложения ацетонкарбоновой кислоты в водном растворе получены следующие значения констант скорости:
| t0C | ||||
| k ∙ 105 сек-1 | 2,46 | 47,5 |
Построить график зависимости «lg k – 1/Т» и определить энергию активации.
2. Для вышеприведенной реакции определить константу скорости и период полураспада при 800С.
Дата публикования: 2014-11-18; Прочитано: 1932 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
