 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Коллигативные свойства растворов электролитов
|
|
Для растворов электролитов уравнения законов Рауля и Вант-Гоффа принимают вид:
∆Р = iР0N, ∆Тзам = iКс, ∆Ткип = iЕс, π = iсRT, (3.10)
где i – изотонический коэффициент Вант-Гоффа.
Изотонический коэффициент связан с величиной степени диссоциации α электролита следующим уравнением:
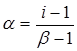 , (3.11)
, (3.11)
где β – число ионов, на которое распадается молекула электролита.
Типовые расчеты
Пример 1
Рассчитайте молярную массу неэлектролита, если 28,5 г этого вещества, растворенного в 785 г воды, вызывает понижение давления пара над раствором на 52,37 Па при 400С. Давление водяного пара при этой температуре равно 7375,9 Па.
Решение.
Согласно закону Рауля ∆Р = Р0 ∙ N, тогда:
N = ∆Р / Р0 = 52,37 / 7375,9 = 0,0071.
Мольная доля растворенного вещества 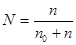 .
.
Число молей растворителя  = 43,61 моль.
= 43,61 моль.
Число молей растворенного вещества 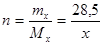 .
.
 , х = 91,40.
, х = 91,40.
Мх = 91,40 г/моль.
Пример 2
Удельная теплота испарения воды при температуре кипения равна 2253 Дж/г. Определить температуру кипения водного раствора, содержащего 0,05 моль нелетучего растворенного вещества в 200 г воды.
Решение.
Из уравнения 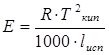 , тогда
, тогда 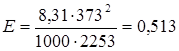 .
.
∆Ткип = Е ∙ с, с = 0,05 / 0,2 = 0,25 моль/кг, ∆Ткип = 0,513 ∙ 0,25 = 0,1280С.
Ткип = 1000 + 0,1280 = 100,1280С.
Пример 3
Сколько граммов: а) этиленгликоля; б) хлорида кальция (считать, что в растворе соль полностью диссоциирована) следует прибавить в 10-литровый сосуд с водой, чтобы раствор замерз при -50С?
Решение.
а) Используя уравнение 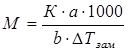 , выразим массу растворенного вещества: а =
, выразим массу растворенного вещества: а = 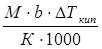 , а =
, а = 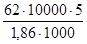 = 1666,6 г.
= 1666,6 г.
б) Используя уравнение 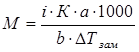 , выразим массу растворенного вещества: а =
, выразим массу растворенного вещества: а = 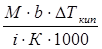 , i = α (β -1) + 1 = 1 ∙ (3 – 1) + 1 = 3
, i = α (β -1) + 1 = 1 ∙ (3 – 1) + 1 = 3
а =  = 994,6 г.
= 994,6 г.
Дата публикования: 2014-11-18; Прочитано: 2137 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
