 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Температура замерзания и кипения растворов
|
|
Вследствие понижения давления насыщенного пара над раствором по сравнению с чистым растворителем понижается температура замерзания и повышается температура кипения растворов по отношению к растворителю.
Зависимость понижения температуры замерзания ∆Тзам = Тзам. р-ля – Тзам. р-ра, и повышения температуры кипения ∆Ткип = Ткип. р-ра – Ткип. р-ля от концентрации выражается уравнениями:
∆Тзам = К ∙ с, (3.2)
∆Ткип = Е ∙ с, (3.3)
где К – криоскопическая константа растворителя;
Е – эбуллиоскопическая константа растворителя;
с – моляльная концентрация (число молей растворенного вещества в 1000 г растворителя).
Криоскопическая и эбуллиоскопическая константы определяются только природой растворителя и могут быть рассчитаны по следующим уравнениям:
 , (3.4)
, (3.4)
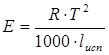 , (3.5.)
, (3.5.)
где lпл – удельная теплота плавления растворителя;
lисп – удельная теплота испарения растворителя.
Свойство растворов понижать температуру замерзания и повышать температуру плавления по сравнению с чистым растворителем используется для определения молекулярной массы М растворенных веществ:
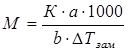 , (3.6)
, (3.6)
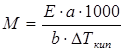 , (3.7)
, (3.7)
где а – масса растворенного вещества, г;
b – масса растворителя, г.
Дата публикования: 2014-11-18; Прочитано: 547 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
