 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Интегрирование уравнения Клаузиуса - Клапейрона и его анализ
|
|
Интегрирование уравнения Клапейрона-Клаузиуса 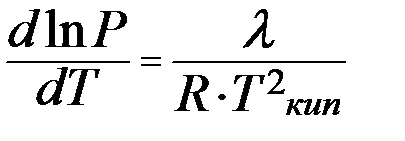 в пределах температур Т1 и Т2, которым соответствуют давления P1 иP2при l = const, дает:
в пределах температур Т1 и Т2, которым соответствуют давления P1 иP2при l = const, дает:
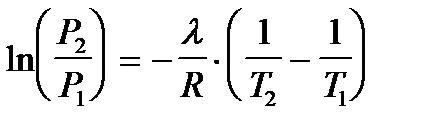 ,
,
После преобразования последнего получают аналитическую форму уравнения Клапейрона-Клаузиуса:
 .
.
Полученное выражение даёт возможность определить:
- неизвестное давление по известным температурам, другому давлению и
теплоте кипения и известному давлению:  ;
;
- неизвестное температуру кипения, по известным давлениям, теплоте кипения и другой температуре: 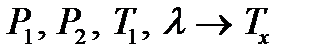 ;
;
- теплоту кипения, если известны при двух давлениях насыщенного пара температуры кипения 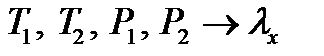 :
:
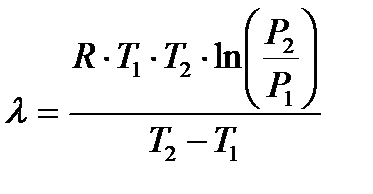
| lnрP |
| lnP2 |
| lnP1 |

|
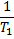
|

|
Неопределённое интегрирование уравнения (5.9) с учётом того, что теплота кипения не зависит от температуры даст уравнение:
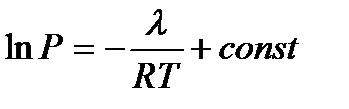 или
или 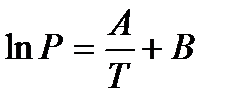 .
.
Выражения представляют уравнения прямой линии с угловым коэффициентом А в координатах 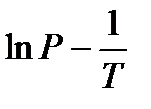 (рис.).
(рис.).
Рис. Зависимость давления насыщенного пара от температуры.
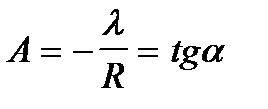
По тангенсу угла наклона прямой можно определить теплоту испарения:
lграф = - Rtga.
Чем больше угол a, тем больше теплота испарения, и следовательно, тем быстрее испаряется жидкость. Тангенс угла 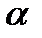 находят из соотношения:
находят из соотношения:
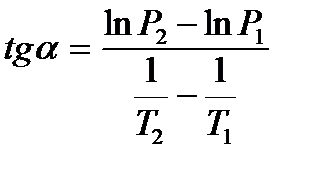 .
.
Определив теплоту кипения вещества аналитически и графически, можно рассчитать приращение энтропии в процессе кипения:
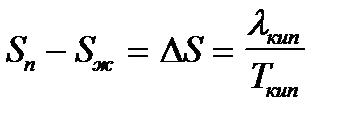 .
.
Химическое равновесие. Классификация равновесных состояний. Признаки равновесных состояний. Закон действующих масс. Вывод константы равновесия для гомогенной реакции. Связь между различными формами выражения констант равновесия.
Дата публикования: 2014-11-18; Прочитано: 2864 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
