 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Вывод дифференциальной формы уравнения Клаузиуса - Клапейрона для процесса кипения
|
|
Рассмотрим процесс фазового превращения на примере кипения жидкости.
Испарение - это фазовый переход на границе раздела жидкость пар или жидкости.
Кипение - это процесс, когда парообразование происходит не только с поверхности но внутри жидкости путём образования пузырьков пара жидкости и их выделения. При этом давление в пузырьках пара, находящихся в равновесии с жидкостью, равно давлению пара над жидкостью.
Температура кипения - это температура, при которой давление насыщенного пара жидкости равно внешнему давлению:
Рнасыщ. пара = Рвнеш.
Нормальной называется температура кипения жидкости, измеренная при нормальном давлении.
Уравнение Клапейрона-Клаузиуса (5.2.) можно преобразовать, приняв следующие приближения:
1. Поскольку Vп >> Vж (например для воды мольный объем в парообразном состоянии при нормальных условиях равен V п =22400 см3, а в жидком состоянии Vж = 18 см3), то в уравнении 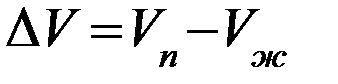 можно пренебречь величиной
можно пренебречь величиной 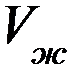 и принять, что
и принять, что 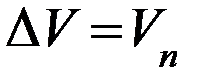 ;
;
2. При невысоких давлениях и температурах (вдали от критических) можно применять уравнение состояния идеального газа (уравнение Клапейрона-Менделеева) и к реальным системам. Тогда
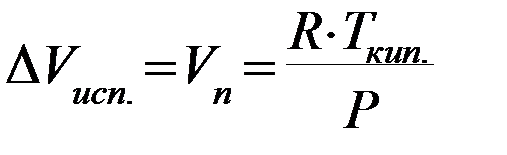 ,
,
где R - универсальная газовая постоянная.
Подставив уравнение 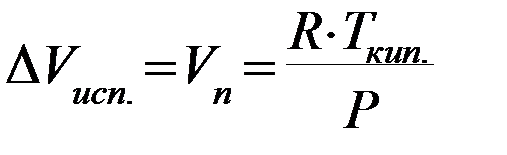 в уравнение К-К
в уравнение К-К 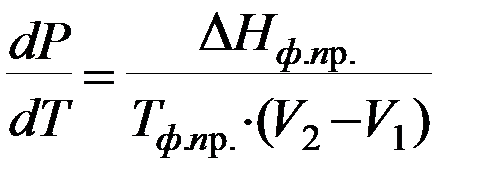 , получим:
, получим:
 .
.
Это уравнение после преобразования: 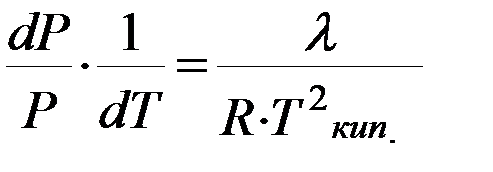
принимает вид: 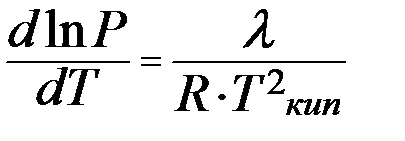 .
.
Теплота испарения l зависит от температуры: c повышением температуры она понижается, а с понижением - повышается; при критической температуре теплота испарения равна нулю.
При температурах, далёких от критической, изменения теплоты испарениямалы и поэтому в небольшом интервале температур, теплоту испарения можно считать величиной постоянной: l = const.
Дата публикования: 2014-11-18; Прочитано: 1976 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
