 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Основные соотношения между термодинамическими функциями. Уравнение Гиббса-Гельмгольца
|
|
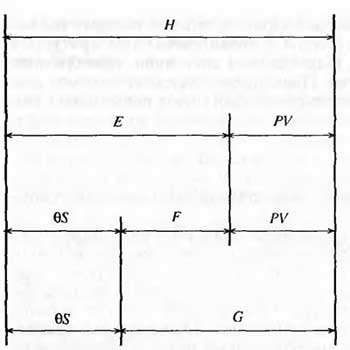 Соответствующие дифференциалы термодинамических потенциалов:
Соответствующие дифференциалы термодинамических потенциалов:
· для внутренней энергии
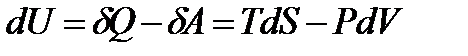 ,
,
· для энтальпии
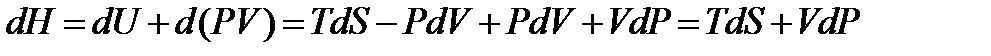
· для свободной энергии Гельмгольца
 ,
,
· для потенциала Гиббса
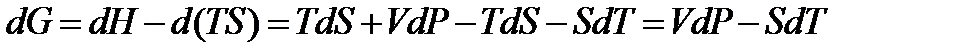
Изохорно-изотермический потенциал. Функции внутренняя энергия U и энтальпия Н редко применяются в химической термодинамике, т.к. условия при которых они характеризуют процесс (V = const, S = const и р = const, S = const) практически неосуществимы. Наибольшее значение имеют характеристические функции: свободная энергия Гельмгольца
F = U - T·S - изохорно-изотермический потенциал и свободная энергия Гиббса
G = H - T·S - изобарно-изотермический потенциал.
Для вывода этих функций воспользуемся обобщенным уравнением I и II законов термодинамики
 ;
;
 ;
;
 ;
;
 .
.
Величину U – T ·S обозначим через  , т. е. F=U – T· S. Тогда
, т. е. F=U – T· S. Тогда  . Так как F = f (Т,V) выражается через U и S, то дифференциал её будет полным, т. е.
. Так как F = f (Т,V) выражается через U и S, то дифференциал её будет полным, т. е.
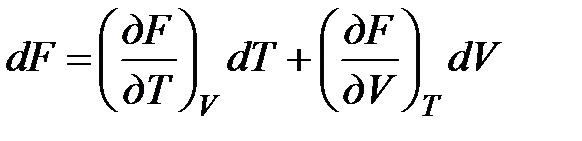 .
.
Сравнивая это уравнение с уравнением (2.39), получим:
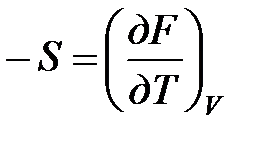 и
и 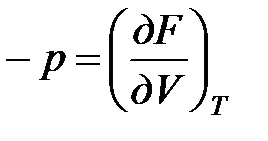 .
.
Как видно, функция F = U - TS, называемая изохорно-изотермическим потенциалом, также является характеристической.
Изобарно-изотермический потенциал обычно обозначается через G (иногда через Z). Она имеет вид:
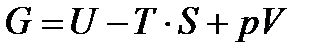 Или
Или 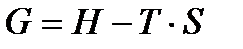 , причем G=f(T, р).
, причем G=f(T, р).
Уравнение 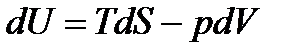 и переписываем его в виде:
и переписываем его в виде:  .
.
К правой и левой частям этого уравнения прибавляем – SdT + Vdp:
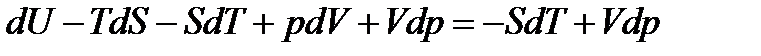 .
.
В результате  . Выражение в скобках есть G=f(T, р), откуда
. Выражение в скобках есть G=f(T, р), откуда
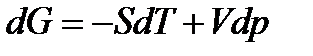 .
.
Полный дифференциал G=f(T, р) будет
 .
.
Из сравнения этого уравнения с уравнением (2.42) следует, что
 ;
; 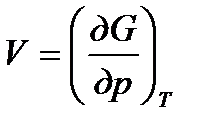 .
.
Функция 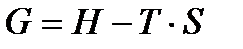 называется изобарно-изотермическим потенциалом. Как и все предыдущие функции, она является функцией состояния, т.е. изменение ее ΔG = G2 - G1 не зависит от пути процесса. Из четырех функций U=f·(V,S), H= f·(p,S), F= f·(T,V) и G= f·(T,p) в термодинамических расчетах наиболее часто используются функции F и G, так как они вычисляются по легко измеряемым параметрам (Т, V, p).
называется изобарно-изотермическим потенциалом. Как и все предыдущие функции, она является функцией состояния, т.е. изменение ее ΔG = G2 - G1 не зависит от пути процесса. Из четырех функций U=f·(V,S), H= f·(p,S), F= f·(T,V) и G= f·(T,p) в термодинамических расчетах наиболее часто используются функции F и G, так как они вычисляются по легко измеряемым параметрам (Т, V, p).
Дата публикования: 2014-11-18; Прочитано: 990 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
