 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Онкогенные вирусы
|
|
Основной особенностью онкогенных вирусов является их способность трансформировать нормальную клетку в опухолевую, которая дает начало доброкачественной или злокачественной опухоли.
Онкогенные ДНК-содержащие вирусы.
Папилломавирусы. Вирусы папилломы кожи и слизистых оболочек кроликов (вирус Шоупа), хомяков, сусликов, кошек, собак, овец, коз, оленей, крупного рогатого скота, лошадей, обезьян и бородавок у человека.
Икосаэдрического типа вирус папилломы диаметром около 55 нм, Его оболочка состоит из 72 капсомеров.
Полиомавирусы включают вирусы полиомы мышей, вакуолизирующий вирус обезьян (SV-40) и SV-40 - подобные вирусы человека. Диаметр капсида 40 нм, Оболочка содержит 72 капсомера.
Вирус полиомы вызывает множественные опухоли при введении мышам, а также другим видам млекопитающих.
Аденовирусы. Из 31 типа аденовирусов онкогенными являются 13 типов аденовирусов человека, 6 типов аденовирусов обезьян, 1 тип аденовирусов крупного рогатого скота, 1 тип аденовирусов собак и 2 типа аденовирусов птиц. Эти вирусы вызывают опухоли у крыс, мышей, хомяков.
Герпесвирусы. Вызывают лимфоидные и эпителиоидные опухоли у различных видов животных: аденокарциномы почек лягушек, лимфомы обезьян, лимфоматоз кур. Герпесвирус Эпштейн-Барр является возбудителем инфекционного мононуклеоза человека и, возможно, лимфомы африканских детей (лимфомы Беркитта), а также рака шейки матки человека. Онкогенные свойства вируса Эпштейн-Барр были подтверждены в опытах заражения этим вирусом обезьян (мармозетов), у которых возникли злокачественные лимфомы. Вирусы простого герпеса 1 и 2, а также вирус цитомегалии способны in vitro вызывать трансформацию нормальных клеток животных и человека. У женщин с карциномой шейки матки в крови выявляют антитела к герпесвирусу 11 типа, а в опухолевых клетках обнаруживают специфические вирусные антигены.
Вирусы группы оспы индуцируют у различных животных (кролики, зайцы, белки) доброкачественные, спонтанно регрессирующие соединительнотканные опухоли. Входящий в эту группу вирус контагиозного моллюска вызывает у человека образование плотных шаровидных узелков на половых органах, в области лобка, живота, на лице, шее и др., достигают небольших размеров и затем регрессируют.
Онкогенные РНК-содержащие вирусы (ретровирусы) входят в состав семейства Retroviridae, т.е. вирусов, содержащих обратную транскриптазу - reverse transcriptase. В зависимости от характера нуклеотида, структуры вирионов и других признаков онковирусы делятся на четыре группы - A, B, C, D.
Онковирусы всех групп имеют ряд общих свойств. Геном их представлен однонитчатой РНК, состоящей из двух идентичных нитей с молекулярной массой 2,5-5 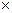 106 каждая, связанных с обратной транскриптазой. В инфицированной клетке обратная транскриптаза (ревертаза), являющаяся РНК-зависимой ДНК-полимеразой образует ДНК-копию вирусного генома, встраивающуюся в хромосому клетки-хозяина. С этого момента интегрированный вирусный геном подчиняется клеточным механизмам регуляции.
106 каждая, связанных с обратной транскриптазой. В инфицированной клетке обратная транскриптаза (ревертаза), являющаяся РНК-зависимой ДНК-полимеразой образует ДНК-копию вирусного генома, встраивающуюся в хромосому клетки-хозяина. С этого момента интегрированный вирусный геном подчиняется клеточным механизмам регуляции.
Вирионы имеют сферическую форму, сложное строение. Внутренний нуклеокапсид покрыт суперкапсидной оболочкой, состоящей из двойного слоя липидов и внешних белков-гликопротеинов, формирующих выступающие булавовидные шипы с утолщениями на концах.
Онковирусы группы С являются возбудителями лейкозов и сарком у птиц и многих видов млекопитающих (мыши, кошки, обезьяны, крупный рогатый скот).
Возбудители Т-клеточных лейкозов человека близки по физико-химическим свойствам и особенностям репродукции к вирусам подсеиейства Oncovirinae, роду Oncovirus, типа С. Хотя присутствие в геноме вирусов Т-клеточных лейкозов трансактивирующего гена, схожим с одним из трансактивирующих генов вирусов подсемейства Lentivirinae (в том числе ВИЧ), дает основания для выделения их в самостоятельную таксономическую единицу, занимающую промежуточное место между подсемействами Oncovirinae и Lentivirinae. Ныне известны два возбудителя Т-клеточных лейкозов человека: HTLV-1 и HTLV-2 (от англ. Human T-Lymphotropic Virus), различающихся по антигенным свойствам. Геном этих вирусов картирован. ДНК провируса имеет такую структуру: 5¢ - LTR - gag - pol - env - tat - LTR - 3¢. Гены gag, pol и env кодируют белки-предшественники, нарезающиеся вирусспецифической протеазой на структурные белки вируса, в том числе и обратную транскриптазу. Ген tat является трансрегулирующим геном. Его продукт - белок - с одной стороны в десятки раз ускоряет експрессию генома вируса, активируя его промотор, а с другой - инактивирует иной ген (возможно - гены), в том числе ген интерлейкина-2 в геноме клетки-хозяина.
Пути заражения - трансфузионный, парентеральный, половой, от матери к ребенку (трансплацентарно, во время родов или вскармливания грудным молоком). Риск заражения зависит от механизма заражения и варьирует в границах 25-80%.
Инкубационный период от нескольких месяцев до десятков лет.
Эндемичными районами распространения являются зоны Карибского моря, Центральной Африки, Юго-Западные острова Японии (в Японии пораженность населения составляет от 1,5 до 5%.
Методов специфической профилактики и терапии не существует.
Лабораторная диагностика Т-клеточного лейкоза осуществляется методом ИФА в непрямом варианте. Объектом первичного исследования является сыворотка крови, в которой выявляют антитела к вирусу. Положительный в ИФА результат подтверждается методом иммуноблота. Нечеткие результаты иммуноблота выявляют с помощью метода радиоиммунопреципитации.
К онковирусам группы С относится и вирус саркомы кур Рауса. Выделенный в 1911 году вирус способен вызывать развитие опухолей не только у кур, но у фазанов, уток, голубей, змей, черепах, а также у млекопитающих - мышей, крыс, хомяков, собак и обезьян.
Под влиянием индуцирующих факторов (облучение животных, действие химических веществ и др.) были выделены различные вирусы лейкозов и сарком у мышей.
Онковирусы группы В были обнаружены в 1936 г. Дж. Биттнером в молоке мышей высокораковой линии. При вскармливании таким молоком мышей низкораковой линии у них возникали опухоли молочных желез.
Онковирусы группы А обнаруживаются, как правило, в ассоциации с онковирусами групп С и В, однако не получены достоверные данные об их участии в канцерогенезе.
Онковирусы группы D выделены из опухолевых и нормальных тканей макак резусов, лангуров и саймири, а также из перевиваемых клеток человека и свиньи.
Теорию о связи вирусов с перерождением клеток в раковые впервые разработал советский ученый Л.А. Зильбер (1941-1944). В основе вирусгенетической теории лежит представление о интеграции вирусного и клеточного геномов. Экспериментально эта точка зрения была обоснована в 1968 г. американскими учеными Р. Далбекко с сотр.
В составе интегрированного в клеточную ДНК вирусного генома имеется ген (гены), получивший название “онкоген”. Предполагают, что онкогены опухолеродных вирусов - это регуляторные клеточные гены, случайно включившиеся в состав вирусного генома. В норме их работа регулируется нормальными клеточными механизмами. Эта регуляция нарушается, когда ген функционирует в составе вирусного генома.
В трансформированных клетках нарушен процесс передачи информации с поверхности на ядерный аппарат, увеличен синтез ДНК, наблюдаются хромосомные аберрации, теряется способность к контактному торможению, усиливается митотическая активность, что приводит к усиленному росту и размножению этих клеток.
ВИЧ-инфекция (инфекция вирусом иммунодефицита человека) - медленно прогрессирующее инфекционное заболевание, возникающее вследствие заражения вирусом иммунодефицита человека, порхающего иммунную систему, вследствие чего организм становится высоко восприимчив к оппортунистическим инфекциям и опухолям, которые в конечном итоге приводят к гибели больного.
Заболевание впервые было описано в 1981 г в США среди гомосексуалистов. Новая болезнь обычно манифестировалась пневмоцистной пневмонией и нередко саркомой Калоши, что было необычным, так как зги заболевания ранее встречались почти исключительно у истощенных больных преклонного возраста с тяжелой иммунодепрессией.
Первоначально состояние иммунной недостаточносги, возникающее у гомосексуалистов, пытались объяснить иммунодепрессивным действием спермы от большого числа партнеров или появлением у них в крови аутоантител к лимфоцитам, или, возможно, иммунодепрессивным действием нитритов, применяемых гомосексуалистами для снижения тонуса мышц заднего прохода. Однако вскоре эти предположения отпали, так как заболевание стали описывать не только у пассивных гомосексуалистов, но и у активных, у которых вышеперечисленные факторы не могли иметь место и, кроме того, все чаще состояние иммунодефицита стали описывать у наркоманов, не имеющих склонности к гомосексуализму.
Важным этапом в установлении инфекционной природы СПИД было выявление большого числа больных среди выходцев с острова Гаити африканского происхождения, у которых не отмечалось склонности к гомосексуализму или употреблению наркотиков и, кроме того, среди них количество заболевших мужчин и женщин было одинаковым, что противоречило американской статистике, согласно которой у жителей США, больных синдромом приобретенного иммунодефицита, число мужчин во много раз превышало число женщин.
Начиная с 1982 года случаи СПИД стали выявляться и среди жителей Западной Европы, первоначально почти исключительно у выходцев из Заира. Хотя среди заболевших по-прежнему преобладали лица с вредными привычками (гомосексуалисты, наркоманы), но все чаще заболевание стали описывать и у лиц, получавших массивные переливания донорской крови. Особенно много больных оказалось среди гемофиликов, получающих УШ и К-факторы свертывания крови, которые готовят из крови нескольких тысяч доноров. Почти одновременно случаи СПИД были описаны и у детей, при этом инфицирование могло произойти или с переливанием крови, или при парентеральных манипуляциях, а в ряде случаев можно было допустить только внутриутробную, так называемую вертикальную передачу вируса от матери к плоду.
Высказывается мнение, что заболевание возникло в начале 50-х годов в Центральной Африке и уже оттуда распространилось в страны Карибского региона, а затем в США и Западную Европу.
Допускается, что вирус СПИД человека произошел от родственных вирусов африканских обезьян, вызывающих у них спидоподобное заболевание. Возможность такой трансформации документируется экспериментальными исследованиями. Предполагается, что новый мутант находился в циркуляции среди коренного населения Центральной Африки, не получая дальнейшего распространения из-за относительной изоляции коренного населения, при этом он мог приобрести дополнительные патогенные свойства. В условиях урбанизации африканского континента, роста проституции, наркомании и пр появилась высокая возможность распространения вируса СПИД. Считается, что из Африки вирус попал на Гаити, а оттуда в США.
Официальное признание новой болезни произошло в 1983 году, а в 1986 году Международный комитет по таксономии вирусов предложил название ВИЧ (HIV) - вирус иммунодефицита человека (от англ. Human Immunodeficiency Virus). Вирус относится к семейству ретровирусов, подсемейству лентивирусов, то есть вирусов медленных инфекций. ВИЧ генетически и антигенно неоднороден - описаны ВИЧ-1 и ВИЧ-2. Родиной вирусов обоих типов считают Африку. ВИЧ-1 является возбудителем пандемии СПИДа, охватившей планету, а ВИЧ-2 встречается только в 15 странах Западной Африки и в некоторых странах Европы и Америки, куда он был завезен.
В 1986 году группой американских исследователей от здоровых людей в Сенегале был выделен вирус, сходный с вирусом африканских зеленых мартышек; сыворотки ВИЧ-инфицированных людей реагировали с антигенами вируса мартышек, но не давали реакции (или они были слабыми) с антигенами ВИЧ. Предполагалось, что вирус мог быть предшественником ВИЧ. Выделенный вирус был назван HTLV-4.
HTLV-4, подобно ВИЧ, инфицирует Т-хелперы, но не убивает их. Есть мнение, что непатогенный вирус HTLV-4 эволюционировал в безвредный вирус африканских зеленых мартышек, который превратился в патогенный ВИЧ-2 - предшественник ВИЧ-1.
Эпидемиология. ВИЧ-инфекция встречается на всех континентах и практически во всех странах, где ведется планомерный поиск больных. По оценке экспертов ВОЗ, во всем мире на 1 июля 1994 года официально зарегистрировано 985119 больных и 16 млн. инфицированных ВИЧ. Эти цифры следует считать приблизительными, поскольку число больных и инфицированных практически невозможно учесть и, кроме того, оно настолько быстро увеличивается, что любая опубликованная цифра, по справедливому замечанию американских авторов, сразу же становится устаревшей. Принято считать, что число больных и инфицированных во всем мире удваивается каждый год. Однако в последние годы, благодаря принятым мерам, увеличение числа больных и инфицированных существенно замедлилось.
Наибольшее число заболевших и инфицированных зарегистрировано в США. Общая пораженность ВИЧ по данным серологических исследований уже сейчас составляет около 100 на 100 тыс. населения, а по некоторым районам страны — 200 и более.
Заболеваемость в Западной Европе остается относительно низкой, однако уровень инфицированности быстро растет и уже по некоторым странам она составляет 20-30 на 100 000 населения.
Заболеваемость и инфицированность в Африке оценить затруднительно. По предварительным данным, нарастание числа случаев СПИД на африканском континенте происходит быстрее, чем в США, чему способствует низкий санитарный уровень, сопутствующие венерические заболевания, ритуальные обряды и др. В отдельных афри-канских странах (Заир, Кения, Замбия) носительство вируса среди взрослого населения достигло 20%, а заболеваемость уже сейчас составляет по некоторым городам 1 на 1000 населения. По пессимистическим прогнозам, число инфицированных в некоторых странах Африки в ближайшие годы может составить 50% и более. Ожидается также, что в максимально пораженных городах до 50% женщин детородного возраста заболеют СПИД и что у 5% детей на протяжении 2 лет после рождения обнаружатся признаки заболевания. Более тяжелый прогноз предполагает 70%-ный уровень инфицированности в последующие 10 лет с возможностью развития СПИД у каждого 4-го родившегося ребенка.
Не менее пессимистические прогнозы высказываются и для Латинской Америки Заболеваемость СПИД в Бразилии на февраль 1994 года составила 49312 случаев. Число инфицированных по некоторым странам Южной Америки приближается к уровню инфицированности в США.
Наименьшая заболеваемость и инфицированность регистрируется на азиатском континенте, что можно считать временным явлением, так как вирус еще не распространился среди коренного населения и практически все случаи болезни выявляются среди приезжих и лиц, контактирующих с иностранцами.
Заражение человека ВИЧ происходит при попадании вируссодержащего материала непосредственно в кровь или на слизистые оболочки. Велика вероятность заражения половым путем и при би- и гетеросексуальных контактах с больными (носителями), причем инфицирование женщин от мужчин чаще, чем мужчин от женщин. ВИЧ передается также через инфицированную кровь (при переливании крови и ее препаратов), при повторном использовании инфицированного медицинского инструментария, Чаще всего это происходит у наркоманов при внутривенном введении наркотических препаратов одними и теми же шприцами и иглами. Менее значимым является вертикальный путь передачи возбудителя, который реализуется в организме беременной женщины, когда плод заражается в матке (трансплацентарный путь). Риск передачи ВИЧ детям от серопозитивных матерей составляет до 50%, зависит от стадии заболевания и увеличивается при грудном вскармливании. Возможно контактное заражение ребенка при родах, а также через грудное молоко. Выявлены случаи заражения матерей от инфицированных грудных детей при вскармливании грудью. Поскольку ВИЧ находят также в слюне и моче и эти биологические жидкости могут при поцелуях и укусах попасть на слизистые оболочки здорового, нельзя исключить также вероятность заражения с помощью этих факторов передачи. Известен уникальный случай заражения ВИЧ пожилой женщины, инфицированной слюной при поцелуях со своим мужем, инфицированным ВИЧ.
Резистентность. ВИЧ нестоек во внешней среде и при кипячении инактивируется за 1 минуту, погибает под воздействием химических агентов, допущенных для проведения дезинфекции.
Морфология. Вирион ВИЧ - сферическая частица диаметром около 100 - 120 нм, состоящая из сердцевины и оболочки (рис. 7). Зовнішня гліколіпідна оболонка віріона двошарова. Зовні віріон має виступа діаметром 15 і довжиною 9 нм (їх виявлено 72), утворені білковими субодиницями – глікопротеїнами. Структурований глікопротеїн (попередник) gp має молекулярну масу 160 (gp 160). Він, у свою чергу, складається з надмембранної (gp 120) і трансмембранної (gp 41) частин. Білок gp 41є глікозованим протеїном, що пронизує двошарову гліколіпідну оболонку віріона. До його складу входять внутрішньовіріонна, власне трансмембранна ділянка, та невелика позавіріонна, з якою молекула gp120 з’єднується двома дісульфідними зв’язками. У складі цих глікопротеїнів є білки, що “пізнають” клітинні рецептори CD4 (білки gp120) та забезпечують проникнення вірусу в клітину-хазяїна (білки gp 41). Поверхневі білки gp160 відрізняються від поверхневих білків інших представників родини ретровірусів високою мінливістю амінокислотних залишків і великими розмірами. Процес нарізання білка – попередника gp160 здійснюється клітинною протеазою в апараті Гольджі у вакуолях з кислим рН.
|
Рис. 7. Структура ВИЧ (схема): 1 - gp120; 2 - gp-41; 3 - липидная двухслойная мембрана; 4 - р-17/18; 5 - p-24/25; 6 - сердцевина; 7 - обратная транскриптаза; 8 - р-7, р-9; 9 - РНК.
Зсередині до глікопротеїнової оболонки щильно прилягає щар так званого матриксного білка, м.м. якого становить 17kD (p17). Товщина шару в межах 5- 7 нм.білки виступів (через gp41) зв’язані з білками матриксу (р17). Центральна, або серцевинна частина віріона (англ. core) має вигляд конусоподібногого “кошика”, побудованого з вірусного білка, м.м. якого становить 24kD (р24). В середині “кошика” є дві крпії однонитчастої РНК, що вкриті білками з м.м. 9 (р9) і 7kD (p7). У серцевині віріона знаходяться білки-ферменти: р66 – зворотна транскриптаза, р34 – ендонуклеаза та р9 – протеаза.
У складі віріона завжди виявляються клітинні антигени комплексу гістосумісності І та ІІ класу.
Геном ВИЧ, представленный двумя копиями одноцепочечной РНК, из 9200 нуклеотидов содержит 9 генов, в том числе три основных (структурных) - gag, env и pol (рис. 8). Прочие гены являются неструктурными, регуляторные функции и способствуют дозреванию вируса и выходу его из инфицированной клетки. С обоих концов полинуклеотидной цепи расположены т.н. длинные концевые повторы - LTR (Long Terminal Repeat). Они не кодируют вирусные белки, но регулируют скорость синтеза ДНК на матрице вирусной РНК и процесс интеграции вновь образованной ДНК в геном клетки-хозяина.
Rev
Дата публикования: 2014-11-19; Прочитано: 1749 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
