 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Время наступления основных этапов инфекции ЦМВ и ВПГ
|
|
Сравнительные данные, полученные при помощи
электронной микроскопии
(по Б. Мейхи, 1988)
| Этапы | Начало события | |
| ЦМВ (дни) | ВПГ (часы) | |
| Слияние клеток и округление | 0,5 | |
| Изменения аппарата Гольджи | ||
| Скрытый период (эклипс-период) | ||
| Появлениебоьшого количества гранул | ||
| Конденсация хроматина | Не наблюдается | |
| Сборка в ядрах первых капсидов | ||
| «Одевание» вирусов ядерной мембраной | 3,5 | :6 |
| «Одевание» вирусов цитоплазматической мембраной | ||
| Лизис клетки | 7 - 8 | 24 - 48 |
В генезе формирования хронических форм инфекции большое значение, по-видимому, имеет способность цитомегаловируса длительно персистировать и репродуцироваться в лейкоцитах, системе мононуклеарных фагоцитов и лимфоидных органах. Надо полагать, что при развитии в организме состояния иммунодепрессии вирус может выходить в жидкую среду и поражать многие органы.
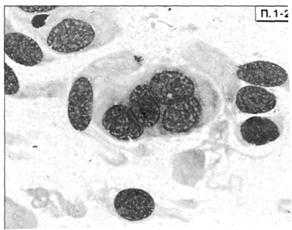
Патоморфологня. Основным морфологическим признаком цитомегалии является образование гигантских клеток с внутриядерными включениями. Эти клетки имеют характерную структуру и не встречаются при других заболеваниях Их ядро расположено эксцентрично, а в центре обнаруживаются ацидофильные включения диаметром 8-20 нм, окруженные светлой зоной, в результате чего клетка приобретает характерный вид, напоминающий совиный глаз. При локализованной форме изменения определяются почти исключительно в слюнных железах, преимущественно околоушных, реже — подчелюстных и очень редко — в подъязычных. Формирование цитомегалических клеток (цитомегалов) отмечается в эпителии слюнных трубок и выводных протоков. В окружающей строме обнаруживаются клеточные лимфогистиоплазма-тические инфильтраты. При генерализованной форме цитомегалическому метаморфозу подвергаются клетки эпителия практически всех органов и систем в легком — бронхи, бронхиолы, альвеолоциты и бронхиальные железы; в почках — извитые канальцы и капсулы клубочков; в печени — желчные протоки; в кишечнике — кишечные железы, ворсинки и т. д. Следствием этого является формирование очаговой или интерстициальной пневмонии, подострого холестатического гепатита, очагового нефрита, катарального или язвенного энтероколита и др. Возможно формирование пороков развития кишечника и других висцеральных органов. При поражении мозга развиваются очаговые некрозы и кальцификаты.
Клиническая картина. Инкубационный период точно не установлен. По-видимому, он колеблется от 15 дней до 3 мес
Различают врожденную и приобретенную цитомегалию. Врожденная цитомегалия часто протекает как генерализованная форма с поражением многих органов и систем. Приобретенная цитомегалия у детей раннего возраста протекает по типу мононуклеозоподобного синдрома, иногда с преимущественным поражением легких, желудочно-кишечного тракта, печени или как генерализованная форма Как врожденная, так и приобретенная цитомегалия может протекать бессимптомно. Принято считать, что число манифестных и бессимптомных форм выражается как 1 10 Кроме того, по течению различают острую и хроническую цитомегалию.
Врожденная цитомегалия. Инфицирование плода происходит от матери, страдающей локализованной (латентной) формой или острой формой цитомегаловирусной инфекции. Вирус гематогенным путем попадает в плаценту и вызывает ее поражение, а затем проникает в кровь и слюнные после рождения от матери или обслуживающего персонала в случае, если они являются носителями вируса.. Заражение возможно при переливании плазмы и крови от доноров-носителей цитомега-ловируса.. Течение болезни часто бывает длительным Ежедневные повышения температуры тела до 39-40°С, часто сопровождаются ознобами, продолжаются 2-4 и более недель.
Диагноз, как правило, вызывает большие затруднения Последовательно такие больные обследуются на сепсис, токсоплаз-моз, иерсиниоз, брюшной тиф и др. В периферической крови у них часто обнаруживаются лимфоцитоз и нередко выявляются атипичные мононуклеары, что формально может дать основание для диагностики инфекционного мононуклеоза.. Цитомегаловирусный мононуклеозоподобный синдром часто возникает через 5-6 недель после переливания крови или ее компонентов (возбудитель в этих случаях персистирует в клетках белой крови донора).
При генерализованной форме приобретенной цитомегалии в процесс последовательно вовлекаются многие органы и системы. Заболевание характеризуется высокой продолжительной лихорадкой, общеинфекционным токсикозом, поражением легких (интерстициальная пневмония), желудочно-кишечного тракта (повторная рвота, понос), сердечно-сосудистой системы, явлениями паренхиматозного гепатита (слабая истеричность, увеличение конъюгированного и неконъюгиро-ванного билирубина, повышение активности пе-ченочноклеточных ферментов и др.) и энцефалита (судорожная готовность, тремор, нистагм, симптомы орального автоматизма и др.). Течение болезни длительное. Прижизненная диагностика затруднена. Исследование мочи и слюны на цитомегалы нечасто дает положительный результа.т В таких случаях предполагают сепсис. В связи с чем больные получают интенсивную антибактериальную терапию без заметного эффекта. Для диагностики может иметь значение обнаружение у больного лимфоцитоза, а не нейгрофилеза, как это свойственно бактериальному сепсису. СОЭ часто бывает нормальной или умеренно ускоренной. Решающее значение для диагноза имеет выявление у больных в сыворотке крови специфических антител класса 1gM к цитомегаловирусу (анти-ЦМВ 1gМ).
 Диагностика. Поставить диагноз цитомегало-вирусной инфекции на основании только клинических данных не представляется возможным. Лабораторная диагностика основана на цитологических, вирусологических и серологических исследованиях У больных цитомегалией пораженные вирусом клетки (цитомегалы) легко десквамиру-ются в просвет протоков пораженных железистых органов и могут легко быть обнаружены в осадках мочи, слюны, спинномозговой жидкости, мокроте, промывных водах желудка и других секретах и экскретах, что следует считать надежным и доступным методом прижизненной диагностики как врожденной, так и приобретенной цитомегалии. Для повышения надежности метода рекомендуется многократно повторять исследование.
Диагностика. Поставить диагноз цитомегало-вирусной инфекции на основании только клинических данных не представляется возможным. Лабораторная диагностика основана на цитологических, вирусологических и серологических исследованиях У больных цитомегалией пораженные вирусом клетки (цитомегалы) легко десквамиру-ются в просвет протоков пораженных железистых органов и могут легко быть обнаружены в осадках мочи, слюны, спинномозговой жидкости, мокроте, промывных водах желудка и других секретах и экскретах, что следует считать надежным и доступным методом прижизненной диагностики как врожденной, так и приобретенной цитомегалии. Для повышения надежности метода рекомендуется многократно повторять исследование.
Для выделения цитомегаловируса используется первичная эмбриональная культура фибробластов человека или линия диплоидных клеток легких эмбриона человека, а также обнаружение вирусной ДHК цепной полимеразной реакцией. Однако эти методы доступны не многим лабораториям.
Для серологического подтверждения диагноза используют РСК, РН, РПГА, реакцию агрегации тромбоцитов и др. Но в настоящее время все большее практи- ческое значение приобретает метод ИФА, позволяющий раздельно определять специфические антитела класса 1gМ и 1gG. Обнаружение в сыворотке крови антител к вирусу цитомегалии класса 1gМ (анти-ЦМВ 1gМ) является надежным и ранним признаком активно протекающей (острой или хронической) щггомегаловирусной инфекции. Определенное диагностическое значение может иметь и быстрое нарастание титра анти-ЦМВ класса 1gG.
Прогноз. При врожденной цитомегалии прогноз часто неблагоприятный. Заболевание может закончиться летально, а при выживании возможны нарушения функции ЦНС в виде снижения интеллекта, глухоты, центральных параличей, микроцефалии, гипо- и гиперкинезии, олигофрении и др (до 90%) Даже у детей с бессимптомно протекающей врожденной цитомегалией возможно снижение интеллекта: они могут отставать в школе, жаловаться на быструю утомляемость, бессонницу, головные боли и т.д.
Приобретенная цитомегаловирусная инфекция, протекающая по типу мононуклеоза, в большинстве случаев заканчивается выздоровлением, при генерализованной форме возможен летальный исход, особенно в тех случаях когда в процесс последовательно вовлекаются легкие, печень, центральная нервная система.
Лечение. Применяют комплекс лекарственных средств в зависимости от поражаемого органа (пневмония, гепатит, желудочно-кишечный тракт и др). При генерализованной цитомегалии показано применение кортикостероидных гормонов, применение интерферона или реаферона, введение витаминов С, К, Р, группы В/ Антибиотики назначают при наслоении бактериальной инфекции и возникновении осложнений. В связи с иммунодепрессивным действием вируса рекомендуют иммуностимуляторы (декарис, нуклеинат натрия, тактивин и др.).
Результаты лечения противовирусными препаратами (ацикловир, аденин арабинозид, виразол и др.) оказались мало эффективными. Обнадеживающий эффект получен при назначении ганцикловира.
Для активной профилактики предложены живые и убитые вакцины. Однако они не получили практического применения.
ЭПШТЕЙН-БАРР ВИРУСНАЯ ИНФЕКЦИЯ
(ИНФЕКЦИОННЫЙ МОНОНУКЛЕОЗ)
Инфекционньй мононуклеоз— острое инфекционное заболевание, вызываемое вирусом Эпштейн-Барр из семейства Herpesviridae, характеризующееся лихорадочным состоянием, ангиной, увеличением лимфатических узлов, печени и селезенки, появлением атипичных мононуклеаров в периферической крови и гетерофильных антител.
Первоначально вирус был выделен из клеток злокачественной лимфомы Беркитга (Вигйй). Вскоре стало очевидным, что этот вирус вызывает инфекционный мононуклеоз, лимфому Беркитта и назофарингеальную карциному.
Лимфома Беркитта — злокачественное заболевание лимфоидной ткани, локализующееся, главным образом, вне лимфатических узлов — в верхней челюсти, почках, яичниках. Заболевание наблюдается преимущественно у детей в отдельных странах Африки и Азии.
Назофарингеальная карцинома — злокачественное опухолевое заболевание носоглотки, которое встречается в основном среди мужского населения в Китае.
На сегодняшний день существует безусловное мнение, что ЭБВ, как и другие вирусы семейства герпеса (вирусы простого герпеса, цитомегаловирус), является одним из реальных кандидатов в опухолевые вирусы человека.
В клеточном геноме этих вирусов имеется информация, активация которой манифестируется как малигнизация. Эта информация обозначается термином "онкоген". Для большинства онкогенов идентифицированы их продукты — "онкобелки". Косвенным подтверждением онкогенности ЭБВ служит выявление р-последова-тельностей нуклеиновых кислот этого вируса в клетках опухолей, а также вирусспецифических антигенов и иммунного ответа на вирус у пациентов со злокачественными новообразованиями. При этом полагают, что ЭБВ может принимать участие либо как промотор эксперессии клеточных проонкогенов, либо как инициатор мутагенеза, либо как "коканцероген", действующий синергично с другими вирусами. В последние годы появилось большое количество сообщений об этиологической роли ЭБВ при многих злокачественных заболеваниях: "волосатой" лейкоплакии полости рта, ряде других лимфоидньк новообразований полости рта, карциноме околоушной железы, раке тимуса, эпителиальном раке печени, карциноме шейки матки. Считается, что во всех случаях ЭБВ играет свою роль совместно с другими факторами, вызывающими иммуносупрессию.
Этиология. ЭБВ относится к семейству герпесвирусов, содержит ДНК, имеет сферическую форму с диаметром частиц 180 нм. Вирус чувствителен к действию эфира, хорошо размножается в культуре клеток опухоли Беркитта, крови больных инфекционным мононуклеозом, лейкемических клетках и в культуре клеток мозга здорового человека Электронно-микроскопический и седиментационный анализ ДНК ЭБВ в нейтральных и щелочных растворах показал, что ДНК вируса представляет собой линейную двунитчатую молекулу ЭБВ содержит следующие специфические антигены- вирусный капсидный антиген (УСА), ядерный антиген (ЕВNА), ранний антиген (ЕА) и мембранный антиген (МА). Время появления и биологическая значимость указанных антигенов неодинаковы. Антиген вирусного капсида является поздним. Мембранный антиген представляет собой комплекс продуктов ранних и поздних генов. Ядерный антиген является ранним, так как во время литической фазы инфекции он предшествует синтезу вирусных частиц. Вирус-специфические антигены — чужеродные белки, индуцирующие специфический иммунный ответ у человека (антитела). Знание сроков появления разных антигенов и выявление антител к ним дают возможность сегодня диагностировать с достаточной достоверностью острую, латентную и хроническую ЭБВ-инфекцию. Обнаружение антител к ядерному и раннему поверхностному антигенам при отсутствии антител к поздним антигенам свидетельствует об острой инфекции. Выявление антител к капсидному антигену и позднему мембранному при отсутствии антител к ранним антигенам служат маркерами давнего инфицирования — латентной инфекции. Спектры антител, возникающих в ответ на антигены ЭБВ, существенно отличаются при разных заболеваниях, ассоциированных с этим вирусом. Так, у пациентов с инфекционным мононуклеозом появляются антитела, относящиеся к трем классам иммуноглобулинов и направленные к тем или иным вирусспецифическим белкам.
Было бы логично предположить, что вариабельность в проявлениях заболеваний, вызываемых ЭБВ находится в зависимости от антигенных различий штаммов вируса. Однако при проверке данная гипотеза подтверждения не получила. Оказалось, что не существует субтипов ЭБВ, специальных для определенной болезни или местности. При сравнении обнаружены минимальные различия среди штаммов ЭБВ, изолированных из некоторых географических ареалов и от разных больных.
Эпидемиология. Многочисленными исследователями установлено, что ЭБВ повсеместно распространен среди человеческой популяции, им поражено 80-100% населения земного шара. Первая встреча с вирусом зависит от социальных условий. В развивающихся странах и социально неблагополучных семьях большинство детей инфицируется к 3 годам, а все население — к совершеннолетию. В развитых странах в социально благополучных семьях встреча с ЭБВ может не произойти до юношеского возраста. В США примерно 50% лиц, поступающих в колледжи (в основном более обеспеченные), оказались не инфицированными ЭБВ.
Проводилось изучение инфицированности ЭБВ среди 586 здоровых лиц в Москве в возрасте от О до 98 лет. Оказалось, что у детей в возрасте до 2 лет антитела к капсидному антигену ЭБВ были обнаружены в 62,5%, в остальных возрастных группах показатели инфицированности колебались от 82% до 100%. Наиболее низкие титры антител обнаружены у детей первого полугодия жизни. Самые высокие титры антител (в 2-3 раза выше, чем во всех других возрастных группах) выявлены у лиц старше 55 лет.
Установлено, что инфицирование ЭБВ протекает по-разному в зависимости от возраста. Попадание ЭБВ в детский организм чаще всего не сопровождается какими-либо клиническими симптомами (бессимптомная инфекция) или протекает под маской ОРЗ (атипичная форма). Типичным клиническим проявлением острой ЭБВ-инфекции считается инфекционный мононуклеоз. У детей первых 3 лет жизни первичное попадание ЭБВ в организм проявляется нередко как ОРЗ с так называемым "мононуклеозоподобным синдромом".
Источником инфекции являются больные бессимптомными и манифестными (стертыми и типичными) формами болезни, а также вирусовыделители. Установлено, что 70-90% лиц, перенесших инфекционный мононуклеоз, периодически выделяют ЭБВ в орофарингеальном секрете. Из носоглоточных смывов вирус выделяется от 2-х до 16 месяцев после перенесенного заболевания. Высказывается мнение, что лица, леченные иммунодепресантами, могут выделять вирус в течение неопределенно долгого времени, даже при отсутствии острой фазы болезни.
Основной путь передачи возбудителя — воздушно-капельный, нередко заражение происходит посредством инфицированной слюны, в связи с чем инфекционный мононуклеоз был назван "болезнью поцелуев". Дети нередко заражаются через игрушки, загрязненные слюной больного ребенка или вирусоносителя. Возможны гемо-трансфузионный (с донорской кровью) и половой пути передачи ЭБВ. Передача инфекции через воду или пищевые продукты маловероятна, однако полностью исключить этот путь пока не представляется возможным. Описаны случаи вертикальной передачи ЭБВ от матери к плоду и высказано предположение, что ЭБВ, наряду с вирусами краснухи, цитомегаловирусом, токсоплазмами и др. агентами, является причиной врожденных аномалий.
Распространенности инфекции способствует скученность, пользование общей посудой, бельем, передача предметов изо рта в рот. Развитию инфекции содействуют факторы, вызывающие снижение общего и местного иммунитета.
Инфекционному мононуклеозу свойственны следующие эпидемиологические особенности:
- цикличность заболеваемости с длительностью эпидемических волн 6-7 лет;
- сезонность с выраженным весенним пиком и незначительным подъемом в октябре месяце;
- развитие эпидемического процесса в основном за счет стертых и бессимптомньк форм болезни;
- преимущественная поражаемость лиц мужского пола;
- наибольшая заболеваемость среди детей дошкольного возраста, организованных в детские коллективы.
Инфекционный мононуклеоз чаще встречается в виде спорадических случаев, однако, возможны эпидемические вспышки заболевания. Контагиозный индекс не установлен, но считается, что он невысок. Эпидемиологический процесс в очагах инфекционного мононуклеоза осуществляется в основном за счет атипичных (стертьк, бессимптомных) форм, которые при специальном обследовании выявляются у контактных в 40-45% случаев. Инкубационный период принято считать равным 15 дням, но есть данные, что он более продолжителен, может затягиваться до 2 мес.
Патогенез. До настоящего времени отсутствует единая концепция патогенеза инфекционного мононуклеоза. Доказано, что в основе патогенетических изменений при данном заболевании лежит лимфопролиферативный процесс, следствием которого является увеличение иммунокомпетентных органов и уровня субпопуляций лимфоцитов. Инфекция ЭБВ не только всеобщая, но и неизбежно хроническая. ЭБВ содержит двухспиральную ДНК, интегрирует ее в геном человеческих В-лимфоцитов. При остром инфекционном мононуклеозе от 0,001 до 0,01% всех циркулирующих В-лимфоцитов инфицированы вирусом. В следующие 12-16 недель количество таких В-лимфоцитов снижается до 0,00001%, но они не исчезают совсем, а персистируют неопределенно дол- го. Лицо, получившее ЭБВ, периодически выделяет его с орофарингеальньми секретами.
Помимо В-лимфоцитов, ЭБВ способен размножаться в эпителии ротоглотки, протоков слюнных желез и, по последним сведениям, в эпителии шейки матки. ЭБВ обладает свойством не убивать инфицированные лимфоциты, а делать их способными к неопределенно долгой культивации.
Пусковым механизмом этих изменений большинство авторов считает адсорбцию ЭБВ на В-лимфоцитах с участием С3-фракции комплемента Однако исследования последних лет показали, чго геном ядра ЭБВ содержит большой ассортимент мигогенов, гомологичных геному нормальных клеточных структур человека, что не исключает роль аутоиммунного процесса в механизме патогенетических изменений при инфекционном мононуклеозе.
Исходя из клинико-иммунологических сопоставлений патогенез инфекционного мононуклеоза можно представить следующим образом: входными воротами являются лимфоидные образования ротоглотки. Здесь происходит первичная репродукция и накопление вирусного материала и откуда вирус гематогенным (возможно и лимфогенным) путем попадает в другие органы и в первую очередь периферические лимфатические узлы, печень и селезенку. Патологический процесс во всех перечисленных органах начинается почти одновременно. В ротоглотке возникают воспалительные изменения, сопровождающиеся гиперемией и отеком слизистой оболочки, гиперплазией всех лимфоидных образований, приводящие к резкому увеличению небных и носоглоточных миндалин, а также всех лимфоидных скоплений на задней стенке глотки ("гранулезный" фарингит). Аналогичные изменения происходят во всех органах, содержащих лимфоидно-ретикулярную ткань, но особенно характерно системное поражение лимфатических узлов, а также печени и селезенки.
Понять интимный механизм происходящих событий позволяют новые данные, дающие основания рассматривать инфекционный мононуклеоз как заболевание иммунной системы. Показано, что вирус содержится и репродуцируется В-лимфоцитами. Под влиянием вируса В-лимфоциты пролиферируют и превращаются в крупные атипичные лимфоциты (мононуклеары). Теоретически этот процесс мог бы закончиться неудержимой трансформацией В-лимфоцитов в бластные клетки, однако в действительности этого не происходит. Дело в том, что в ответ на фиксацию вируса на поверхности В-лимфоцита активируются Т-клетки супрессоры, а также естественные киллеры и включаются механизмы ангигелозависимого К-клеточного цитолиза. Эти механизмы, с одной стороны, тормозят пролиферацию и дифференциацию В-лимфоцитов, а с другой — вызывают лизис инфицированных В-лимфоцитов, способствуя выходу вируса в свободную циркуляцию с последующей его элиминацией гуморальными специфическими антителами. Вследствие поликлональной активации В-лимфоцитов в остром периоде инфекционного мононуклеоза под действием вируса Эпштейна-Барра происходит повышение образования гетерофильных антител против различных антигенов, нарушается антителообразование, не происходит переключение синтеза 1gМ на 1gС, что влечет за собой повышение в периферической крови концентрации 1gМ.
В период реконвалесценции инфекционного мононуклеоза, образовавшиеся иммунные комплексы не удаляются из организма, чему способствует их состав (крупномолекулярный белок М) и низкий уровень нейтрофилов в периферической крови. При тяжелых формах патологический процесс может развиваться не только в лимфоретикулярных тканях, но возможно и поражение ЦНС, мышцы сердца, поджелудочной железы и др. Чаще эти изменения возникают в связи с лимфоидной инфильтрацией в эти органы, но не исключается и непосредственное вирусное поражение.
Иммунитет. После перенесенного заболевания остается стойкий иммунитет. Повторные случаи заболевания крайне редки. В системе иммунной защиты имеют значение как гуморальные антитела, так и клеточные факторы. Показано, что гуморальные антитела защищают В-лимфоциты от реинфекции или повторного заражения вирусом Эшптейна-Барра, а Т-клетки, благодаря памяти пожизненно сохраняют способность элиминировать В-лимфоциты в случае их нового заражения вирусом.
Диагноз. В типичных случаях диагноз не вызывает затруднений. Тем не менее, полиморфизм клинических проявлений и вовлечение в патологический процесс иммунной системы диктуют необходимость лабораторного подтверждения диагноза.
Методы выделения ЭБВ и его антигенов в практической работе не используются, но применяются в научных исследованиях. В основу серологической диагностики инфекционного мононуклеоза положено выявление в сыворотке крови больных гетерофильных антител по отношению к эритроцитам различных животных (эритроциты барана, быка, лошади и др.). Гетерофильные антитела при инфекционном мононуклеозе относятся к классу иммуноглобулинов М.
Реакцию агглютинации (РА) трипсинизированных бычьих эритроцитов сывороткой больного, обработанной экстрактом почек морской свинки, для диагностики инфекционного мононуклеоза предложил Р. Тотсвис (1960). Положительный результат этой реакции при инфекционном мононуклеозе отмечается в 90% случаев, при других заболеваниях — в 2-3%.
Высокий процент положительных результатов получают при постановке реакции Гоффа-Бауера, для которой используют формализированные эритроциты лошади (;% суспензию).
К перспективным методам лабораторной диагностики инфекционного мононуклеоза мы относим ИФА, позволяющий раздельно определить антитела класса 1gМ и 1gG к Эпштейн-Барр вирусному антигену.
Лечение. Специфического лечения при инфекционном мононуклеозе нет. Ацикловир, с успехом применяющийся при лечении некоторых герпетических инфекций, при инфекционном мононуклеозе неэффективен, хотя при других проявлениях ЭБВ инфекции ("волосатая лейкоплакия полости рта") оказывает положительное действие. Назначают симптоматическую и патогенетическую терапию в зависимости от формы болезни. При всех формах болезни как базисную терапию применяют жаропонижающие средства (бруфен сироп, "Детский Тайленол", "Детский Мотрин" и др.), десенсибилизирующие препараты, антисептики для купированная местного процесса, витаминотерапию, при функциональных изменениях со стороны печени — желчегонные средства. Антибактериальная терапия назначается при наличии выраженных наложений в ротоглотке, а также при возникновении осложнений. При выборе антибактериального препарата следует помнить, что ампициллин противопоказан при инфекционном мононуклеозе, так как в 70% случаев его назначение сопровождается тяжелыми аллергическими реакциями (сыпь, отек Квинке, токсико-аллергическое состояние). Имеются сообщения о высокой эффективности метронидазола (флагил, трихопол), снимающего интоксикацию и симптомы заболевания в течение одних суток.
В тяжелых случаях, когда имеет место резкое увеличение лимфаденоидной ткани носоглотки и ротоглотки, назначают кортикостероиды (преднизолон, дексаметазон) из расчета 2-2,5 мг/кг массы в сутки, коротким курсом (не более 5-7 дней).
НАТУРАЛЬНАЯ ОСПА
Вирус натуральной оспы принадлежит к семейству Poxviridae, подсемейству Chordopoxvirinae, роду Ortopoxvirus. К другим представителям этого рода принадлежит вирус осповакцины, вирус оспы мышей, кроликов, коров, грызунов, верблюдов, обезьян.
Морфология. Вирус натуральной оспы является ДНК-содержащим, имеет форму параллелепипеда с закругленными углами, размеры его - 250-300 нм. Сердцевина вируса хорошо различается в виде двояковогнутого диска, возле нее расположены овальные структуры - боковые тела. Эти структуры окружены внешней оболочкой.
Геном представлен двуспиральной линейной нефрагментированной молекулой ДНК массой около 132х 106 D. В состав вириона входят 30-33 структурных белка, три из них связаны с ДНК и образуют нуклеопротеид, более половины белков формируют сердцевину вириона, а остальные расположены в его внешней части и на поверхности. Гликопротеиды поксвирусов находятся на внешней поверхности сердцевины вириона, где они образуют слой так называемых трубочек.
Кроме структурных белков в составе вириона выявлено 10 ферментов, обеспечивающих различные стадии репродукции вируса. Однако масса генома поксвирусов настолько велика, что он может содержать информацию не менее чем о 80 белках-ферментах.
Внешняя оболочка вируса представлена липопротеидами, среди которых преобладают фосфолипиды, синтезированные вирусом в цитоплазме клетки. Поверхностные белки вируса организованы в ворсинки, с которыми связаны инфекционные свойства возбудителя.
Культивирование. Вирус натуральной оспы хорошо развивается в куриных эмбрионах, вызывая на хорион-аллантоисной оболочке белых, мелких, плотных точечных поражений. Вирус хорошо культивируется на первичных и перевиваемых клеточных культурах человека, обезьяны, овцы и других животных, проявляя выраженное цитопатическое действие в виде округления и увеличения клеток с последующим их отторжением от стекла.
Антигенная структура. У вируса натуральной оспы не обнаружено антигенных разновидностей или вариантов, он имеет общие антигены с вирусом вакцины. Вирус оспы имеет общие антигены с эритроцитами человека группы А и АВ.
Резистентность. Вирус устойчив к действию фенола, высыханию, в высушенных оспенных корочках и в 50% глицерине сохраняется месяцами, легко переносит низкую температуру. Вирус чувствителен к действию света, при температуре 100оС погибает моментально, при 60оС - в течение 1 часа 1% растворы хлорамина, лизола, фенола инактивируют вирус через 30 минут, а 1% раствор хлорной извести - через 1 час.
Эпидемиология и патогенез у человека. Источник болезни - больной человек. Заражение происходит воздушно-капельным и воздушно-пылевым путем, а также посредством контакта с заразным материалом. Были зарегистрированы случаи оспы у людей, инфицированных вирусом обезьяньей оспы.
Репродукция вируса начинается через 1-1,5 часа после заражения. Цикл репродукции вируса завершается за 6-7 часов. Репродукция вируса начинается с транскрипции сверхранних иРНК, кодирующих синтез “раздевающего” белка (он завершает депротеинизацию вирионов), после чего синтезируются ранние иРНК, транслирующие информацию о синтезе вирус-специфической репликазы. С дочерних молекул ДНК транслируется информация о синтезе многочисленных структурных и функциональных вирусных белков. Формирование вирионов происходит в цитоплазме клетки-хозяина. Зрелые вирионы доставляются через аппарат Гольджи к клеточной оболочке и при выходе из клетки приобретают двухслойную внешнюю оболочку из компонентов клетки-хозяина.
Во время болезни в крови находится вирус, обладающий резко выраженными дерматотропными свойствами. Он также поражает слизистые оболочки и другие ткани и органы.
Для натуральной оспы характерны лихорадка, высыпания, образование пустул и рубцов на коже. В стадии нагноения присоединяется вторичная (стафилококковая и стрептококковая) инфекция. Летальность в зависимости от тяжести заболевания колеблется в широких пределах - от 0 до 100%; в среднем она равна 15-20%, при геморрагической форме - 100%.
У лиц с группой крови А и АВ натуральная оспа протекает тяжелее, смертельные исходы и поствакцинальные осложнения бывают чаще, постинфекционный и поствакцинальный иммунитет слабого напряжения.
Лабораторная диагностика натуральной оспы включает вирусологические (выделение вируса на куриных эмбрионах, клеточных культурах), серологические (микроферментный анализ, реакция торможения гемагглютинации, реакция связывания комплемента, реакция нейтрализации) и экспресс-методы (выявление под микроскопом элементарных телец-включений Пашена, выявление вирусного антигена в биологическом материале методами ИФА, РПГА) исследований.
Лечение. Специфическое лечение не разработано. В первые дни болезни применяют противооспенный иммуноглобулин, полученный из крови людей, специально вакцинированных против оспы, а также метисазон.
Иммунитет. У большинства людей, болевших оспой остается прочный иммунитет. Повторные заболевания крайне редки.
Применение противооспенной вакцинации привело к тому, что в 1980 году ВОЗ объявила о полной ликвидации этой болезни во всем мире, в связи с чем прививки против оспы были повсеместно прекращены.
Краснуха. Возбудителем заболевания является РНК-содержащий вирус, принадлежащий к семейству Togaviridae, роду Rubivirus. Этот вирус является единственным представителем рода, не входящего в экологическую группу арбовирусов.
Морфология. Вирус имеет сложную структуру, преимущественно сферической формы диаметром около 60 нм. Геном представлен однонитчатой нефрагментированной РНК. Вирионая РНК инфекционна и во взаимодействии со структурным полипептидом формирует нуклеокапсид изометрической формы. Вирус имеет суперкапсид, в состав которых входят два структурных белка. Белки вируса обладают гемолитической, гемагглютинирующей и нейраминидазной активностью.
Резистентность. Вирус чувствителен к ультрафиолетовым лучам, формалину и эфиру. Инактивируется при 56оС в течение 60 минут. Длительно сохраняется при 3-4оС, особенно в замороженном состоянии.
Патогенез. Вирус краснухи патогенен для макак-резусов, кроликов, хомяков, эмбрионов кур. Источником заражения служат больные люди. Заражение происходит воздушно-капельным путем. Наиболее восприимчивыми являются дети в возрасте 2-14 лет. Описаны эпидемические вспышки среди военнослужащих США.
С места первичной локализации вирус проникает в кровь, лимфатические узлы, плаценту у беременных женщин. Наиболее характерные признаки болезни - сыпь, воспаление лимфатических узлов. В период высыпания температура тела поднимается до 38оС. У взрослых краснуха протекает тяжелее, чем у детей, при более высокой температуре, сильных головных болях и болях в шейных мышцах. В качестве осложнений могут быть энцефалиты и энцефаломиэлиты. Вирус краснухи вызывает различные аномалии развития плода (микроцефалия, глухота, пороки сердца, катаракта и др.).
Иммунитет. После перенесенного заболевания иммунитет стойкий и пожизненный.
Лабораторная диагностика. Выделение вируса краснухи из материала больных в культуре клеток сложно и трудоемко. Оптимальным является использование (если возможно) первично-трипсинизированных культур клеток почек зеленых мартышек (Vero), эмбриона кролика либо перевиваемых клеточных культур,
В связи с трудоемкостью и длительностью выделения вируса на клеточных культурах (цитопатическое действие развивается медленно к 21 дню культивирования) для диагностики краснухи используют преимущественно серологические методы исследований (реакцию нейтрализации - РН. реакцию торможения гемагглютинации - РТГА, иммуноферментный анализ - ИФА и др.).
Лечение симптоматическое. Вводят иммуноглобулин из донорской крови, хотя эффективность его невысокая, антигистаминные препараты.
Для специфической профилактики разработана и апробирована живая ослабленная вакцина.
Дата публикования: 2014-11-19; Прочитано: 739 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
