 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Уравнения максимальной работы (уравнения Гиббса-Гельмгольца)
|
|
Свойства функций F и G дают возможность установить связь между максимальной работой процесса, протекающего равновесно, и теплотой того же процесса, но протекающего неравновесно.
 = – S, F = U – TS, F = U + T
= – S, F = U – TS, F = U + T 
Запишем это уравнение для двух состояний системы:
F1 = U1 + T 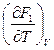 , F2 = U2 + T
, F2 = U2 + T 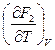
F1 – F2 = U1 – U2 + T  (F1 – F2)V = – DF
(F1 – F2)V = – DF
Amax =  + T
+ T  (1)
(1)
Видно: зная Amax (или изменение изохорного потенциала) и зависимость ее от Т, можно вычислить теплоту процесса (т.е. изменение внутренней энергии).
Если же известна Q процесса, то для расчета Amax необходимо интегрировать уравнение (1), причем появляется постоянная интегрирования, для определения которой необходимы дополнительные сведения.
Уравнение (1) – уравнение максимальной работы (уравнение Гиббса-Гельмгольца) – может быть записано и в форме:
DF = DU + T 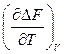 (2)
(2)
Другие варианты уравнения Гиббса-Гельмгольца:
 = – S, G = H – TS, G = H + T
= – S, G = H – TS, G = H + T 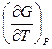
G1 = H1 + T 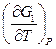 , G2 = H2 + T
, G2 = H2 + T 
G1 – G2 = H1 – H2 + T  (G1 – G2)P
(G1 – G2)P
A¢max =  + T
+ T 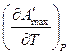 (3)
(3)
DG = DH + T  (4)
(4)
DU = QV и DH = QP справедливы, если в 1-м случае не совершается никакая работа (А = 0), а во 2-м случае совершается только работа расширения (А¢ = 0). Поэтому в уравнениях (1) и (3) теплоты  и
и  относятся не к процессам, которым соответствуют работы А или А¢, а к процессам, протекающим между теми же начальным и конечным состояниями, но без совершения работы (для QV) или с совершением только работы расширения (для QP), т.е. в неравновесных условиях. Теплоты же равновесного процесса, равные ТDS, выражаются последними членами уравнений (1) и (3).
относятся не к процессам, которым соответствуют работы А или А¢, а к процессам, протекающим между теми же начальным и конечным состояниями, но без совершения работы (для QV) или с совершением только работы расширения (для QP), т.е. в неравновесных условиях. Теплоты же равновесного процесса, равные ТDS, выражаются последними членами уравнений (1) и (3).
Исходя из вышеизложенного, эти уравнения можно записать так:
– DF = Amax = – QV, неравн + QV, равн
– DG = A¢max = – QP, неравн + QP, равн
Дата публикования: 2015-11-01; Прочитано: 357 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
