 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Изохорно-изотермический потенциал
|
|
(Изохорный потенциал, свободная энергия, энергия Гельмгольца)
dQ = dU + dA £ TdS
dA £ TdS - dU; T = const
A £ T (S2 - S1) - (U2 - U1), A £ (U1 - TS1) - (U2 - TS2)
U - TS = F DF = DU - TDS
F - свободная энергия системы; F - функция состояния системы, т.к. U, T, S - тоже функции.
A £ F1 - F2; A £ - DF
В равновесных процессах A = - DF (равна убыли F) Þ работа равновесного процесса (максимальная работа) не зависит от пути, а определяется лишь начальным и конечным состояниями системы.
U = F + TS
U можно рассматривать как состоящую из двух частей - свободной энергии F и связанной энергии TS: лишь часть внутренней энергии (свободная энергия F, которую система отдает вовне при T = const) может превратиться в работу. Другая часть внутренней энергии - связанная энергия - при изменении системы при T = const не дает работы, а переходит только в теплоту:
TS = K; dK = TdS + SdT; SdT = 0
dK = TdS; DK = TDS = Q
Для процессов, протекающих с изменением Т (Т ¹ const) деление «U» на свободную и связанную не может быть проведено и сами термины не имеют общего значения.
Экстенсивные и интенсивные параметры состояния системы:
1. Экстенсивные (емкостные) параметры зависят от количества вещества (от массы, V): это m, V, CP, CV, S, U. Эти параметры обладают свойством аддитивности.
2. Интенсивные параметры от количества вещества не зависят, а определяются специфическим характером состояния системы. Это Т, Р, химический потенциал. Экстенсивные факторы, отнесенные к единице массы (объема) становятся интенсивными (плотность вещества r, Vуд).
S обладает свойством аддитивности (S всей системы равна сумме S частей системы). S - фактор емкости связанной энергии.
Изохорный потенциал есть функция V и Т:
1. Равновесные процессы: F = U – TS
dF = dU – TdS – SdT, dU = TdS – dA
dF = TdS – dA – TdS – SdT
dF = – PdV – SdT, F = F(V,T)
– это полный дифференциал функции от V,T.
dF = 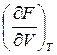 dV +
dV + 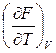 dT;
dT; 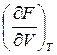 = – P,
= – P, 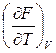 = – S
= – S
P – мера убыли F с ростом V при T = const
S – мера убыли F с ростом Т при V = const
2. Неравновесные процессы
dU £ TdS – dA, dF £ TdS – PdV – TdS – SdT
Дата публикования: 2015-11-01; Прочитано: 576 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
