 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Решение. Пусть масса раствора серной кислоты (w% = 61,25 %) будет х г, тогда из уравнения реакции
|
|
SO3 + H2O = H2SO4.
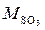 = 80 г/моль;
= 80 г/моль;  = 98 г/моль.
= 98 г/моль.
Пусть масса раствора серной кислоты (w % = 61,25 %) будет х г, тогда из уравнения реакции и условия задачи следует, что масса H2SO4 (w % = 100 %) составит 49 г. По правилу смешения получим
49∙100 + 61,25∙ х = (40 + х)∙73,5.
Отсюда х = 160 г.
Ответ. Масса раствора серной кислоты с концентрацией 61,25 % составляет 160 г.
Пример 11. Определите массовую долю (w %) CaCl2 в растворе, полученном при растворении CaCl2∙6H2O массой 21,9 г в воде объемом 100 см3.
Дата публикования: 2015-10-09; Прочитано: 571 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
