 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Сложная реакция
|
|
Для расчета равновесного состава смеси, в которой протекает сложная реакция, описываемая несколькими уравнениями, надо использовать только стехиометрически независимые уравнения как при расчете состава реагирующей смеси.Возможная последовательность расчета такая.
- Определяется базисная система стехиометрически независимых уравнений, позволяющая выразить концентрации всех компонентов смеси через степени превращения ключевого вещества в каждом уравнении выбранной системы.
Обозначим их C (x). Число определенных степеней превращения и количество уравнений в базисной системе совпадают.
Например, для конверсии метана определена базисная система уравнений
CН4 + Н2О = СО + 3Н2;
СН4 + 2Н2О = СO2 + 4Н2.
и получены выражения для концентраций всех веществ, т.е. C (x).
2. Сложное превращение может быть представлено протекающими реакциями, не обязательно совпадающими с уравнениями для расчета состава реагирующей смеси, но их число такое же, как в базисной системе уравнений. Для этих уравнений известны константы равновесия, и можно определить уравнения равновесия. Обозначим их K P j (C).
В примере конверсии метана такими реакциями являются реакции
CН4 + Н2О = СО + 3Н2;
СО + Н2О = СО2 + Н2,
и химическое равновесие - K P(C) - определяется уравнениями:
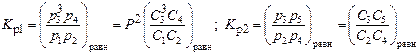
где К Р1, К Р2 – константы равновесия; р 1, р 2, р 3, р 4, р 5 – равновесные парциальные давления соответственно CН4, Н2О, Н2, СО, СО2; Сi – соответствующие концентрации (мольные доли).
3. Полученные зависимости C(x) подставляем в выражения KPj(C) и получаем зависимости KPj(х), в которых x становятся равновесными степенями превращения XР, т.е. получаем зависимости KP(XР). Для заданных условий (температура, давление) определяем константы равновесия реакций, и из уравнений KP(XР) определяем все значения XP. Теперь из имеющихся зависимостей C(x) можно рассчитать равновесный состав реакционной смеси – концентрации всех компонентов.
Изменение химического равновесия достигается изменением внешних условий. Направленность влияния определяется правилом, называемом принципом Ле-Шателье:
Дата публикования: 2015-10-09; Прочитано: 264 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
