 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Число подуровней на энергетических уровнях
|
|
| Главное квантовое число n | Орбитальное число l | Число подуровней | Обозначение подуровня |
| 1s | |||
| 0, 1 | 2s2p | ||
| 0, 1, 2 | 3s3p3d | ||
| 0, 1, 2, 3 | 4s4p4d4f |
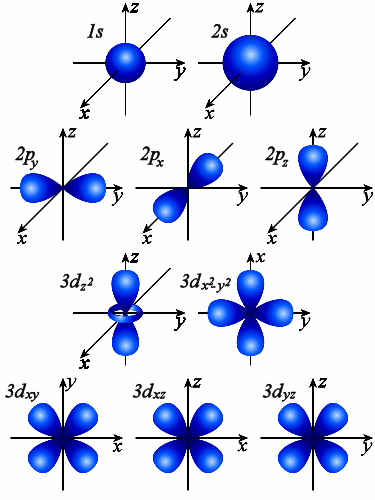
Рис. 7. Изображение форм и ориентаций
s -, p -, d -, орбиталей с помощью граничных поверхностей.
Квантовое число ml называют магнитным. Оно определяет пространственное расположение атомной орбитали и принимает целые значения от – l до + l через нуль, то есть 2 l + 1 значений (табл. 27).
Орбитали одного подуровня (l = const) имеют одинаковую энергию. Такое состояние называют вырожденным по энергии. Так p -орбиталь – трехкратно, d – пятикратно, а f – семикратно вырождены. Граничные поверхности s -, p -, d -, орбиталей показаны на рис. 7.
s -орбитали сферически симметричны для любого n и отличаются друг от друга только размером сферы. Их максимально симметричная форма обусловлена тем, что при l = 0 и μ l = 0.
Таблица 27
Дата публикования: 2014-11-18; Прочитано: 714 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
