 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Т.е., при которых одни и те же исходные вещества, одновременно реагируя между собой, образуют разные продукты
|
|
Примером подобного типа реакций является реакция разложения бертолетовой соли KClO3, способная протекать при определённых условиях в двух направлениях

Параллельно по двум и более механизмам может протекать распад ядер атомов некоторых радиоактивных элементов. Особенно часто параллельные реакции встречаются в органической химии. Например, при сульфировании толуола серной кислотой могут одновременно образоваться орто- и парасульфопроизводные:

В некоторых случаях параллельными могут быть и биохимические реакции, протекающие в клетках живых организмов. Например, ферментативное брожение глюкозы:
1) С6H12O6 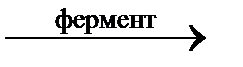 2 С2H5OH + 2CO2 ↑
2 С2H5OH + 2CO2 ↑
спиртовое брожение
2) С6H12O6 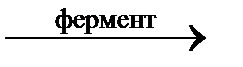 СH3 – CH(OH) – COOH
СH3 – CH(OH) – COOH
молочнокислое брожение
При определённых условиях многие параллельные реакции могут протекать преимущественно только в каком-нибудь одном направлении.
Скорость параллельной реакции определяется скоростью наиболее быстрой её стадии.
Последовательными называются такие реакции, в которых образование конечного продукта из исходных веществ происходит не непосредственно, а обязательно через ряд промежуточных стадий, протекающих одна за другой в строго определённой последовательности. Схематически такой процесс можно изобразить следующим образом:
А → В → С → D,
где каждой буквой обозначается отдельная стадия процесса. В общем случае число таких стадий в последовательных реакциях может быть самым разным (от нескольких единиц до нескольких десятков). Причём каждая из стадий, в свою очередь, не обязательно является простой моно- или бимолекулярной реакцией, но может быть и сложной.
Последовательные реакции распространены в природе и особенно часто они наблюдаются в биохимических процессах, протекающих в живых организмах, растениях. В качестве примера таких реакций можно привести фотосинтез и биологическое окисление глюкозы, гидролиз олиго- и полисахаридов и т.д.
Расчёт кинетики последовательных реакций сложен и достаточно точно может быть осуществлён лишь для сравнительно простых процессов, состоящих из небольшого числа стадий.
Однако, если одна из стадий последовательной реакции обладает значительно меньшей скоростью, чем все остальные, то общая скорость реакции будет определяться скоростью именно этой стадии, которая в данном случае называется лимитирующей .
Например, реакция хлорирования оксида азота (II)
2NO + Cl2 = 2NOCl
состоит из двух стадий:
1) NO + Cl2 = NOCl2;
2) NOCl2 + NO = 2NOCl
Первая стадия протекает быстро с образованием нестойкого продукта NOCl2. Вторая стадия является медленной и лимитирующей. Скорость всей реакции описывается кинетическим уравнением
u= k 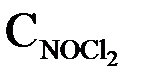 · CNO
· CNO
и общий порядок данной реакции равен 2.
Сопряжёнными называют реакции, протекающие по следующей схеме:
А + В ® М
А + С ® D
Одна из этих реакций может протекать самостоятельно, а вторая реакция осуществима только в присутствии первой. Таким образом, протекание одной реакции инициирует осуществление второй.
Сопряжённые реакции возможны в биохимии. Они протекают в клетках, причём энергию, необходимую для течения второй реакции с ΔG2 > 0, доставляет первая реакция, для которой ΔG1 < 0. Причём │ΔG1│> │ΔG2│, т.е. весь процесс в целом протекает с уменьшением энергии Гиббса. Подобные биохимические реакции иначе называются тандемными.
Часто механизм сопряжённых реакций заключается в образовании на первой стадии активных промежуточных частиц (радикалов или ионов), которые инициируют протекание всех остальных реакций.
Схему сопряженных реакций такого типа можно в общем виде представить следующим образом:

где С – активная промежуточная частица.
Например, бензол в водном растворе не окисляется Н2О2, но при добавлении соли двухвалентного железа происходит его превращение в фенол и дифенил. Чтобы «запустить данный процесс, ионы Fe2+ сперва вступают во взаимодействие с Н2О2, образуя радикалы ·ОН
Fe2+ + H2O2 → Fe3+ + OH– + ˙ OH,
которые затем реагируют как с бензолом
С6Н6 + ˙ ОН → ˙ С6Н5 + Н2О
˙ С6Н5 + ˙ ОН → С6Н5ОН
так и с Fe2+
Fe2+ + ˙ OH → Fe3+ + OH–
Явление химической индукции впервые было исследовано Н.А. Шиловым в 1905 г.
Цепными называют химические реакции, протекающие через ряд регулярно повторяющихся элементарных стадий с участием активных частиц, содержащих в своём составе атомы с неспаренными электронами на внешнем энергетическом уровне (или по другому – свободных радикалов).
К цепным относятся реакции горения, полимеризации и поликонденсации, распада ядер и др.
Механизм цепных реакций состоит в том, что свободные радикалы (часто в их роли выступают одиночные атомы) обладают высокой химической активностью. Они легко вступают во взаимодействие с устойчивыми молекулами и превращают их в активные частицы, которые затем образуют продукты реакции и новые радикалы, и таким образом возникает цепь дальнейших стадий. Цепная реакция продолжается, пока не прореагирует всё вещество, или пока не исчезнут активные частицы-радикалы.
Для цепных реакций характерны три этапа: 1) зарождение цепи; 2) развитие цепи или её рост; 3) обрыв цепи.
Зарождение цепи начинается с элементарного химического акта, в результате которого образуется активная частица. Этот процесс требует затраты энергии и может идти при нагревании вещества, воздействии ионизирующего излучения, действии катализатора.
Например, в реакции синтеза хлороводорода и водорода и хлора, протекающей по цепному механизму (Н2 + Cl2 = 2 HCl), возникновению цепи соответствует процесс
Cl2 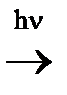 2 ∙ Сl
2 ∙ Сl
Развитие цепи представляет собой периодическое повторение стадий реакции с участием образовавшихся радикалов. Они иначе называются звеньями цепи:
Н2 + · Cl → HCl + ˙ H
˙ H + Cl2 → HCl + ˙ Cl
H2 + ˙ Cl → HCl + ˙ H
Cl2 + ˙ H → HCl + ˙ Cl и т.д.
Длина цепи определяется числом молекул исходного вещества, прореагировавшего в результате одного акта зарождения цепи, до её обрыва.
По особенностям стадии развития цепные реакции делят на неразветвлённые и разветвлённые. В первом случае количество свободных активных частиц-радикалов остаётся неизменным на протяжении всего данного этапа.
В разветвлённых цепных реакциях расход одной активной частицы приводит к образованию нескольких (двух или более) других активных частиц. Схематически это можно представить следующим образом:

Обрыв цепи соответствует исчезновению активных частиц в результате их взаимодействия друг с другом:
˙ H + ˙ H = H2
˙ Cl + ˙ Cl = Cl2 обрыв цепи
˙ H + ˙ Cl = HCl
Кроме того, он может происходить при адсорбции частиц стенками сосуда, при столкновении двух активных частиц с третьей (называемой ингибитором), которой активные частицы отдают избыточную энергию. Поэтому для цепных реакций характерны зависимость их скорости от размеров, формы и материала реакционного сосуда, от наличия посторонних инертных веществ, выполняющих роль ингибитора.
Скорость неразветвлённых цепных реакций определяется скоростью наиболее медленной стадии, т.е. зарождением цепи. Для каждой стадии в реакциях данного типа используются обычные уравнения химической кинетики (первого или второго порядка).
Разветвлённые химические реакции могут протекать по сложному кинетическому закону и не иметь определённого порядка. «Размножение» радикалов в них часто приводит к лавинообразному течению процесса, которое вызывает взрыв. Однако и в этих реакциях возможен обрыв цепи. Поэтому бурное увеличение скорости процесса (вплоть до взрыва) происходит в том случае, если темп разветвления цепи опрежает темп её обрыва. Теория цепных реакций была разработана в трудах академика Н.Н. Семёнова, С.Н. Хиншельвуда (Англия) и др. учёных.
Существуют цепные реакции, в которых в роли активных частиц выступают не радикалы, а ионы, образующиеся в результате гетеролитического разрыва химической связи:
А: В → Аˉ: + В+
Подобный механизм на практике часто реализуется в реакциях полимеризации непредельных органических соединений.
Дата публикования: 2014-11-03; Прочитано: 1036 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
