 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Вводная часть. Уважаемые искатели научной истины, Вы уже вооружены знаниями условий реализации аксиомы Единства
|
|
ДЕСЯТАЯ И ОДИНАДЦАТАЯ ЛЕКЦИИ АКCИОМЫ ЕДИНСТВА
ЭВОЛЮЦИЯ ТЕОРИЙ АТОМА
Вводная часть
Уважаемые искатели научной истины, Вы уже вооружены знаниями условий реализации аксиомы Единства. Она помогла нам найти уравнения для расчета спектров атомов и ионов, из которых следует отсутствие орбитального движения электронов в атомах. Теперь мы должны понять суть ошибочности постулатов и теорий атома, доказывавших орбитальное движение электрона. Наиболее последовательно эти постулаты и теории кратко изложены в книге [17].
Первое представление о структуре атома было теоретически обосновано Нильсом Бором в 1913 г. Главным его вкладом в теорию атома является гипотеза о квантовании орбитального момента импульса  электрона атома водорода (рис. 40) [17]
электрона атома водорода (рис. 40) [17]
 , (218)
, (218)
где  - масса электрона;
- масса электрона;  - орбитальная скорость электрона;
- орбитальная скорость электрона;  - радиус орбиты;
- радиус орбиты; 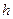 - постоянная Планка;
- постоянная Планка;  - номер орбиты, главное квантовое число.
- номер орбиты, главное квантовое число.
Из условия квантования (218), как мы уже показали, легко выводится формула для расчета спектра атома водорода [1]. Считается, что правило квантования орбитального момента импульса, предложенное Нильсом Бором, оставалось гипотезой до тех пор, пока Луи Де Бройль[1] не высказал предположение о том, что длина волны  электрона связана с его импульсом
электрона связана с его импульсом  соотношением
соотношением  и что в орбите электрона должно укладываться целое число
и что в орбите электрона должно укладываться целое число  волн электрона
волн электрона  . Из этого сразу последовал постулат Бора о квантовании орбитального момента импульса
. Из этого сразу последовал постулат Бора о квантовании орбитального момента импульса  электрона [1]
электрона [1]
 (219)
(219)
и появилась странность. Как понимать тот факт ( ), что длина окружности первой орбиты (
), что длина окружности первой орбиты ( ) равна длине одной волны
) равна длине одной волны  электрона? Отсутствие ответа на этот вопрос не смутило Арнольда Зоммерфельда и он предложил в 1915 г. теорию о движении электронов по эллиптическим орбитам. При этом он допустил, что энергия электрона на каждой из таких орбит не меняется. Меняется только орбитальный момент импульса
электрона? Отсутствие ответа на этот вопрос не смутило Арнольда Зоммерфельда и он предложил в 1915 г. теорию о движении электронов по эллиптическим орбитам. При этом он допустил, что энергия электрона на каждой из таких орбит не меняется. Меняется только орбитальный момент импульса  . Конечно, это странное допущение и, тем не менее, оно было принято, и процесс развития теории атома в орбитальном направлении продолжился [17].
. Конечно, это странное допущение и, тем не менее, оно было принято, и процесс развития теории атома в орбитальном направлении продолжился [17].
Зоммерфельд ввел новое правило квантования орбитального момента импульса. Вместо зависимости (219) он предложил зависимость [17]
 , (220)
, (220)
где  - второе квантовое число.
- второе квантовое число.
В результате появилась необъяснимая закономерность изменения обоих квантовых чисел  и
и  . Так, при
. Так, при  ,
,  . Когда
. Когда  , второе квантовое число принимает значения 0 или 1. Если
, второе квантовое число принимает значения 0 или 1. Если  , то
, то  принимает значения 0, 1 или 2 и т. д. При расчете спектров было установлено, что
принимает значения 0, 1 или 2 и т. д. При расчете спектров было установлено, что 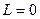 для основного состояния электрона. Однако с точки зрения классической механики электрон в этом случае должен двигаться по прямой линии, проходящей через ядро [17].
для основного состояния электрона. Однако с точки зрения классической механики электрон в этом случае должен двигаться по прямой линии, проходящей через ядро [17].
Так множились противоречия теории орбитального движения электрона в атоме и неясно было, как эти противоречия устранять. Почему орбитальный момент импульса электрона должен равняться нулю, когда он находится на первой орбите? Этот вопрос висит в воздухе до сих пор. Физики и химики привыкли к такому положению и уже не замечают этого вопроса. Не получив ответа на него, исследователи пошли дальше. Они присвоили названия состояниям электрона в момент, когда он имеет различные орбитальные моменты импульса (табл. 31) [17].
Таблица 31.
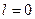
| 
|
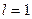
| 
|

| 
|

| 
|

| 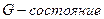
|
Последующие исследования показали, что в действительности орбитальный момент импульса изменяется по зависимости [17]
 . (221)
. (221)
Углубление теории орбитального движения Зоммерфельдом не позволило рассчитывать спектры атомов сложнее водородоподобных (атомов и ионов с одним электроном) атомов. Это означало отсутствие понимания процесса взаимодействия электрона с ядром атома. Но на это не обращали внимание и двигались дальше в ложном направлении [17].
Так как заряд электрона отрицательный, то условились считать, что векторы орбитального момента импульса  и магнитного момента
и магнитного момента  электрона направлены противоположно. Странное соглашение. Векторные свойства физическим величинам задаёт Природа, а знак электрону приписан человеком. Разве этого достаточно, чтобы считать векторы
электрона направлены противоположно. Странное соглашение. Векторные свойства физическим величинам задаёт Природа, а знак электрону приписан человеком. Разве этого достаточно, чтобы считать векторы  и
и  противоположно направленными? [17].
противоположно направленными? [17].
Следующее соглашение оказалось ещё абсурднее. Известно, что спин  – величина векторная. Он характеризует вращение частицы, в данном случае - вращение электрона относительно своей оси симметрии. Чтобы объяснить расщепление спектральных линий при наличии магнитного поля, было принято соглашение считать, что его проекция
– величина векторная. Он характеризует вращение частицы, в данном случае - вращение электрона относительно своей оси симметрии. Чтобы объяснить расщепление спектральных линий при наличии магнитного поля, было принято соглашение считать, что его проекция  на выбранное направление может иметь лишь два значения [17]
на выбранное направление может иметь лишь два значения [17]
 , (222)
, (222)
где  .
.
На этом странности теории атома не закончились. Было введено понятие «полный момент импульса», равный  . Здесь
. Здесь  - квантовое число полного момента импульса, а величина
- квантовое число полного момента импульса, а величина  изменятся так
изменятся так  и
и  [17].
[17].
Странно, но вопрос о закономерности изменения энергии связи электрона с ядром атома при орбитальных переходах электрона так никто и не поставил. А ведь это главный вопрос при анализе всех химических реакций. Почему он не был поставлен? Это - загадка и историки науки, несомненно, будут разгадывать её. Не был поставлен и второй фундаментальный вопрос: каким образом электроны двух атомов, летающие по орбитам вокруг их ядер, соединяют атомы в молекулы? Вместо того, чтобы поставить эти вопросы и искать на них ответы, исследователи пошли дальше в тупиковом направлении. Обилие квантовых чисел затуманило орбитальное движение электрона в атоме. Плотность этого тумана увеличило уравнение Шредингера (17).
Из уравнения Шредингера (17) следовала невозможность определения положения электрона в атоме. Можно было оценить лишь плотность вероятности пребывания его в атоме. Чтобы спасти идею орбитального движения электрона, плотность этой вероятности назвали орбиталью и стали представлять её в виде электронного облака определенной формы (рис. 79) [27].

Дата публикования: 2014-11-04; Прочитано: 1356 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
