 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Важнейшие области применения лития и его соединений
|
|
Благодаря своим уникальным свойствам литий играет важную роль в индустриальном развитии современного общества. Области его практического применения, неразрывно связанные с применением высоких технологий, весьма разнообразны и включают:
· производство первичных и вторичных аккумуляторных батарей;
· производство химических компонентов для ядерных энергетических реакторов;
· производство специальных масел и смазок;
· производство стекла, керамики и синтетических волокон;
· производство первичного алюминия;
· металлургию легких конструктивных сплавов;
· производство хладагентов и систем осушки воздуха;
· производство дезинфицирующих средств и др.
Металлургия алюминия. Одна из наиболее важных и традиционных областей применения лития – применение его в электролитическом получении алюминия. Добавка карбоната лития (Li2CO3) в электролитическую ванну позволяет снизить температуру плавления электролита, уменьшить выделение фтора, увеличить электропроводность электролита, уменьшить расход анода и криолита (K3AlF6) и, следовательно, уменьшить расход электроэнергии, т.е. снизить себестоимость металла. На 1 тонну алюминия расходуется 2,5-3,5 кг Li2CO3. Потребление лития растет с каждым годом пропорционально объему мировой добычи алюминия.
Ядерная энергетика – это главная применения лития, делающая его одним из важнейших металлов.
Изотопы 6Li и 7Li обладают разными ядерными свойствами (сечение поглощения тепловых нейтронов, продукты реакций) и среда их применения различна. Гафнат лития входит в состав специальных ядерных отходов, содержащих плутоний. Изотоп Li-6 применяется в термо-ядерной энергетике. При облучении нуклида 6Li тепловыми нейтронами получается радиоактивный изотоп тритий:
 +
+  =
=  +
+  (21)
(21)
Благодаря этому 6Li может применяться как замена радиоактивного нестабильного и неудобного в обращении трития как в военных (термоядерное оружие), так и в мирных (управляемый термоядерный синтез) целях. В термоядерном оружии обычно применяется дейтерид лития 6LiD.
Изотоп Li-7 используется в ядерных реакторах в качестве теплоносителя (часто в виде сплава с Na или Cs-133) для охлаждения реакторов. Использование лития как теплоносителя основано на том, что он имеет большой диапазон жидкого состояния при малой плотности и высокой теплопроводности. Фторид 7Li в сплаве с фторидом бериллия (66 % LiF + 34 % BeF2) носит название «флайб» и применяется как высокоэффективный теплоноситель и растворитель фторидов урана и тория в высокотемпературных жидкосиловых реакторах.
Смазочные материалы. В авиации и военной технике широко применяются литиевые консистентные смазки, содержащие до 10 % стеарата лития. Они сохраняют уникальные физические свойства в температурном интервале от - 50 до + 150 ºC.
Силикатная промышленность. Высококачественные концентраты минералов лития, а также Li2CO3, Li2SiO3 широко используются в производстве стекла и керамики, Добавки лития повышают химическую и физическую устойчивость. Глазури и эмали с добавкой лития более плотны, блестящи, устойчивы к атмосферным воздействиям. Добавки лития используются в производстве стекла для катодно-лучевых трубок, сверхчувствительных, легкоплавких и других специальных стекол. При варке стекла добавки лития снижают температуру плавления и вязкости расплава.
Литий как дегазатор и рафинирующий агент. Так как литий химически активен, его используют для удаления газов из расплавленных металлов. Литий реагирует с водородом, кислородом, серой и азотом. Образующиеся при этом соединения имеют сравнительно низкие плотности и температуры плавления. Это важно для удаления твердых примесей из металла. Металлический литий обычно используют для дегазации меди, в особенности для получения отливок с высокой электропроводностью. Количество добавляемого лития составляет 0,01 % для бронз и 0,02 % для меди с высокой электропроводностью (вес отливки ~90 кг).
Сплавы. Сплавы лития с серебром и золотом, а также медью являются очень эффективными припоями. Сплавы лития с магнием, скандием, медью, кадмием и алюминием – новые перспективные материалы в авиации и космонавтике. На основе алюмината и силиката лития создана керамика, затвердевающая при комнатной температуре и используемая в военной технике, металлургии и, в перспективе, термоядерной энергетике. Литий эффективно упрочняет сплавы свинца и придает им пластичность и стойкость против коррозии. Эффективны стандартные алюминиевые сплавы, дополнительно легированные 1-3 % лития для использования в авиаракетокосмической технике. Пример такого сплава, %: 94,98 Al; 2,2 Li; 2,7 Cu; 0,12 Zr. Плотность таких сплавов меньше плотности стандартных сплавов на 8-12 %, они более устойчивы к коррозии, прочностные характеристики сохраняются или улучшаются. Применение их в самолетостроении позволяет снизить массу самолета на 20 %. Применение этих сплавов сдерживается высокой стоимостью, которая в 6-10 раз выше стоимости конкурирующих композиционных материалов.
Электроника. Триборат лития-цезия используется как оптический материал в радиоэлектронике. Кристаллические ниобат лития, LiNbO3, и танталат, LiTaO3, являются нелинейными оптическими материалами и широко применяются в нелинейной и интегральной оптике. На их основе создаются устройства для модуляции и отклонения лазерного луча, устройства для обработки и отображения информации, запоминающие устройства.
Лазерные материалы. Монокристаллы фторида лития используются для изготовления лазеров (КПД 80 %) на центрах свободной окраски и для изготовления оптики с широкой спектральной полосой пропускания.
Кондиционирование воздуха. Высокогигроскопичный бромид, LiBr, и хлорид, LiCl, благодаря их способности поглощать дымы, пары H2O, CO2, NH3, органические вещества используют для кондиционирования воздуха в различных помещениях.
Литий-ионные аккумуляторы. Литий-ионные аккумуляторы получили широкое распространение практически во всех сферах деятельности человека, начиная от бытовой техники и заканчивая оснащением космического оборудования, став в то же время объектом для исследований в направлении улучшения общей эффективности, долговечности и надежности.
Классический литий ионный аккумулятор состоит из отрицательного графитового электрода (катод), положительного электрода (анод) и электролита, заполняющего пространство между электродами. В зависимости от типа анода литиевые элементы способны создавать напряжение от 1,5 до 3,6В, что выше, чем у любых других элементов. В качестве анода используется, как правило, оксид переходного металла, содержащего литий, например, кобальтит лития, литий-марганцевые шпинели (LiMn2O4); в последнее время показана перспективность использования более дешевого LiFeO4. Аккумуляторы такого типа используются в кардиостимуляторах, в портативных компьютерах. Они имеют большую плотность, чем металлогидридные, и работают без подзарядки в полтора раза дольше. Из рис. 9 видно, что процесс зарядки-разрядки батареи не ограничивается переносом только ионов лития. Одновременно в том же направлении происходит перенос электрона, так что убыль положительного заряда (Li+) компенсируется уходом электрона, а прибыль положительного заряда (Li+) на катоде – приходом электрона. Перенос электронов осуществляется по внешнему токопроводу, соединяющих оба электрода. Уравнения основных реакций, протекающих в литий-ионном аккумуляторе:
заряд:
LiCoO2 – xLi+ – xē → Li1-xCoO2 (22)
6C + xLi+ + xē → LixC6 (23)
разряд:
Li1-xCoO2 + xLi+ + xē → LiCoO2 (24)
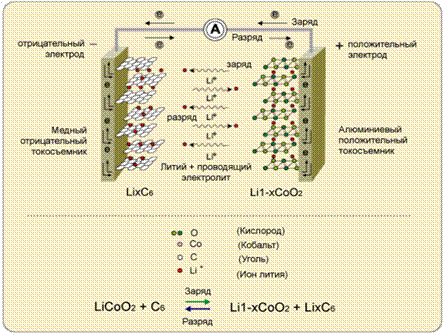 |
Рис. 9. Механизм работы литий-ионного аккумулятора
Технология производства литиевых аккумуляторов непрерывно совершенствуется в направлении поиска и усовершенствования материалов электродов и состава электролита.
В 2009 году исследователи из Массачусетского технологического института (MIT) предложили новую технологию изготовления литий-ионных аккумуляторов, которая позволяет сократить время зарядки батарей с часов и десятка минут до секунд.
Дата публикования: 2015-10-09; Прочитано: 4740 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
