 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Зміна ентропії в реальних системах
|
|
Процес вирівнювання температур тим ближчий до оборотного, чим швидше у всьому об’ємі змішуваних тіл зникають місцеві (локальні) неоднорідності температур і чим менші розміри (об’єми) цих тіл. У реальному нерівноважному процесі швидкість вирівнювання температур тіл, що дотикаються, розрахована на одиницю об'єму, обернено пропорційна теплоємності тіл.
Якщо в калориметр із певною кількістю води за заданої температури опустити нагріте до більшої температури тіло, відбудеться теплообмін і встановиться загальна температура. Повторимо дослід із тими ж вихідними даними, зменшивши теплоємність зануреного тіла; одержимо ближчий до оборотного процес. Ступінь його оборотності в ізольованій системі можна визначити, розрахувавши зміну ентропії. Для твердого і рідкого тіла  , де
, де 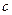 – питома теплоємність тіла,
– питома теплоємність тіла,  – його маса.
– його маса.
Роботою розширення можна знехтувати, тому 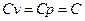 . Зміна ентропії процесу між станами 1 і 2:
. Зміна ентропії процесу між станами 1 і 2:
 . (10)
. (10)
Внаслідок адитивності ентропії  ,
,
де  - зміна ентропії системи тіла,
- зміна ентропії системи тіла,  - зміна ентропії одного тіла,
- зміна ентропії одного тіла,
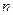 - кількість тіл системи.
- кількість тіл системи.
До складу цієї системи входять: досліджуване тіло масою 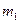 з питомою теплоємністю
з питомою теплоємністю 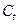 і початковою температурою
і початковою температурою 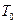 (температура пари киплячої води за шкалою Кельвіна), калориметр масою
(температура пари киплячої води за шкалою Кельвіна), калориметр масою  , з питомою теплоємністю
, з питомою теплоємністю  й початковою температурою
й початковою температурою 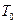 ; вода в калориметрі, масою
; вода в калориметрі, масою  з
з 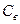 - питомою температурою води й початковою температурою
- питомою температурою води й початковою температурою  . Після закінчення процесу теплообміну встановиться температура
. Після закінчення процесу теплообміну встановиться температура  .
.
Під час вирівнювання температури ентропія кожного з тіл змінюється:
 (тіло);
(тіло);  (калориметр),
(калориметр),  (вода).
(вода).
Зміна ентропії всієї системи:
 . (11)
. (11)
Розраховуємо зміну ентропії декількох тіл під час опускання їх у воду.
Хід роботи
1. Використовуючи дані вимірювань роботи №14, розраховують  за формулою (11).
за формулою (11).
Контрольні питання
1. Друге начало термодинаміки.
2. Що таке ентропія та її зміни?
3. Оборотні й необоротні процеси.
Лабораторна робота №14
Дата публикования: 2015-09-17; Прочитано: 294 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
