 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Свойства лиофобных коллоидных растворов
|
|
Основные свойства лиофобных золей связаны с их ультрамик-рогетерогенностью, т. е. мельчайшими размерами частиц дисперсной фазы, и огромной суммарной поверхностью раздела между дисперсной фазой и дисперсионной средой.
Молекулярно-кинетические свойства (МКС). К ним относятся свойства, связанные с тепловым движением частиц: броуновское движение, диффузия, осмос. Эти свойства зависят от размеров и массы частиц дисперсной фазы (броуновское движение и диффузия), а также от числа частиц в единице объема системы (осмотическое давление). Так как размеры коллоидных частиц значительно больше размеров отдельных ионов и молекул, то, при одинаковой массовой концентрации, число коллоидных частиц в единице объема коллоидного раствора будет гораздо меньше, чем число молекул или ионов в единице объема истинных растворов низкомолекулярных веществ. Этим объясняется тот факт, что МКС в коллоидных растворах выражены менее интенсивно, чем в истинных: скорость диффузии коллоидных частиц очень мала, осмотическое давление коллоидных растворов низкое. Так, осмотическое давление 1 % истинного раствора сахара составляет 79,5 кПа, а 1 % коллоидного раствора сульфида мышьяка(3) AS2S3 - всего 3,4 • 10-3 кПа. Оптические свойства. Специфическим свойством коллоидных растворов является их способность рассеивать свет. Это обусловлено гетерогенностью коллоидных систем и размерами коллоидных частиц.
Грубодисперсные системы, размеры частиц в которых (r > > 10-6 м) значительно превышают длины волн видимого света (𝝀 = (3,6-7,6) • 10-7 м), отражают свет и поэтому выглядят мутными. В истинных растворах низкомолекулярных веществ молекулы и ионы имеют размеры 10-10-10-9 м, что значительно меньше длин волн видимого света, поэтому они пропускают свет и являются прозрачными.
Если размеры коллоидных частиц (r = 10-7-10-6 м) соизмеримы с длинами волн видимого света, то такие коллоидные растворы рассеивают свет вследствие явления дифракции. Рассеяние света можно наблюдать при боковом освещении коллоидного раствора: в случае точечного источника света - в виде светящегося конуса (эффект Тиндаля), а при обычном боковом освещении - в виде голубоватой опалесценции раствора. Согласно закону Рэлея интенсивность рассеянного света I зависит от интенсивности I 0 и длины волны X падающего света, объема частиц V и их концентрации с:

где К - константа, зависящая от соотношения коэффициентов преломления дисперсионной среды и дисперсной фазы.
Из этого выражения следует, что чем меньше длина волны падающего излучения, тем больше будет рассеяние. Этим объясняется голубоватая опалесценция при боковом освещении коллоидных растворов. Красный свет имеет наибольшую длину волны (620-760 нм) в видимой части спектра и рассеивается в меньшей степени. Поэтому запрещающие сигналы имеют красный цвет. Рассеянный солнечный свет, который образуется из-за аэрозольных частиц в атмосфере, имеет голубую окраску и создает голубой цвет неба. На способности золей рассеивать свет основаны такие методы анализа, как нефелометрия и ультрамикроскопия, которые используются для определения концентрации частиц и их размеров в гетерогенных биологических средах.
Диализ. Биологические жидкости, как правило, содержат одновременно вещества в коллоидном состоянии и в виде отдельных молекул и ионов. Очистка коллоидных растворов от истинно растворенных веществ основывается на том, что относительно крупные коллоидные частицы, в отличие от молекул и ионов, не проникают сквозь поры животных и растительных мембран. На практике в качестве мембраны используется пленка из коллодия или целлофана (производные целлюлозы), а также кишечная ткань.
Диализ - процесс очистки коллоидных растворов от ионов и молекул низкомолекулярных примесей в результате их диффузии в чистый растворитель сквозь полупроницаемую мембрану.
Простейший способ диализа заключается в том, что коллоидный раствор помещают во внутренний сосуд, дно или стенки которого представляют собой мембрану с избирательной проницаемостью, погруженный во внешний сосуд с чистым растворителем (обычно вода). В результате диффузии молекулы и ионы, способные проникать сквозь поры мембраны, переходят в наружный сосуд. В обычных условиях диализ протекает очень медленно. Для ускорения процесса необходимо увеличить градиент концентраций растворенных веществ по обе стороны мембраны. Это легко осуществить периодической или непрерывной сменой растворителя в наружном сосуде (рис. 27.3, а).
Для ускорения очистки коллоидных растворов от ионов растворенных электролитов используют также метод электродиализа. В этом случае во внешний сосуд помещают электроды и подают постоянный электрический ток (рис. 27.3, б).
Электродиализ - это диализ в условиях наложения постоянного электрического поля, под действием которого катионы и анионы приобретают направленное движение к электродам.
 |
Электродиализ особенно эффективен при малых концентрациях удаляемого электролита, когда градиент концентраций невелик.
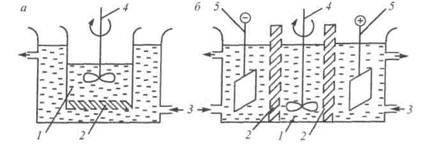
Рис. 27.3. Схемы диализатора (а) и электродиализатора (б):
1 - диализуемый коллоидный раствор; 2 - мембрана; 3 - подача растворителя; 4 - мешалка; 5 - электроды
В биологических жидкостях количественное определение низкомолекулярных веществ часто проводят методом компенсационного диализа, или вивидиализа. В этом случае биологическая жидкость в диализаторе омывается не чистым растворителем, а растворами с различными концентрациями определяемого вещества. Так, содержание сахара в сыворотке крови определяется путем диализа сыворотки по сравнению с изотоническим раствором, к которому добавляют различные количества сахара. Концентрация сахара во внешнем растворе не изменяется лишь в том случае, когда она равна концентрации сахара в анализируемой сыворотке. Таким образом было выявлено наличие глюкозы и мочевины в крови.
По принципу диализа работает аппарат «искусственная почка» (АИП), применяемый при острой почечной недостаточности, которая может наступить в результате отравления сулемой, сульфаниламидными препаратами, при уремии после переливания крови, при тяжелых ожогах и т. п. АИП подключается к системе кровообращения больного, и кровь протекает через систему, снабженную мембранами с избирательной проницаемостью, которые снаружи омываются физиологическим раствором. При этом кровь в процессе диализа очищается от вредных примесей, после чего поступает обратно в организм.
Устойчивость коллоидных растворов. Биологические жидкости живого организма, такие как кровь, плазма, лимфа, спинномозговая жидкость, моча, представляют собой коллоидные системы. О состоянии организма можно судить по многим показателям этих жидкостей, и прежде всего крови. Наличие патологических процессов сопровождается изменением количества форменных элементов крови (эритроцитов, лейкоцитов и др.), скорости оседания эритроцитов (СОЭ), свертываемости крови и др. Все эти свойства связаны с устойчивостью биологических жидкостей, поэтому изучение устойчивости коллоидных растворов и факторов, влияющих на нее, очень важно для медиков и биологов.
Устойчивость дисперсных систем характеризует способность дисперсной фазы сохранять состояние равномерного распределения частиц дисперсной фазы во всем объеме дисперсионной среды.
В дисперсных системах различают седиментационную и агрегативную устойчивость.
Едиментационная устойчивость характеризует способность частиц дисперсной фазы находиться во взвешен ном состоянии и не оседать под действием сил тяжести.
Агрегативная устойчивость характеризует способность частиц дисперсной фазы противодействовать их слипанию между собой и тем самым сохранять неизменными cвои размеры.
Грубодисперсные системы гетерогенны и неустойчивы. Они самопроизвольно расслаиваются на дисперсную фазу и дисперсионную среду, так как относительно крупные частицы дисперсной фазы под действием сил тяжести оседают (седиментируют).
Истинные растворы гомогенны и неограниченно устойчивы, поскольку в них не происходит самопроизвольное выделение растворенного вещества из системы.
Коллоидные растворы относятся к ультрамикрогетерогенным системам и по устойчивости занимают промежуточное положение между грубодисперсными системами и истинными растворами. Коллоидные растворы обычно представляют собой седиментационно устойчивые системы, что обусловлено малыми размерами частиц и их интенсивным броуновским движением.
Агрегативная устойчивость коллоидных растворов с ионным стабилизатором обусловлена наличием на поверхности частиц "рыхлой" ионной атмосферы из гидратированных противоионов, которая увеличивает сродство коллоидных частиц к дисперсной среде и препятствует их слипанию (коагуляции). Ее можно рассматривать как результат взаимодействия двух противоположно направленных сил, которые одновременно действуют на сближающиеся коллоидные частицы: вандерваальсовых сил межмолекулярного притяжения и электростатических сил отталкивания, которые возникают между одноименно заряженными частицами. При сближении коллоидных частиц на расстояние 10-9-10-6 м в области перекрывания их ионных атмосфер, в тонких жидких пленках, разделяющих две твердые поверхности (поверхности ядер), возникает так называемое расклинивающее давление. Оно складывается из трех основных составляющих:
- электростатическое отталкивание одноименно заряженных частиц за счет большого скопления противоионов в области контакта ионных атмосфер;
-
 |
расклинивание за счет упругих свойств гидратных оболочек, окружающих противоионы и состоящих из ориентированных (упорядоченных) диполей воды;
Рис. 27.4. Схема агрегативной устойчивости мицелл коллоидных растворов
- расклинивание за счет осмотического всасывания молекул растворителя в область контакта ионных атмосфер, т. е. в область большого скопления противоионов.
В коллоидных растворах с ионным стабилизатором главной составляющей расклинивающего давления является электростатическое отталкивание одноименно заряженных частиц. Величина расклинивающего давления зависит от заряда твердой фазы, т. е. от значения межфазного потенциала Фмф, а также от толщины ионной атмосферы, главным образом ее диффузного слоя, т. е. от значения  (рис. 27.4). Чем выше заряд твердой фазы, чем больше толщина диффузного слоя и больше значение
(рис. 27.4). Чем выше заряд твердой фазы, чем больше толщина диффузного слоя и больше значение  , тем больше расклинивающее давление между частицами и выше агрегативная устойчивость коллоидного раствора. Когда диффузный слой мицеллы тонкий и
, тем больше расклинивающее давление между частицами и выше агрегативная устойчивость коллоидного раствора. Когда диффузный слой мицеллы тонкий и  меньше 30 мВ, упругие свойства диффузного слоя невелики, и поэтому при столкновении мицелл происходит перекрывание этих слоев, что приводит к преобладанию сил притяжения и потере агрегативной устойчивости. Таким образом, коллоидные растворы с ионным стабилизатором агрегативно неустойчивы, если их мицеллы имеют
меньше 30 мВ, упругие свойства диффузного слоя невелики, и поэтому при столкновении мицелл происходит перекрывание этих слоев, что приводит к преобладанию сил притяжения и потере агрегативной устойчивости. Таким образом, коллоидные растворы с ионным стабилизатором агрегативно неустойчивы, если их мицеллы имеют  относительно устойчивы, если
относительно устойчивы, если  и устойчивы, если
и устойчивы, если 
Коагуляция. Лиофобные коллоидные растворы, как термодинамически неустойчивые системы, могут разрушаться самопроизвольно или под влиянием внешних воздействий. Разрушение коллоидных растворов начинается с их коагуляции.
Коагуляцией называется процесс слипания коллоидных частиц с образованием более крупных агрегатов из-за потери коллоидным раствором агрегативной устойчивости.
В результате коагуляции укрупненные частицы дисперсной фазы легко седиментируют, и происходит расслоение системы. Таким образом, причиной коагуляции является потеря агрегативной устойчивости коллоидным раствором, а следствием коагуляции - уменьшение его седиментационной устойчивости.
Практически коагуляцию можно вызвать различными внешними воздействиями: добавлением небольших количеств электролита, концентрированием коллоидного раствора, изменением температуры, действием ультразвука, электромагнитного поля и др.
Явление коагуляции лежит в основе многих патологических процессов, протекающих в живых системах. Коагуляция коллоидных растворов фосфата кальция и холестерина в крови приводит к образованию осадков и отложению их на внутренней поверхности кровеносных сосудов (склеротические изменения сосудов).
Коагуляция проявляется в процессе свертывания крови. Свертывание крови играет в организме две противоположные роли: с одной стороны, уменьшает потерю крови при повреждении ткани, с другой - вызывает образование тромбов в кровеносной системе. Свертывание крови - очень сложный ферментативный процесс. Одновременно в крови действует антисвертывающая система, основой которой является гепарин - антикоагулянт крови.
Природу крови необходимо учитывать при ее консервировании. Так как свертыванию крови способствуют катионы кальция, то их удаляют из крови, предназначенной для консервирования, используя различные физико-химические способы. Например, добавка цитрата натрия переводит кальций в осадок, после чего кровь сохраняется в охлажденном состоянии, оставаясь пригодной для переливания в течение 30 суток. Цельную кровь можно декальцинировать также методом ионообмена, используя для этого Na-катиониты.
Коагуляция под действием электролитов. В биологических системах наибольшее практическое значение имеет коагуляция при добавлении небольших количеств электролита, поскольку коллоидные растворы клеток и биологических жидкостей находятся в соприкосновении с электролитами. Коагуляцию коллоидного раствора может вызвать любой электролит. Однако для каждого электролита необходима своя минимальная концентрация, называемая порогом коагуляции (спк).
Порогом коагуляции называется минимальное количество электролита, которое надо добавить к коллоидному раствору, чтобы вызвать явную коагуляцию (заметную на глаз) — помутнение раствора или изменение его окраски.
 |
Порог коагуляции можно рассчитать по формуле:
где сэл - исходная концентрация раствора электролита; V эл - объем раствора электролита, добавленного к коллоидному раствору; VKp -объем коллоидного раствора.
Величина, обратная порогу коагуляции, называется коагулирующим действием (у): 
Коагулирующее действие электролитов на коллоидные растворы с ионным стабилизатором подчиняется правилу Шульце -Гарди:
Коагуляцию коллоидных растворов вызывают любые ионы, которые имеют знак заряда, противоположный заряду гранул. Коагулирующее действие ионов (у) тем сильнее, чем выше заряд иона-коагулянта.
Коагулирующее действие иона-коагулянта прямо пропорционально его заряду в шестой степени: у = f(z6). Например, коагуляция золя AgI с отрицательно заряженными гранулами (потенциалопределяющие ионы - анионы I-) происходит за счет действия положительно заряженных ионов. Поэтому при добавлении к этому золю растворов NaCl, CaCl2, AICI3 коагулирующее действие катионов Na+, Са2+, А13+ будет резко возрастать; y(Na+): у(Са2+): у(Аl3+) = 1: 64: 729. Коагуляция золя Agl с положительно заряженными гранулами (потенциалопределяющие ионы -катионы Ag+), наоборот, идет за счет отрицательно заряженных ионов. Добавление к золю растворов КCl, K2SO4, Кз[Fе(СN)6] вызовет увеличение коагулирующего действия анионов в следующем порядке: у(Сl-): y(SO4(2-)): y[Fe(CN)6]3- = 1: 64: 729.
От правила Шульце - Гарди встречаются отклонения, поскольку на коагулирующее действие иона кроме заряда влияют радиус коагулирующего иона, а также природа иона, сопутствующего иону-коагулянту.
Сильное влияние электролита на коагуляцию коллоидных растворов следует учитывать при введении растворов солей в живые организмы. При этом имеет значение не только концентрация, но и заряд вводимых ионов. Так, физиологический раствор хлорида натрия (0,9 %) нельзя заменить изотоническим раствором сульфата магния, поскольку в этой соли имеются двухзарядные ионы Mg2+ и S04(2-), обладающие более высоким коагулирующим действием, чем ионы Na+ и Сl-.
При инъекциях электролита в мышечную ткань или кровь человека необходимо вводить его постепенно, медленно, чтобы не вызвать коагуляцию биологических коллоидных систем. Быстрое введение электролита из-за малой скорости диффузии его в крови или мышечной ткани приводит к накоплению электролита, локальному (местному) превышению его пороговой концентрации и вызывает коагуляцию биосубстратов, которую трудно остановить. При медленном введении электролит успевает уноситься с током крови и диффундировать в соседние ткани, поэтому пороговая концентрация не достигается и коагуляция не наступает. Это явление в живых тканях называется "привыканием".
Механизм коагуляции. Роль электролитов при коагуляции заключается в уменьшении расклинивающего давления между сближающимися коллоидными частицами. Это может происходить двумя путями: за счет уменьшения заряда поверхности твердой фазы (заряда поверхности ядра), т. е. за счет снижения межфазного потенциала Фмф, или за счет уменьшения толщины (сжатия) ионных атмосфер мицелл при неизменном заряде поверхности их ядер. В связи с этим возможны два вида коагуляции: нейтрализационная и концентрационная.
Нейтрализационная коагуляция наступает под действием электролита, который химически взаимодействует с потенциалопределяющими ионами, связывая их в прочное соединение (например, переводя в осадок) и тем самым уменьшая заряд поверхности ядра. Нейтрализационная коагуляция наблюдается, например, при добавлении K2S к коллоидному раствору AgI с положительно заряженными гранулами (потенциалопределяющие ионы - катионы Ag+). Между коагулирующими анионами S2- и потенциалопределяющими катионами Ag+ происходит реакция с образованием малорастворимого соединения Ag2S, что приводит к разрушению мицеллы AgI:

В результате связывания потенциалопределяющих катионов Ag+ межфазный потенциал фмф падает и число противоионов NO3(-), необходимых для компенсации заряда поверхности ядра, уменьшается. Таким образом, ионные атмосферы вокруг ядер становятся тоньше, снижается расклинивающее давление между сближающимися частицами, а это в свою очередь приводит к их слипанию в более крупные агрегаты.
Концентрационная коагуляция наступает под действием электролита, который химически не взаимодействует с ионами стабилизатора и не изменяет заряд поверхности ядра мицеллы. Однако в этом случае коагулирующее действие проявляют те ионы добавленного электролита, которые являются противоионами для данных мицелл, так как за счет повышения их концентрации они проникают внутрь гранулы, сжимая (уплотняя) ионную атмосферу мицеллы вокруг ядра. Концентрационная коагуляция происходит при неизменном межфазном потенциале фмф, но сопровождается, как правило, уменьшением  . Концентрационная коагуляция наблюдается, например, при добавлении нитратов к коллоидному раствору AgI, мицеллы которого содержат противоионы N03(-):
. Концентрационная коагуляция наблюдается, например, при добавлении нитратов к коллоидному раствору AgI, мицеллы которого содержат противоионы N03(-):

По мере увеличения концентрации добавляемых ионов NO3(-) они способствуют внедрению противоионов диффузного слоя в адсорбционный слой. При этом диффузный слой сжимается, и может наступить такое состояние, при котором диффузный слой исчезнет вовсе и гранула станет электронейтральной. В таком состоянии расклинивающее давление между сближающимися частицами минимально, и это приводит к слипанию частиц в более крупные агрегаты.
Поскольку заряд гранул в этих условиях равен 0, то в электрическом поле они не приобретают направленного движения к электродам, так как гранула находится в изоэлектрическом состоянии.
Изоэлектрическим состоянием называется состояние коллоидных частиц, при котором электрокинетический потенциал  равен 0 и которое характеризуется отсутствием направленного движения гранул в электрическом поле.
равен 0 и которое характеризуется отсутствием направленного движения гранул в электрическом поле.
В агрегативно устойчивом состоянии коллоидного раствора значение  колеблется в пределах 50-70 мВ. При уменьшении
колеблется в пределах 50-70 мВ. При уменьшении  под действием электролита до 25-30 мВ в системе не наблюдается никаких внешних изменений (помутнения или изменения окраски), так как скорость коагуляции еще очень низкая, вследствие чего эта стадия (I) коагуляции называется "скрытой" коагуляцией (рис. 27.5). Дальнейшее добавление электролита свыше Спк вызывает еще большее сжатие диффузного слоя и уменьшение
под действием электролита до 25-30 мВ в системе не наблюдается никаких внешних изменений (помутнения или изменения окраски), так как скорость коагуляции еще очень низкая, вследствие чего эта стадия (I) коагуляции называется "скрытой" коагуляцией (рис. 27.5). Дальнейшее добавление электролита свыше Спк вызывает еще большее сжатие диффузного слоя и уменьшение  , что сопровождается помутнением раствора, и начинается "явная" коагуляция. Вначале скорость коагуляции быстро увеличивается (стадия II), а затем становится постоянной, когда значение
, что сопровождается помутнением раствора, и начинается "явная" коагуляция. Вначале скорость коагуляции быстро увеличивается (стадия II), а затем становится постоянной, когда значение  станет равным нулю и наступит стадия быстрой коагуляции (III).
станет равным нулю и наступит стадия быстрой коагуляции (III).
Коагуляция смесями электролитов. На практике коагуляция часто вызывается действием смеси электролитов. При этом существует три возможных варианта взаимодействия между электролитами: аддитивное действие, антагонизм и синергизм.
 |
Рис. 27.5. Влияние концентрации электролита на скорость коагуляции
Аддитивность - это суммирование коагулирующего действия ионов, вызывающих коагуляцию.
Аддитивное действие проявляется в тех случаях, когда электролиты, содержащие коагулирующие ионы, не взаимодействуют химически между собой. Например, смесь солей КСl и NaN03 проявляет аддитивное действие по отношению к коллоидным растворам как с отрицательно, так и с положительно заряженными гранулами. В первом случае коагуляцию вызывают катионы К+ и Na+, во втором - анионы Сl- и NO3(-).
Антагонизм - это ослабление коагулирующего действия одного электролита в присутствии другого.
 |
Антагонизм действия наблюдается в тех случаях, когда в результате химической реакции между электролитами коагулирующие ионы связываются в нерастворимое соединение (выпадают в осадок) либо в прочный комплекс, который не обладает коагулирующей способностью. Например, коагулирующее действие катионов РЬ2+ по отношению к отрицательно заряженным гранулам ослабляется в присутствии NaCl, так как протекает реакция, в результате которой уменьшается концентрация коагулирующих ионов Рb2+ в растворе из-за выпадения в осадок РbСl2:
Синергизм — это усиление коагулирующего действия одного электролита в присутствии другого.
Синергизм действия возможен, когда между электролитами происходит химическое взаимодействие, в результате которого образуется многозарядный ион, обладающий очень высокой коагулирующей способностью. Например, коагулирующее действие FeCl3 и KCNS по отношению к положительно заряженным гранулам (коагулирующие ионы Сl(-) и CNS-) усиливается во много раз, так как происходит реакция, в результате которой образуются многозарядные анионы [Fe(CNS)6]3-, проявляющие высокую коагулирующую способность:

Используя электролиты в лабораторной и медико-санитарной практике, необходимо всегда учитывать возможность коагуляции в биологических средах. Так, при введении различных лекарственных веществ в организм (в виде инъекций) следует предварительно убедиться в том, что эти вещества не являются синергистами, чтобы избежать возможной коагуляции. С другой стороны, при очистке промышленных вод вредным может оказаться антагонизм вводимых электролитов, препятствующий разрушению коллоидных загрязнений.
Гетерокоагуляция, взаимная коагуляция. В природных водах, как и в промышленных сточных водах, коагуляция нередко происходит в результате смешивания дисперсных систем, содержащих разнородные частицы.
Гетерокоагуляцией называется коагуляция коллоидных растворов, содержащих разнородные частицы, отличающиеся по химической природе, знаку или величине заряда.
Частным случаем гетерокоагуляции является взаимная коагуляция — слипание разноименно заряженных гранул коллоидных растворов. При этом коагуляция происходит тем полнее, чем полнее нейтрализуются заряды гранул.
Гетерокоагуляции широко используется на практике в связи с проблемой очистки природных и промышленных вод. В воду, содержащую коллоидные примеси, добавляют соли алюминия или железа(3), которые являются хорошими коагулянтами. Эти соли в результате гидролиза дают малорастворимые гидроксиды Аl(ОН)3 или Fe(OH)3, образующие коллоидные растворы с положительно заряженными гранулами. В результате происходит коагуляция, сопровождающаяся образованием хлопьев из агрегированных разнородных мицелл, которые выпадают в осадок.
Пептизация. В процессе коагуляции, связанной с потерей агрегативной устойчивости, происходит разрушение коллоидного раствора, сопровождающееся выпадением осадка - коагулята. Однако, если коагуляту возвратить агрегативную устойчивость, то может произойти обратный процесс - пептизация.
Пептизацией называется процесс, обратный коагуляции - превращение осадка, образовавшегося в результате коагуляции, в устойчивый коллоидный раствор.
Пептизация может проводиться двумя путями, каждый из которых приводит к увеличению агрегативной устойчивости за счет восстановления достаточно рыхлых ионных атмосфер у мицелл:
- промыванием коагулята чистым растворителем (дисперсионной средой), что приводит к вымыванию из системы ионов, вызвавших коагуляцию, и разрыхлению ионных атмосфер вокруг частиц;
- добавлением специального электролита-пептизатора, ионы которого, адсорбируясь на поверхности частиц коагулята, восстанавливают рыхлые ионные атмосферы вокруг этих частиц и способствуют переходу их в коллоидное состояние.
Однако не всякий полученный при коагуляции осадок поддается пептизации. Важнейшие условия эффективной пептизации заключаются в следующем:
- к пептизации способны только свежеполученные осадки, так как увеличение продолжительности контакта частиц дисперсной фазы между собой приводит к постепенному уплотнению осадка и вытеснению жидкой фазы из его структуры;
- необходимо добавление небольших количеств электролита-пептизатора, в ином случае может вновь наступить коагуляция;
- пептизации способствуют перемешивание и нагревание.
Процесс пептизации лежит в основе лечения ряда патологических изменений в организме человека: рассасывания атеросклеротических бляшек на стенках кровеносных сосудов, почечных и печеночных камней или тромбов в кровеносных сосудах под действием антикоагулянтов. При этом необходимо учитывать своевременность введения лекарственных веществ (антикоагулянтов) в кровь: застарелые тромбы в кровеносных сосудах, а также уплотнившиеся камни практически не пептизируются, т. е. не рассасываются.
Дата публикования: 2014-10-16; Прочитано: 4008 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
