 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Квантовая теория атома водорода
|
|
34.1. Модель атома Резерфорда-Бора
Резерфорд предложил ядерную(планетарную) модель атома. Согласно этой модели, вокруг положительного ядра, имеющего заряд Ζе (Ζ — порядковый номер элемента в системе Менделеева, е — элементарный заряд), размер 10-15 – 10-14 м и массу, практически равную массе атома. В области с линейными размерами порядка 10-10 м по замкнутым орбитам движутся электроны, образуя электронную оболочку атома. Так как атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т. е. вокруг ядра должно вращаться Ζ электронов.
Считаем, что электрон движется вокруг ядра по круговой орбите радиуса r. При этом кулоновская сила взаимодействия между ядром и электроном сообщает электрону центростремительное ускорение. Второй закон Ньютона для электрона, движущегося по окружности под действием кулоновской силы, имеет вид:
 =
=  , (34.1)
, (34.1)
где mе, и υ — масса и скорость электрона на орбите радиуса r, ε 0 — электрическая постоянная.
Уравнение (34.1) содержит два неизвестных: r и υ. Следовательно, существует бесчисленное множество значений радиуса и соответствующих ему значений скорости а значит, и энергии, удовлетворяющих этому уравнению. Поэтому величины r, υ (следовательно, и Е) могут меняться непрерывно, т. е. может испускаться любая, а не вполне определенная порция энергии. Тогда спектры атомов должны быть сплошными. В действительности же опыт показывает, что атомы имеют линейчатый спектр. Из выражения (34.1) следует, что при r ~10-10 м скорость движения электронов - υ ~106 м/с, а ускорение ~ 1022 м/с2. Согласно классической электродинамике, ускоренно движущиеся электроны должны излучать электромагнитные волны и вследствие этого непрерывно терять энергию. В результате электроны будут приближаться к ядру и, в конце концов, упадут на него. Таким образом, атом Резерфорда оказывается неустойчивой системой, что опять-таки противоречит действительности.
Попытки построить модель атома в рамках классической физики не привели к успеху. Преодоление возникших трудностей потребовало создания качественно новой — квантовой— теории атома.
Исследования спектров излучения разреженных газов (т. е. спектров излучения отдельных атомов) показали, что каждому газу присущ определенный линейчатый спектр, состоящий из отдельных спектральных линий или групп близко расположенных линий. Самым изученным является спектр наиболее простого атома — атома водорода.
И. Бальмер подобрал эмпирическую формулу, описывающую все известные в то время спектральные линии атома водорода в видимой области спектра:
ν = R  (n =3, 4, 5,...), (34.2)
(n =3, 4, 5,...), (34.2)
где R =3,29×1015 с-1 —постоянная Ридберга.
Из выражения (34.2) вытекает, что спектральные линии, отличающиеся различными значениями п, образуют группу или серию линий, называемую серией Бальмера.
В спектре атома водорода было обнаружено еще несколько серий.
В ультрафиолетовой области спектра находится серия Лаймана:
ν= R  (n =2, 3, 4, 5,...),
(n =2, 3, 4, 5,...),
В инфракрасной области спектра были также обнаружены:
Серия Пашена ν = R 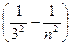 (n = 4, 5, 6,...),
(n = 4, 5, 6,...),
Серия Брэкета ν = R 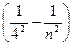 (n = 5, 6, 7,...),
(n = 5, 6, 7,...),
Серия Пфунда ν = R 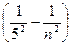 (n = 6, 7, 8,...),
(n = 6, 7, 8,...),
Серия Хэмфри ν = R  (n = 7, 8, 9,...),
(n = 7, 8, 9,...),
Все приведенные выше серии в спектре атома водорода могут быть описаны одной формулой, называемой обобщенной формулой Бальмера:
ν = R  , (34.3)
, (34.3)
где т имеет в каждой данной серии постоянное значение, т = 1, 2, 3, 4, 5, 6 (определяет серию), п принимает целочисленные значения начиная с т+ 1 (определяет отдельные линии этой серии).
Приведенные выше сериальные формулы подобраны эмпирически и долгое время не имели теоретического обоснования, хотя и были подтверждены экспериментально с очень большой точностью.
Дата публикования: 2014-10-04; Прочитано: 1492 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
