 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Решение. В данном способе титрования к определяемому раствору добавляется известный избыток титранта (I)
|
|
В данном способе титрования к определяемому раствору добавляется известный избыток титранта (I). Затем избыток непрореагировавшего титранта (I) оттитровывают титрантом (II). Закон эквивалентов для обратного титрования имеет вид:
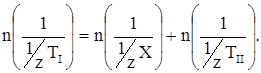
Фактор эквивалентности аммиака в реакциях кислотно-основного взаимодействия равен единице.
М(NH3) = 17,03 г/моль.
Записываем закон эквивалентов:
n(KOH) = n(NH3) + n(1/2H2SO4)(NH3) = C(KOH)∙V(KOH)∙10-3 - C(1/2H2SO4)∙V(H2SO4)∙10-3
10-3 - пересчет объемов титрантов в литры.(NH3) = (0,1150 моль/л ∙ 30,00∙10-3 л - 0,1050 моль/л ∙ 6,30∙10-3)∙17,03 г/моль = 0,04748 г

Тема III. Кислотно-основное титрование. Определение точки эквивалентности. Расчет кривых титрования сильных и слабых кислот и оснований. Титрование солей. Индикаторы, применяемые в методе кислотно-основного титрования, их выбор. Количественные расчеты.
В основе кислотно-основного титрования лежит реакция нейтрализации, и в процессе титрования изменяется рН раствора. Поэтому при изучении данной темы необходимо уметь правильно определять состав раствора и рассчитывать рН в ходе титрования. Для правильного выбора индикатора важно знать, что такое точка эквивалентности, скачок рН, точка начала скачка и конца, чем определяется величина скачка рН, что такое интервал перехода окраски индикатора и его показатель титрования - рТ.
Пример 1. Рассчитать скачок титрования 10,00 мл 0,2 М раствора NaOH 0,1 М раствором HCl. Скачок титрования определяется в пределах 0,1% между недостатком и избытком титранта от эквивалентного количества.
В точке начала скачка раствор NaOH недотитрован на 0,1%, т.е. нейтрализация проведена на 99,9%. Рассчитаем добавленный объем HCl в точке начала скачка. Эквивалентный объем HCl равен:
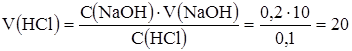 мл
мл
мл - 100%
V(HCl) - 99,9%
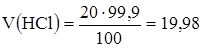 мл.
мл.
Концентрация неоттитрованного количества NaOH:

рОН = -lg[OH-] = 4,17= 14 - 4,17 = 9,83.
В точке конца скачка титрования раствор перетитрован на 0,1%.
Объем добавленной HCl, очевидно, равен 20,02 мл
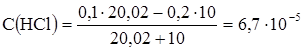
рН = 4,17.
Ответ: скачок титрования лежит в пределах от 9,83 до 4,17.
Пример 2. Рассчитать рН в точке эквивалентности и скачок титрования 20 мл 0,1 М раствора муравьиной кислоты (КHCOOH = 1,8∙10-4) 0,2 М раствором KOH. Подобрать индикатор.
Дата публикования: 2014-11-18; Прочитано: 677 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
