 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Пример 3. При построении калибровочного графика для винной кислоты были получены следующие данные на клиновом поляриметре:
|
|
При построении калибровочного графика для винной кислоты были получены следующие данные на клиновом поляриметре:
| Концентрация винной кислоты, % | ||||
| Показания поляриметра, мм | 9,9 | 19,1 | 27,3 | 34,9 |
Сколько граммов винной кислоты надо растворить в 250 мл воды, чтобы отсчет по шкале был 23,5 мм.
Решение: строим график зависимости концентрации винной кислоты (%) от отсчета по шкале.
Для 23,5 мм по графику находим w = 24,7% и рассчитываем навеску винной кислоты (g):
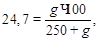 отсюда
отсюда  г.
г.
4. Потенциометрический метод анализа
Решение задач сводится к трем типам расчетов:
1. Расчет равновесного напряжения гальваноцепи, состоящей из электрода сравнения с постоянным потенциалом и индикаторного электрода (электрода измерения) с переменным потенциалом, зависящим от концентрации вещества в растворе.
В качестве электрода сравнения используют стандартный водородный электрод Pt½H2½2H+, каломельный Hg(ж)½Hg2Cl2(к)½KCl или хлорсеребряный Ag ½AgCl(к)½KCl электроды.
Электрод с меньшей величиной электродного потенциала играет роль анода. На аноде идет процесс окисления. На другом электроде с большим значением электродного потенциала – катоде идет процесс восстановления.
Е = Е (+) – Е (–),
где Е – напряжение, Е (+)и Е (–) – электродные потенциалы катода и анода соответственно.
2. Расчет рН исследуемой системы, состоящей из таких же пар электродов, погруженных в раствор определяемого вещества.
3. Расчет либо содержания вещества в титруемом растворе, либо потенциала индикаторного электрода в различные моменты титрования. Такое титрование и расчеты возможны для реакций окисления–восстановления, образования и разрушения комплексных соединений, нейтрализации (кислотно-основное взаимодействие), которые сопровождаются изменением равновесного напряжения системы.
4.1. Вычисление электродных потенциалов и напряжения
Дата публикования: 2014-11-18; Прочитано: 1200 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
