 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Обработка полученных результатов
|
|
1. Определить постоянную калориметра. Для этого на миллиметровой бумаге построить график зависимости температуры от времени: Т = f(t) (рис. 10). Масштаб по оси абсцисс: 1 мин = 1 см. Масштаб по оси ординат: 0,1 0 = 1 см.
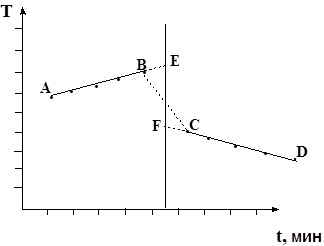
Рис. 10. График изменения температуры при растворении KCl.
Прямая АВ относится к начальному периоду, ВС – к главному, СD – конечному периоду. Точка В – последний отсчет начального периода, точка С – первый отсчет конечного периода. Через середину отрезка ВС провести перпендикуляр в оси абсцисс. Продолжить прямые АВ и CD до пересечением с перпендикуляром. Отрезок EF будет характеризовать действительное изменение температуры в опыте, т.е. ∆T. Крутизна наклона прямых АВ и CD зависит от характера теплообмена с окружающей средой. Определив ∆T, рассчитать постоянную калориметра W по уравнению 5.5:
 (5.5)
(5.5)
где m1 и m2 – масса воды и растворяемой соли соответственно; ∆H – молярная теплота растворения соли (для KCl ∆H = 18 841 Дж/моль); М – молярная масса растворяемой соли; С – удельная теплоемкость раствора (для раствора KCl С = 4,103 Дж/г·К).
2. Найти изменение температуры для суспензии исследуемого адсорбента ∆T расчетным способом:
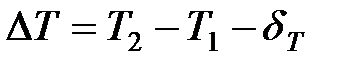 (5.6)
(5.6)
где Т2 – последний отсчет главного периода; Т1 – последний отсчет начального периода; δТ – поправка на потерю тепла в окружающую среду.
Поправку δТ рассчитать по уравнению Щукарева (5.7):
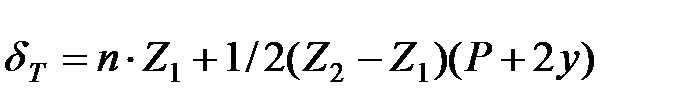 (5.7)
(5.7)
где n - общее число интервалов главного периода;
Z1 – среднее изменение температуры между двумя отсчетами в начальном периоде (разность первого и последнего отсчета, деленная на число измерений);
Z2 – среднее изменение температуры между двумя отсчетами в конечном периоде (разность первого и последнего отсчета, деленная на число измерений);
Р – число первых интервалов главного периода, когда температура растет быстро (не менее 0,003 0);
y – число остальных измерений главного периода, когда температура растет медленно.
Если в конечном периоде температура не падает, а повышается, то Z2 становится отрицательной величиной. Если температура в конечном периоде не изменяется, то Z2 = 0.
3. Рассчитать удельную теплоту смачивания Q по уравнению (5.8):
 (5.8)
(5.8)
где W – постоянная калориметра; m1 и m2 – масса воды и исследуемого образца соответственно; С – удельная теплоемкость исследуемого вещества.
4. Рассчитать теплоту смачивания 1 м2 поверхности твердого тела q водой по уравнению 5.3 используя справочные данные, приведенные ниже.
5. Найти удельную поверхность исследуемого адсорбента, используя уравнение 5.4.
Таблица 5.1
Поверхностное натяжение воды на границе с воздухом при различных температурах
| Температура, оС | s . 103, н/м | Температура, оС | s . 103, н/м |
| 74,22. | 72,59 | ||
| 74,07 | 72,44 | ||
| 73,93 | 72,28 | ||
| 73,78 | 72,13 | ||
| 73,64 | 71,97 | ||
| 73,49 | 71,82 | ||
| 73,34 | 71,66 | ||
| 73,19 | 71,50 | ||
| 73,05 | 71,35 | ||
| 72,90 | 71,18 | ||
| 72,75 | 70,38 |
Таблица 5.2
Удельные теплоемкости
| № | Вещество | С, Дж/г×К |
| Al2O3 | 0,774 | |
| SiO2 | 0,741 |
Контрольные вопросы и задания
1. Чем обусловлен тепловой эффект смачивания?
2. Что такое дифференциальная теплота смачивания?
3. Что такое интегральная теплота смачивания?
4. Для чего и в каком случае используют показатель теплоты смачивания?
5. Физический смысл термического коэффициента смачивания.
Дата публикования: 2014-11-19; Прочитано: 773 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
