 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Определение теплоты смачивания
|
|
Цель работы: определить теплоту смачивания водой адсорбентов и вычислить их удельную поверхность.
Приборы и реактивы: калориметр (1 шт.), механическая мешалка (1 шт.), термометр Бекмана (1 шт.), секундомер, плоскодонная колба емкостью на 500 мл (1 шт), стакан емкостью на 1 л (1шт.), цилиндр на 500 мл (1 шт), KCl, вода, адсорбенты.
Смачивание твердой поверхности какой-либо жидкостью сопровождается обычно выделением теплоты, вызываемым действием межмолекулярных сил твердой смачиваемой поверхности и смачивающей жидкости. Особенно заметно выделение тепла при смачивании пористых или высокодисперсных тел, обладающих большой поверхностью.
Теплота, выделяющаяся при смачивании 1 г вещества жидкостью, называется интегральной теплотой смачивания или просто теплотой смачивания.
Величина теплоты смачивания зависит от природы жидкости и твердого тела, а также от величины его смачивающей поверхности. Вещества, которые хорошо смачиваются водой и выделяют при этом большое количество теплоты, чем при смачивании органическими жидкостями, называются гидрофильными. Вещества, которые плохо смачиваются водой, и большее количество теплоты выделяют при смачивании органическими жидкостями, чем водой, называются гидрофобными. Если отношение теплоты смачивания водой к теплоте смачивания бензолом больше единице, то вещество гидрофильное и наоборот.
Поверхностная энергия твердого тела после смачивания уменьшается на величину, равную поверхностной энергии смачивающей жидкости. За счет этого уменьшается и теплота смачивания. Величина теплоты смачивания 1 м2 поверхности твердого тела q выражается формулой 5.1:
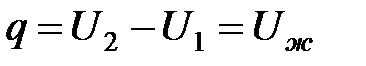 (5.1)
(5.1)
где U2 – полная поверхностная энергия смачиваемого тела на границе твердое тело – жидкость; U1 – полная поверхностная энергия смачиваемого тела на границе твердое тело – воздух; Uж – полная поверхностная энергия смачивающей жидкости на границе жидкость – газ.
Полная поверхностная энергия жидкости согласно уравнению Гиббса – Гельмгольца при T = const может быть выражена следующим образом:
 (5.2)
(5.2)
где σ - поверхностное натяжение жидкости,  - температурный коэффициент, который для воды равен –0,151·10-3 Дж/м2·К.
- температурный коэффициент, который для воды равен –0,151·10-3 Дж/м2·К.
Отсюда:
 (5.3)
(5.3)
Это уравнение справедливо для тех случаев, когда жидкость полностью смачивает твердую поверхность.
Поверхностное натяжение на границах твердое тело – газ, твердое тело – жидкость практически измерить невозможно, поэтому нельзя вычислить полную поверхностную энергию твердого тела до и после смачивания. Но можно найти полную поверхностную энергию смачивающей жидкости Uж, которая равна теплоте смачивания.
Теплота смачивания 1 г вещества Q (удельная теплота смачивания) имеет вид:
 (5.4)
(5.4)
где q – теплота смачивания 1 м2 поверхности (Дж/м2); S – удельная поверхность адсорбента (м2/г).
Теплоту смачивания находят экспериментально калориметрическим методом. Зная теплоту смачивания, можно рассчитать удельную поверхность адсорбента.
Порядок выполнения работы
1. Исследуемый адсорбент (по указанию преподавателя) поместить в фарфоровую чашечку и высушить в сушильном шкафу в течение 1-1,5 ч. Затем охладить в эксикаторе до комнатной температуры.
2. Установить термометр Бекмана в интервале между 2 и 3 0.
3. Взвесить 2 г хлорида калия.
4. В калориметр налить 200 мл воды и закрыть его крышкой с двумя отверстиями (для термометра Бекмана и мешалки). Погрузить термометр, опустить мешалку и включить перемешивание, постепенно увеличивая скорость, но не доводя до разбрызгивания воды. Термостатировать воду в течение 5 мин.
5. Как только изменение температуры станет равномерным начать отсчеты показаний термометра через 30 с в течение 5 мин.
6. После 10 отсчетов выключить мешалку, засыпать навеску хлорида калия и, включив мешалку, продолжить запись температуры через 30 с в течение 5 мин (время высыпания вещества не более 30 с). Результаты записать в таблицу:
Таблица
| № | Время от начала опыта, мин | Показания термометра для воды, град. | Время от начала опыта, мин | Показания термометра для раствора КСl, град. |
7. Взвесить 2 г исследуемого образца.
8. В калориметр налить 200 мл воды на 2-3 0С выше комнатной и закрыть его крышкой. Термометр и мешалку погрузить в воду, включить мешалку и дать установиться температуре всех частей калориметра. Термостатировать воду в течение 5 мин.
9. Как только изменение температуры станет равномерным начать отсчеты показаний термометра через 30 с в течение 5 мин. Это начальный период.
10. После 10 отсчетов выключить мешалку, засыпать навеску исследуемого вещества и, включив мешалку, продолжить запись температуры через 30 с (время высыпания вещества не более 30 с). С момента высыпания вещества начинается главный период, который продолжается до тех пор, пока наблюдается неравномерное повышение температуры. Как только начнется понижение температуры (или равномерное повышение), начинается конечный период, в котором тоже надо сделать 10 отсчетов. Результаты записать в таблицу:
Таблица
Дата публикования: 2014-11-19; Прочитано: 3516 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
