 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Химическое равновесие. Химические реакции бываютнеобратимыми и обратимыми
|
|
Химические реакции бывают необратимыми и обратимыми.
Необратимыми называют реакции, которые протекают только в одном направлении.
В частности, к необратимым реакциям относятся те, которые сопровождаются образованием осадка, газа или малодиссоциирующего вещества (например, Н2О).
Примеры:
BaCl2 + K2SO4 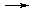 BaSO4¯ + 2KCl
BaSO4¯ + 2KCl
Na2CO3 + 2HCl 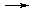 2NaCl + CO2 + H2O
2NaCl + CO2 + H2O
HCl + KOH 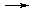 KCl + H2O
KCl + H2O
Необратимые реакции протекают до конца, т.е до полного израсходования одного из реагентов. Выход продукта в таких реакциях близок к 100%. Практика показывает, что таких реакций не так много.
Обратимыми называют реакции, которые одновременно протекают в двух противоположных направлениях.
Большинство реакций являются обратимыми. Такие реакции не протекают до конца и характеризуются выходом продукта, который всегда <100%. При записи подобных реакций вместо знака равенства пользуются противоположно направленными стрелками.
Примеры:
N2 + 3H2 ⇄ 2NH3
H2 + I2 ⇄ 2HI
2NO + O2 ⇄ 2NO2
Следует отметить, что полностью необратимых реакций в природе не существует. Для любого химического процесса можно подобрать такие условия, при которых он станет обратимым.
Дата публикования: 2014-11-18; Прочитано: 758 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
