 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Термодинамика равновесных процессов
|
|
Рассмотрим обратимую гомогенную реакцию, протекающую в закрытой системе при T = const и p = const, в общем виде:
aA + bB ⇄ cC + dD.
Изменение энергии Гиббса при протекании химической реакции можно определить по формуле:
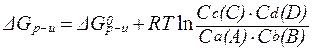
| (1) |
где c(A), c(B), c(C) и c(D) - текущие концентрации веществ.
Это уравнение называется изотермой химической реакции или уравнением изотермы Вант-Гоффа.
Согласно I постулату термодинамики в определенный момент система самопроизвольно достигнет равновесного состояния. Такое состояние называют химическим равновесием.
Химическое равновесие - это динамическое состояние системы, которое характеризуется:
1. Энергетической выгодностью, т.е. минимальным значением и отсутствием изменений энергии Гиббса (G = Gmin, DG = 0).
2. Постоянством параметров и функций состояния, в том числе концентраций исходных веществ и продуктов реакции. Концентрации веществ, которые устанавливаются при химическом равновесии, называются равновесными концентрациями и обозначаются квадратными скобками, например [A].
Поскольку в состоянии химического равновесия DG = 0, можем записать:
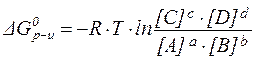
При постоянстве внешних условий подлогорифмическое отношение равновесных концентраций является величиной постоянной и называется константой равновесия K.
Тогда:

| (2) |
Заменив натуральный логарифм на десятичный и подставив значение R = 8,31×10-3 кДж/моль×К, получим:

| (3) |
Это уравнение позволяет производить расчет изменения энергии Гиббса при протекании химической реакции, а также расчет константы химического равновесия при различных температурах:
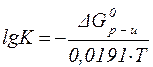
| (4) |
Последнее соотношение позволяет определить равновесный состав системы.
Если  << 0, то К >> 1 и равновесие устанавливается при практически полном стехиометрическом израсходовании исходных веществ.
<< 0, то К >> 1 и равновесие устанавливается при практически полном стехиометрическом израсходовании исходных веществ.
Если  >> 0, то К << 1 и исходные вещества практически не взаимодействуют друг с другом.
>> 0, то К << 1 и исходные вещества практически не взаимодействуют друг с другом.
Дата публикования: 2014-11-18; Прочитано: 444 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
