 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Механизмы протекания химических реакций
|
|
Механизмом химической реакции называют последовательность и характер стадий реакции. В соответствии с механизмом различают простые и сложные реакции.
Простыми (элементарными) называют реакции, протекающие в одну стадию. К простым реакциям относят диссоциацию большинства двухатомных молекул. Например: Br2 = 2Br.
Сложные реакции протекают в несколько стадий. Среди сложных реакций различают: конкурирующие, последовательные, сопряженные, обратимые, цепные, фотохимические и др.
1. Конкурирующие реакции можно схематично записать так:
A + B1 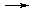 X1
X1
A + B2 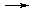 X2
X2
Например: при нитровании фенола одновременно протекают два процесса – образование орто- и пара-нитрофенола.
2. Последовательные реакции можно записать в виде:
A 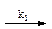 B
B 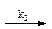 C.
C.
Примером является реакция гидролиза соли, образованной многоосновной кислотой или многокислотным основанием:
Na2CO3 + H2O = NaHCO3 + NaOH; (k1);
NaHCO3 + H2O = H2CO3 + NaOH; (k2).
Биохимические реакции в организме человека в большинстве случаев являются последовательными. Например, глюкоза, поступающая в организм, в процессе окисления превращаясь в пировиноградную кислоту, претерпевает девять последовательных превращений (процесс гликолиза).
3. Сопряженные реакции отвечают общей схеме:
a) A + B 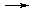 M;
M;
b) A + C 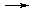 N.
N.
При этом реакция (а) может протекать самостоятельно, тогда как реакция (b) протекает только при наличии реакции (а).
4. Обратимые реакции. Большинство реакций в той или иной степени обратимы, поэтому следует учитывать как прямую, так и обратную реакцию:
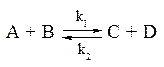
Например, обратимой является реакция образования аммиака:
N2 + 3H2 ⇄ 2NH3.
Скорость прямой реакции убывает с течением времени, а скорость обратной реакции возрастает до момента выравнивания обеих скоростей, когда наступит состояние подвижного химического равновесия.
Если скорость реакции в прямом направлении значительно превышает скорость обратного процесса, то считают, что реакция протекает практически до конца.
5. Цепные реакции - это реакции, протекающие с участием химически активных частиц (свободных атомов и радикалов) и состоящие из большого количества повторяющихся стадий.
Образование свободных радикалов, необходимых для начала цепной реакции, происходит при разрыве связей в молекуле и всегда бывает сопряжено с затратой энергии, которая может быть получена:
а) при поглощении молекулой кванта света:
Br2 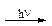 Br• + Br•;
Br• + Br•;
б) при электрическом разряде:
O2 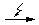 O• + O•;
O• + O•;
в) под воздействием a-, b-, g-излучений (радиоактивный распад);
г) при использовании внутренней тепловой энергии самой системы.
Радикалы, вследствие своей валентной ненасыщенности и высокой химической активности, существуют лишь очень недолго, но они переводят устойчивые молекулы в активное состояние. Начавшаяся цепная реакция продолжается до тех пор, пока не прореагирует все вещество или пока активные частицы по каким-либо причинам не исчезнут. Роль активных радикалов могут играть атомы водорода, хлора, кислорода и группы: СН3–, –ОН, –SH, С6Н5– и др.
По механизму протекания цепных реакций они делятся на неразветвленные и разветвленные.
К неразветвленным цепным реакциям относятся реакции синтеза HCl(газ); НВr(газ) и другие, протекающие, например, под действием света:
H2 + Cl2 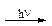 2HCl(газ).
2HCl(газ).
Примером разветвленной цепной реакции, когда расход одной или нескольких активных частиц приводит к образованию значительно большего количества таких частиц, является реакция горения водорода (рис. 1).
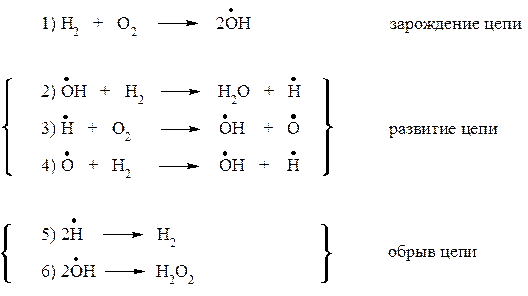
Рис. 1. Схема цепной реакции горения водорода.
Для зарождения цепи необходима высокая температура. Особенность развития цепи в данной реакции состоит в том, что поглощение одного радикала 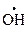 , первоначально необходимого для совершения этой группы реакций, приводит затем к образованию трех радикалов /
, первоначально необходимого для совершения этой группы реакций, приводит затем к образованию трех радикалов / 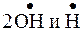 /.
/.
Актуальным является изучение цепных реакций, возникающих в организме человека при воздействии проникающей радиации, так как образующиеся радикалы способны оказывать воздействие на биологические макромолекулы (ДНК, РНК и др.), что, в свою очередь, вызывает мутации и приводит к наследственным заболеваниям.
6. Фотохимическими называются реакции, которые протекают только при наличии излучения в широком интервале энергий: от видимого и ультрафиолетового до рентгеновского и g-лучей.
Энергия активации здесь обеспечивается за счет излучения, под действием которого молекулы исходных веществ переходят в электронно-возбужденное состояние.
Механизмы фотохимических реакций разнообразны. Несмотря на это, во всех случаях можно выделить первичные процессы, непосредственно вызываемые действием света, и вторичные реакции, не требующие освещения для своего протекания и называемые поэтому темными.
К первичным процессам относятся следующие:
1. Возбуждение молекул или атомов, в результате чего образуются менее устойчивые частицы, способные к дальнейшим превращениям:
M + hn 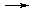 M*.
M*.
2. Диссоциация молекул на атомы или радикалы (фотолиз):
AB + hn 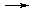 A + B.
A + B.
3. Ионизация молекул или атомов с выделением электрона (фотоэффект):
M + hn 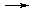 M+ + e.
M+ + e.
Фотохимические реакции подчиняются следующим законам:
I закон фотохимии:
Химически активным является лишь то излучение, которое поглощается реакционной смесью.
II закон фотохимии:
Каждый поглощенный квант света вызывает превращение одной молекулы.
Фотохимические реакции отличаются слабой зависимостью скорости реакции от температуры. Это объясняется тем, что в первичных реакциях за счет поглощения света приобретается настолько большая энергия, что повышение температуры может изменить ее лишь незначительно.
Дата публикования: 2014-11-18; Прочитано: 3599 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
