 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Реакции I порядка
|
|
Для реакций I порядка убыль концентрации реагента определяется уравнением:
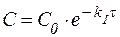
| (8) |
где С – концентрация вещества в данный момент времени;
С0 – начальная концентрация вещества;
kI – константа скорости реакции первого порядка;
t – время.
В логарифмической форме это выражение выглядит так:
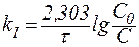
| (9) |
Из приведенных формул можно сделать ряд важных заключений:
1) константа скорости реакции первого порядка имеет размерность [время-1] и может быть выражена в обратных секундах, минутах, часах и т. д.;
2) величина kI не зависит от способа выражения концентрации реагента;
3) в реакциях первого порядка одинаковым промежуткам времени отвечают одинаковые доли прореагировавшего вещества.
Последнее утверждение позволяет ввести понятие период полупревращения.
Периодом полупревращения (t1/2) называют время, необходимое для превращения половины первоначального количества вещества.
Таким образом, в момент времени t = t1/2 количество непрореагировавшего вещества составляет 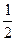 С0. В этом случае:
С0. В этом случае:
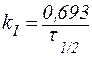 . .
| (10) |
Из данной формулы следует, что в реакциях первого порядка период полупревращения не зависит от начальной концентрации реагента.
В некоторых случаях удобно использовать формулу:
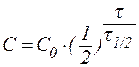 , ,
| (11) |
которая позволяет определить время, за которое превращению подвергнется определенное количество исходного вещества.
В организме человека процессы метаболизма лекарственных препаратов протекают, в основном, в соответствии с уравнением реакции первого порядка. Период, за который превращению подвергается половина действующего начала препарата называется периодом полувыведения или полуэлиминации. Зная величины kI и t1/2, можно рассчитать оптимальные промежутки времени между приемами лекарственного средства.
Кинетические уравнения реакций различного порядка представлены в табл. 2.
Табл. 2. Кинетические уравнения реакций различного порядка.
| Порядок реакции | Кинетическое уравнение | Решение кинетического уравнения* | Период полупревращения |
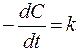
| 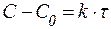
| 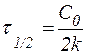
| |
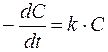
| 
| 
| |
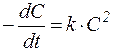
| 
| 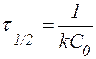
| |

| 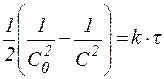
| 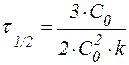
|
* при равных исходных концентрациях реагирующих веществ
Из приведенных уравнений следует, что для реакций различного порядка константы скорости имеют неодинаковые размерности. Действительно, константа скорости реакции второго порядка имеет размерность [л·моль-1·время-1)], третьего порядка - [л2·моль-2·время-1].
Таким образом, сравнивать значения констант скорости реакций различного порядка нельзя.
Дата публикования: 2014-11-18; Прочитано: 462 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
