 |
Главная Случайная страница Контакты | Мы поможем в написании вашей работы! | |
Химические свойства циклоалканов
|
|
По многим свойствам циклоалканы похожи на алканы. Они также вступают в реакции замещения с галогенами, нитруются азотной кислотой.
Наиболее устойчивым среди голоядерных циклоалканов является циклогексан. В отличие от других циклоаканов, не имеющих заместителей, его молекула не является плоской и в ней отсутствует напряжение – и это при небольшом отклонении от Байеровского угла (109о 28//) между двумя валентностями sp 3-гибридизованного атома углерода, которое составляет у циклогексана – 5о16//. Для сравнения это отклонение у циклопентана составляет + 44//, у циклобутана + 9о 44//, циклопропана даже + 24о 44//. Последние три молекулы являются плоскими. Как следствие, теплота сгорания в пересчете на одну группу - СН2 - у циклогексана наименьшая и составляет 659,03 кДж/моль, что почти равно теплоте сгорания, приходящейся на одну группу -СН2- у алканов.
5.2.1. Реакции изомеризации. Пятичленные цикланы могут превращаться в шестичленные в присутствии катализаторов кислотного типа, подобного AlCl 3 или AlBr3. При этом расширение цикла идет за счет включения в него  -углеродного атома:
-углеродного атома:
 | |||
 | |||





 С R R R. (5.1)
С R R R. (5.1)
 |
Эта реакция используется для получения ценного сырья – циклогексана. Как видно из уравнения (5.1), реакция может быть обратимой при определенных условиях. Такой тип изомеризации называют структурной скелетной с изменением цикла. Существуют и другие виды изомеризации циклоалканов.
Структурная скелетная без изменения цикла:


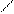
 СН3
СН3
 СН3
СН3
 . (5.2)
. (5.2)




 СН2СН3 СН3 СН3
СН2СН3 СН3 СН3
 |
Пространственная геометрическая (цис – транс) изомерия:


 СН3
СН3
 |  | ||

 . (5.3)
. (5.3)
СН3 СН3 СН3
5.2.2. Реакция дегидрирования.  На бифункциональных катализаторах при 240 – 420 оС на гидрирующе-дегидрирующих центрах металлических катализаторов (Pt, Ni, Pd) образуются циклоалкены, а на кислотных центрах (Al2O3) – карбкатионы:
На бифункциональных катализаторах при 240 – 420 оС на гидрирующе-дегидрирующих центрах металлических катализаторов (Pt, Ni, Pd) образуются циклоалкены, а на кислотных центрах (Al2O3) – карбкатионы:
С С С


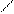
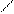
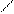



 М К К + К М
М К К + К М











 , (5.4)
, (5.4)


 - Н2 + Н2
- Н2 + Н2
- 3Н2
 |
где М – металлические центры;
К – кислотные центры.
5.2.3.Действие окислителей. Практическое применение имеют реакции для получения капрона и найлона через капролактам, последовательность которых приведена на рис. 5.1.
Окисление циклогексана проводят 35 - процентнойазотной кислотой при 120–125 оС и давлении 0,4–0,5 МПа и мольном соотношении кислоты к циклогексану 1,33:1. Нитроциклогексан восстанавливают в циклогексаноноксим водородом в среде аммиака на медном катализаторе при 80–130 оС, давлении 17 – 20 МПа с выходом оксима 85 – 90 %.
Окисление циклогексана кислородом воздуха ведут в жидкой фазе при 120–130 оС, давлении 1,5–2,0 МПа в присутствии нафтената Со или стеарата Мп. В конечном счете можно одновременно получать адипиновую кислоту и 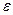 -капролактам.
-капролактам.

 HNO3, NxOy NO2
HNO3, NxOy NO2
 | |||||
 |  | ||||



 циклогексан
циклогексан


















 + О2 +H2 - H2O О ОН - Н2 циклогексанон + HNO3 циклогексанол NH2OH
+ О2 +H2 - H2O О ОН - Н2 циклогексанон + HNO3 циклогексанол NH2OH




 НО - N +[О] +NOCl + O2 - - НСl
НО - N +[О] +NOCl + O2 - - НСl


 оксим циклогексана НООС(СН2)4СООН
оксим циклогексана НООС(СН2)4СООН
адипиновая кислота
 | |||
 | |||
изомеризация +Н2SO4 + SO3 + NH3
300-390 оС, H3PO4
 NH NC(CH2)4CN
NH NC(CH2)4CN



 (СН2)5 адиподинитрил + C = O 80 – 100 оС
(СН2)5 адиподинитрил + C = O 80 – 100 оС
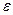 - капролактам + Н2; 4,9 – 7,8 МПа
- капролактам + Н2; 4,9 – 7,8 МПа



 - [- HN(CH2)5CO-]x- NH2 (CH2)6NH2 капрон (найлон 6) гексаметилендиамин
- [- HN(CH2)5CO-]x- NH2 (CH2)6NH2 капрон (найлон 6) гексаметилендиамин
-  [HN(CH2)6NHCO(CH2)4CO - ]x -
[HN(CH2)6NHCO(CH2)4CO - ]x -
анид (найлон 6,6)
Рис. 5.1. Схема переработки циклогексана в синтетические волокна
Получение 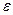 -капролактама путем нитрозирования циклогексана раствором нитрозилхлорида проводят путем облучения видимым светом с длиной волны 450 – 550 мкм и насыщения раствора хлороводородом:
-капролактама путем нитрозирования циклогексана раствором нитрозилхлорида проводят путем облучения видимым светом с длиной волны 450 – 550 мкм и насыщения раствора хлороводородом:

 NOCl + HCl
NOCl + HCl



 NOH
NOH  HCl. (5.5)
HCl. (5.5)
И далее хлоргидрат циклогексаноксима изомеризуют в капролактам.
5.2.4. Гидрирование циклоалканов. При каталитическом гидрировании трех-, четырех- и пятичленные циклы разрываются с образованием соответствующих алканов. Наиболее легко эта реакция протекает с циклопропаном и его гомологами. Пятичленный цикл разрывается только при высокой температуре.
 Рd
Рd

 + Н2 СН3 – СН2 – СН3; (5.6)
+ Н2 СН3 – СН2 – СН3; (5.6)
 Pd, 300 оС
Pd, 300 оС
 + Н2 СН3 – (СН2)3 – СН3. (5.7)
+ Н2 СН3 – (СН2)3 – СН3. (5.7)
Иначе протекает реакция с шестичленными циклами. С этим же катализатором они, наоборот, дегидрируются с образованием ароматических соединений:
 |  |

 Рd, 300 оC + H2 . (5.8)
Рd, 300 оC + H2 . (5.8)
5.2.5. Галогенирование. Реакция галогенирования протекает по-разному в зависимости от величины цикла. При хлорировании циклопропана кольцо разрывается:

 + Сl2 CH2Cl – CH2 – CH2Cl. (5.9)
+ Сl2 CH2Cl – CH2 – CH2Cl. (5.9)
Циклобутан взаимодействует с хлором двояким образом:

 CH2Cl– (CH2)2 – CH2Cl (5.10)
CH2Cl– (CH2)2 – CH2Cl (5.10)

 + Cl2
+ Cl2
. CH – Cl + HCl (5.11)
Пяти- и шестичленные циклы вступают только в реакции замещения:


 + Сl2 CHCl + HCl. (5.12)
+ Сl2 CHCl + HCl. (5.12)
5.2.6. Реакция пербромирования открыта Густавссонном и Коноваловым. Протекает в присутствии АlВr3 в качестве катализатора. Она является качественной реакцией на циклоалканы, в том числе и гибридных структур.

 Br Br
Br Br
 AlBr3
AlBr3




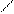
 СН3 + 8Вr2 Br CH3 + 11HBr. (5.13)
СН3 + 8Вr2 Br CH3 + 11HBr. (5.13)


Br Br
пентабромтолуол
5.2.7. Действие галогеноводородов. С ними реагирует только циклопропан и его гомологи:
 |
 + НВr BrСН2 – СН2 – СН3. (5.14)
+ НВr BrСН2 – СН2 – СН3. (5.14)
5.2.8. Термические реакции. Главными продуктами крекинга циклоалканов являются низшие алканы, алкены, алкадиены и водород. Незамещенные циклоалканы могут распадаться по следующим направлениям:

 3СН2 = СН2
3СН2 = СН2

 СН2 = СН – (СН2)3 – СН3
СН2 = СН – (СН2)3 – СН3



 СН2 = СН2 + СН2 = СН – СН2 – СН3 (5.15)
СН2 = СН2 + СН2 = СН – СН2 – СН3 (5.15)
 СН3 – СН3 + СН2 = СН – СН = СН2
СН3 – СН3 + СН2 = СН – СН = СН2
 |
 СН2 = СН – (СН2)2 – СН = СН2 + Н2.
СН2 = СН – (СН2)2 – СН = СН2 + Н2.
 Первичный распад исходной молекулы происходит с разрывом связи С– С и образованием бирадикала: С6Н12
Первичный распад исходной молекулы происходит с разрывом связи С– С и образованием бирадикала: С6Н12 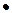 СН2 – (СН2)4 – СН2
СН2 – (СН2)4 – СН2 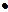 , который распадается на стабильные молекулы:
, который распадается на стабильные молекулы:
 3СН2 = СН2
3СН2 = СН2

 СН2 – (СН2)4 – СН2
СН2 – (СН2)4 – СН2 
СН2 = СН – (СН2)3 – СН3. (5.16)
Реакция (5.16) идет по нецепному механизму.
Алкилзамещенные циклоалканы распадаются по радикальноцепному механизму путем разрыва связи С – С в боковой цепи или обрыва радикала  СН 3 в случае метилпроизводных циклоалканов. Бициклические циклоалканы также подвергаются дециклизации, крекингу и дегидрированию.
СН 3 в случае метилпроизводных циклоалканов. Бициклические циклоалканы также подвергаются дециклизации, крекингу и дегидрированию.
5.2.9. Каталитические превращения циклоалканов.
а) в 1911 г. Н. Д. Зелинский открыл реакцию, названную его именем:

 Pt, Pd, Ni
Pt, Pd, Ni

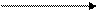 + 3H2; (5.17)
+ 3H2; (5.17)
250 – 300 оC
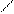
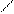

 CH3 катализатор СН3
CH3 катализатор СН3

 + 3Н2; (5.18)
+ 3Н2; (5.18)
температура
б) каталитическое диспропорционирование:



 Рt, Pd
Рt, Pd

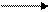 3 2 +; (5.19)
3 2 +; (5.19)
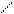


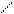
 CH = CH2 Pt, Pd C2H5 C2H5
CH = CH2 Pt, Pd C2H5 C2H5
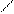
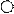
 3 2 +; (5.20)
3 2 +; (5.20)
в) перераспределение водорода между реагентами:

 Pt, Ni, Cu
Pt, Ni, Cu

 + 3R –CH = CH2 3 + 3R – CH2 – CH3; (5.21)
+ 3R –CH = CH2 3 + 3R – CH2 – CH3; (5.21)
г) внутримолекулярная изомеризация – перераспределение водорода на дегидрирующем катализаторе:





 Pt, Pd, Ni СH = CH2 CH2 – CH3. (5.22)
Pt, Pd, Ni СH = CH2 CH2 – CH3. (5.22)
винилциклогексан этилциклогексен
Дата публикования: 2014-11-02; Прочитано: 3161 | Нарушение авторского права страницы | Мы поможем в написании вашей работы!
